
把CO2通入NaOH溶液中,當生成Na2CO3和NaHCO3的物質的量之比為2:1時,CO2和NaOH的物質的量之比為( )
A.3:2 B.3:4 C.3:5 D.1:2
科目:高中化學 來源:2016-2017學年黑龍江大慶實驗中學高一12月月考化學卷(解析版) 題型:選擇題
下列說法正確的是
A.可用托盤天平稱取25.2gNaCl固體,也可用10mL量筒取5.20mL的鹽酸
B.失電子數越多的原子還原性越強
C.KMnO4→MnO2、H2S→SO2兩個變化過程均需要加入還原劑才能實現
D.飽和電解質溶液不一定比飽和非電解質溶液導電能力強
查看答案和解析>>
科目:高中化學 來源:2017屆河北省高三上調研四化學試卷(解析版) 題型:選擇題
向甲、乙、丙三個密閉容器中充入一定量的A和B,發生反應:A(g) + xB(g)  2C(g)。各容器的反應溫度、反應物起始量、反應過程中C的濃度隨時間變化關系分別以下表和下圖表示:
2C(g)。各容器的反應溫度、反應物起始量、反應過程中C的濃度隨時間變化關系分別以下表和下圖表示:

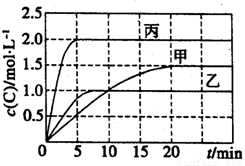
下列說法正確的是
A.10min內甲容器中反應的平均速率v(A)=0.025mol·L-1·min-1
B.由圖可知:T1<T2,且該反應為吸熱反應
C.若平衡時保持溫度不變,改變容器體積平衡不移動
D.T1℃,起始時甲容器中充入0.5molA、1.5molB,平衡時A的轉化率為25%
查看答案和解析>>
科目:高中化學 來源:2016-2017學年黑龍江省高一12月月考化學試卷(解析版) 題型:選擇題
a g Mg、Al合金完全溶解在C1 mol·L-1、V1L HCl溶液中,產生bmolH2。再向反應后的溶液中加入C2 mol·L-1、V2 L NaOH溶液,恰好使沉淀達到最大值,且沉淀質量為d g。下列關系錯誤的是( )
A.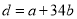 B.C1=C2V2/V1
B.C1=C2V2/V1
C.鋁為 (12b-a)/9 mol D.與金屬反應后剩余鹽酸為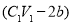 mol
mol
查看答案和解析>>
科目:高中化學 來源:2016-2017學年黑龍江省高一12月月考化學試卷(解析版) 題型:選擇題
下列離子方程式書寫正確的是( )
A.Na投入到水 中:Na+H2O═Na++OH-+H2↑
中:Na+H2O═Na++OH-+H2↑
B.AlCl3溶液中加入足量的氨水:Al3++4OH-═AlO2-+2H2O
C.三 氯化鐵溶液中加入銅粉:Fe3++Cu==Fe2++Cu2+
氯化鐵溶液中加入銅粉:Fe3++Cu==Fe2++Cu2+
D. 碳酸氫鈣溶液中滴加氫氧化鈉溶液至Ca2+恰好完全沉淀:Ca2++HCO3ˉ+OHˉ=CaCO3↓+H2O
查看答案和解析>>
科目:高中化學 來源:2017屆寧夏高三上月考四化學試卷(解析版) 題型:填空題
【化學——選修3:物質結構與性質】
請回答下列問題:
(1)寫出硅原子基態時的核外電子排布式:______________。硅元素位于元素周期表的第_________族。
(2)從晶體類型來看,金剛石屬于_________晶體。
(3)甲烷分子中碳原子的雜化方式為________。SO42-的空間構型為_______________。
(4)實驗測定HF的相對分子質量時,實驗測定值一般高于理論值的原因是______________。
(5)NaCl和CsCl熔點高的是 ,(填化學式)其主要原因是 。
(6)CaF2晶胞結構如圖所示,該晶體的密度為a g/cm3,則晶胞的體積是 (只要求列出算式)。
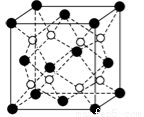
查看答案和解析>>
科目:高中化學 來源:2017屆江蘇省高三12月月考化學試卷(解析版) 題型:填空題
數十年來,化學工作者對碳的氧化物做了廣 泛深入的研究并取得了一些重要成果。如利用CO2和CH4重整可制合成氣(主要成分為CO、H2),已知重整過程中部分反應的熱化學方程式為:
泛深入的研究并取得了一些重要成果。如利用CO2和CH4重整可制合成氣(主要成分為CO、H2),已知重整過程中部分反應的熱化學方程式為:
I.CH4(g)=C(s)+2H2(g) ΔH= + 75.0 kJ·mol-1
II.CO2(g)+H2(g)=CO(g)+H2O(g) ΔH = + 41.0 kJ·mol-1
III.CO(g)+H2(g)=C(s)+H2O(g) ΔH = -131.0 kJ·mol-1
(1)反應CO2(g)+CH4(g)=2CO(g)+2H2(g)的ΔH = kJ·mol-1。
(2)固定n(CO2)=n(CH4),改變反應溫度,CO2和CH4的平衡轉化率見圖甲。
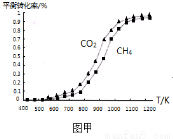
同溫度下CO2的平衡轉化率 (填“大于”或“小于”)CH4的平衡轉化率,其原因是 。
②高溫下進行該反應時常會因反應I生成“積碳”(碳單質),造成催化劑中毒,高溫下反應I能自發進行的原因是 。
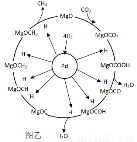
(3)一定條件下Pd-Mg/SiO2催化劑可使CO2“甲烷化”從而變廢為寶,其反應機理如圖乙所示,該反應的化學方程式為 。
(4)CO常用于工業冶煉金屬,右圖是在不同溫度下CO還原四種金屬氧化物達平衡后氣體中lg[c(CO)/c(CO2)]與溫度(t)的關系曲線圖。下列說法正確的是 。(填序號)
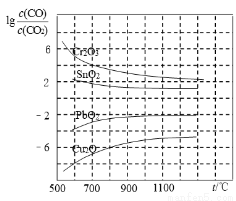
A.工業上可以通過增高反應裝置來延長礦石和CO接觸的時間,減少尾氣中CO的含量
B.CO不適宜用于工業冶煉金屬鉻(Cr)
C.工業冶煉金屬銅(Cu)時較低的溫度有利于提高CO的利用率
D.CO還原PbO2的反應ΔH>0
(5)在載人航天 器中應用電化學原理,以Pt為陽極,Pb(CO2的載體)為陰極,KHCO3溶液為電解質溶液,還原消除航天器內CO2同時產生O2和新的能源CO,總反應的化學方程式為:
器中應用電化學原理,以Pt為陽極,Pb(CO2的載體)為陰極,KHCO3溶液為電解質溶液,還原消除航天器內CO2同時產生O2和新的能源CO,總反應的化學方程式為: 2CO2
2CO2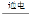 2CO+O2,則其陽極的電極反應式為 。
2CO+O2,則其陽極的電極反應式為 。
查看答案和解析>>
科目:高中化學 來源:2016-2017學年浙江省高一上期中化學試卷(解析版) 題型:選擇題
同溫同壓下,等物質的量的SO2和CO2相比較,下列敘述正確的是
A.質量比為11:16 B.密度比為11:16
C.體積比為11:16 D.分子個數比為1:1
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com