
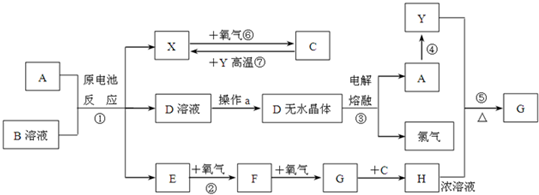
分析 C為無色液體,由氣體X(X由原電池反應得到,可能是H2)和氧氣反應得到,故C應是H2O,X是H2,根據反應⑦可知非金屬Y是C.由電解D無水晶體得到A與Cl2,可知D為氯化物且是離子化合物,結合A+B溶液發生原電池反應得到X、D、E,可知B為氯化物,且B是一種鹽,受熱極易分解,反應生成的H2與E氣體,B應水解呈酸性,由轉化關系:E→F→G→H,屬于常溫下氣體E的連續氧化得到氣體G,在中學階段中N、S元素化合物符合轉化關系,考慮反應①是金屬與NH4Cl溶液發生的原電池反應,可推出E為NH3、F為NO、G為NO2,則H為HNO3.(1)中反應④為A在某種氣體中燃燒,生成單質Y和A的氧化物,應為Mg與二氧化碳的反應,可推出A為Mg,則D為MgCl2,結合反應①可推知B為NH4Cl,驗證符合轉化關系,據此解答.
解答 解:C為無色液體,由氣體X(X由原電池反應得到,可能是H2)和氧氣反應得到,故C應是H2O,X是H2,根據反應⑦可知非金屬Y是C.由電解D無水晶體得到A與Cl2,可知D為氯化物且是離子化合物,結合A+B溶液發生原電池反應得到X、D、E,可知B為氯化物,且B是一種鹽,受熱極易分解,反應生成的H2與E氣體,B應水解呈酸性,由轉化關系:E→F→G→H,屬于常溫下氣體E的連續氧化得到氣體G,在中學階段中N、S元素化合物符合轉化關系,考慮反應①是金屬與NH4Cl溶液發生的原電池反應,可推出E為NH3、F為NO、G為NO2,則H為HNO3.(1)中反應④為A在某種氣體中燃燒,生成單質Y和A的氧化物,應為Mg與二氧化碳的反應,可推出A為Mg,則D為MgCl2,結合反應①可推知B為NH4Cl,驗證符合轉化關系,
(1)反應④為Mg與二氧化碳的反應生成MgO與碳,反應方程式為:2Mg+CO2$\frac{\underline{\;點燃\;}}{\;}$2MgO+C,
故答案為:2Mg+CO2$\frac{\underline{\;點燃\;}}{\;}$2MgO+C;
(2)Mg與石墨作電極,NH4Cl的濃溶液作電解質,構成原電池,Mg為負極,石墨為正極,負極反應:Mg-2e-=Mg2+,正極反應:2NH4++2e-=NH3↑+H2↑,
故答案為:Mg-2e-=Mg2+;2NH4++2e-=NH3↑+H2↑;
(3)從MgCl2溶液制備MgCl2的無水晶體,應注意防止水解,應將D溶液在HCl氣流中蒸干,
故答案為:將D溶液在HCl氣流中蒸干;
(4)反應②是氨的催化氧化,反應化學方程為:4NH3+5O2$\frac{\underline{催化劑}}{△}$4NO+6H2O;
故答案為:4NH3+5O2$\frac{\underline{催化劑}}{△}$4NO+6H2O;
(5)反應⑤是碳與濃硝酸反應生成CO2、NO2、H2O,方程式為:C+4HNO3(濃)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+4NO2↑+2H2O,
故答案為:C+4HNO3(濃)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+4NO2↑+2H2O.
點評 本題考查無機物的推斷、原電池、金屬鎂的性質、氮及其化合物的性質,側重于學生的分析能力和元素化合物知識的綜合運用的考查,為高考常見題型,注意把握題給信息,結合轉化關系進行推斷,(2)為易錯點,該原電池實質為銨根離子水解,Mg再與氫離子反應生成氫氣,難度中等.


科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 如圖所示裝置可用來制取和觀察Fe(OH)2在空氣中被氧化時顏色的變化.實驗時必須使用鐵屑和6mol/L的硫酸,其他試劑任選.填寫下列空白.
如圖所示裝置可用來制取和觀察Fe(OH)2在空氣中被氧化時顏色的變化.實驗時必須使用鐵屑和6mol/L的硫酸,其他試劑任選.填寫下列空白.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 .
.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 乙醇 | 溴乙烷 | 正丁醇 | 1-溴丁烷 | |
| 密度/g•cm-3 | 0.7893 | 1.4604 | 0.8098 | 1.2758 |
| 沸點/℃ | 78.5 | 38.4 | 117.2 | 101.6 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
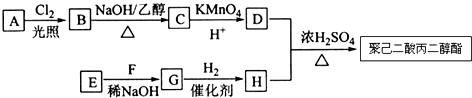
 .
. .
.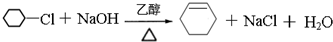 .
.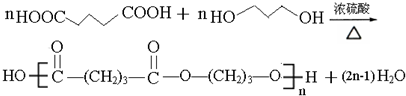 .
.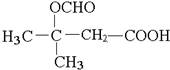 (寫出其中一種結構簡式).
(寫出其中一種結構簡式).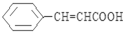 )的合成路線示意圖.
)的合成路線示意圖.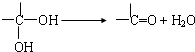
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 乙醇、乙酸都能與鈉反應 | |
| B. | 乙醇、乙酸互為同分異構體 | |
| C. | 乙醇、乙酸都是高分子化合物 | |
| D. | 乙醇、乙酸都能使紫色石蕊試液變紅色 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com