
分析 無色溶液中一定不含MnO4-;
①取適量試液,加入過量鹽酸,有氣體生成,并得到溶液,說明一定含CO32-、CO32-與Ba2+、Al3+反應產生沉淀,一定不含Ba2+,Al3+;
②在①所得溶液中加入HNO3酸化的AgNO3,出現白色沉淀,由于①中引入氯離子,故不能判斷此溶液中一定含有Cl-;
③取另一支試管,先加入過量的HCl酸化,再加入過量的NaHCO3溶液,有氣體生成同時析出白色沉淀甲,甲的質量為3.9g,說明溶液中一定含有AlO2-,沉淀甲為氫氧化鋁,且物質的量為0.05mol;
④在③所得溶液中加入過量的Ba(OH)2溶液,有白色沉淀乙析出,氫氧化鋇和過量的碳酸氫鈉溶液反應生成碳酸鋇沉淀,或者與原溶液中的硫酸根生成硫酸鋇沉淀,依據電中性原則得出,溶液中一定含有:Na+,據此解答即可.
解答 解:無色溶液中一定不含MnO4-;
①取適量試液,加入過量鹽酸,有氣體生成,并得到溶液,說明一定含CO32-、CO32-與Ba2+、Al3+反應產生沉淀,一定不含Ba2+,Al3+;
②在①所得溶液中加入HNO3酸化的AgNO3,出現白色沉淀,由于①中引入氯離子,故不能判斷此溶液中一定含有Cl-;
③取另一支試管,先加入過量的HCl酸化,再加入過量的NaHCO3溶液,有氣體生成同時析出白色沉淀甲,甲的質量為3.9g,說明溶液中一定含有AlO2-,沉淀甲為氫氧化鋁,且物質的量為0.05mol;
④在③所得溶液中加入過量的Ba(OH)2溶液,有白色沉淀乙析出,氫氧化鋇和過量的碳酸氫鈉溶液反應生成碳酸鋇沉淀,或者與原溶液中的硫酸根生成硫酸鋇沉淀,依據電中性原則得出,溶液中一定含有:Na+,
(1)溶液中一定不存在的離子是:Ba2+,Al3+,MnO4-,
故答案為:Ba2+,Al3+,MnO4-;
(2)依據分析可知:一定存在的是:Na+、AlO2-、CO32-,
故答案為:Na+、AlO2-、CO32-;
(3)向沉淀中加入過量HCl,全部溶解沉淀為碳酸鋇,部分溶解沉淀為碳酸鋇與硫酸鋇的混合物,
故答案為:向沉淀中加入過量HCl,全部溶解沉淀為碳酸鋇,部分溶解沉淀為碳酸鋇與硫酸鋇的混合物;
(4)碳酸根與氫離子反應生成二氧化碳氣體與水,偏鋁酸根與氫氣反應生成鋁離子和水,離子反應方程式為:CO32-+2H+=CO2↑+H2O,AlO2-+4H+=Al3++2H2O,
故答案為:CO32-+2H+=CO2↑+H2O;AlO2-+4H+=Al3++2H2O;
(5)依據分析可知:溶液中一定含有AlO2-,3.9g氫氧化鋁的物質的量為:$\frac{3.9g}{78g/mol}$=0.05mol,則原溶液中每份含AlO2-物質的量為0.05mol,則原溶液中含AlO2-物質的量0.1mol,
故答案為:AlO2-;0.1mol.
點評 本題考查了物質檢驗,離子反應的性質應用,反應現象的分析判斷,注意加入過量試劑的作用,題目難度中等.


 53天天練系列答案
53天天練系列答案科目:高中化學 來源: 題型:選擇題
| A. | 6:3:2 | B. | 1:2:3 | C. | 3:6:2 | D. | 2:1:3 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 蒸發結晶時,應使混合物中的水分完全蒸干后,才能停止加熱 | |
| B. | 過濾時,溶液的液面高于濾紙的邊緣 | |
| C. | 分液操作時,下層液體從分液漏斗下口放出后,再將上層液體從上口倒到另一個燒杯中 | |
| D. | 萃取操作時,應選擇有機萃取劑,且萃取劑的密度必須比水大 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
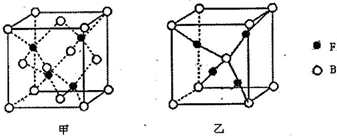
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 放熱的反應發生時不必加熱,吸熱反應都需要加熱后才能發生 | |
| B. | 化學反應的反應熱只與反應體系的始態和終點狀態有關,而與反應的途徑無關 | |
| C. | 化學反應一定有能量變化,當△H為“-”時,表示該反應為吸熱反應 | |
| D. | 已知C(s)+$\frac{1}{2}$O2(g)=CO(g)的反應熱為-110.5kJ/mol,說明碳的燃燒熱為110.5kJ/mol |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ③ | |||||
| 三 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | υ正(NH3)=υ正(H2S) | B. | υ正(NH3)=υ逆(H2S) | C. | υ逆(NH3)=υ逆(H2S) | D. | υ(NH3)=υ(H2S) |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
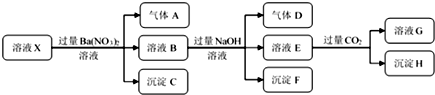
| A. | 若要確定溶液X中是否含有Fe3+,其操作為取少量原溶液于試管中,加入適量KSCN溶液,溶液變血紅色,則含有Fe3+ | |
| B. | 沉淀C為BaSO4,沉淀H為BaCO3,工業上往BaCO3中加入飽和的Na2CO3可以實現BaSO4的轉變 | |
| C. | 溶液中一定含有H+、Al3+、NH4+、Fe2+、SO42-、Cl- | |
| D. | 若溶液X為100 mL,產生的氣體A為112 mL(標況),則X中c(Fe2+)=0.05 mol•L-1 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com