
分析 (1)設出氧氣的物質的量,然后根據差量法及壓強關系列式計算出達到平衡時消耗氧氣的物質的量,然后計算出用O2的濃度變化來表示反應的化學反應速率;
(2)計算出反應消耗的二氧化硫的物質的量,再根據轉化率的表達式計算出二氧化硫的轉化率;
(3)計算出達到平衡時各組分的濃度,然后根據平衡常數的表達式計算出該溫度下該反應的平衡常數.
解答 解:設達到平衡時消耗氧氣的物質的量為x,
則:2SO2(g)+O2(g)?2SO3(g)△n
2 1 2 1
x x
達到平衡時氣體的總物質的量為:4mol+4mol-x=8mol-x,
壓強和物質的量成正比,則:$\frac{8mol-x}{8mol}$=80%,
解得:x=1.6mol,
(1)達到平衡時消耗氧氣的物質的量為1.6mol,用O2的濃度變化來表示反應的化學反應速率為:v(O2)=$\frac{\frac{1.6mol}{2L}}{5min}$=0.16mol/(L•min),
答:用O2的濃度變化來表示反應的化學反應速率為0.16mol/(L•min);
(2)二氧化硫的轉化率為:$\frac{3.2mol}{4mol}$×100%=80%,
答:SO2的轉化率為80%;
(3)達到平衡時,各組分的濃度為:c(SO2)=$\frac{4mol-1.6mol×2}{2L}$=0.4mol/L,c(O2)=$\frac{4mol-1.6mol}{2L}$=1.2mol/L,c(SO3)=$\frac{3.2mol}{2L}$=1.6mol/L,
該溫度下該反應的平衡常數為:K=$\frac{1.{6}^{2}}{0.{4}^{2}×1.2}$=$\frac{40}{3}$=13.3,
答:該溫度下該反應的平衡常數為13.3.
點評 本題考查了化學反應速率、化學平衡常數、轉化率等計算,題目難度中等,注意掌握化學反應速率、化學平衡常數的概念及計算方法,明確密閉容器中物質的量與壓強成正比的關系.


 新課標快樂提優暑假作業陜西旅游出版社系列答案
新課標快樂提優暑假作業陜西旅游出版社系列答案科目:高中化學 來源: 題型:選擇題
| A. | Al3+、S2-、Na+、Cl- | B. | K+、Fe3+、S2-、OH- | ||
| C. | Ba2+、HCO3-、Fe3+、H+ | D. | Na+、Al3+、SO42-、NO3- |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 鑒別方法 | Fe2+ | Fe3+ |
| 直接觀察色 | 淺綠色 | 棕黃色 |
| 與KSCN溶液 | 無現象 | 血紅色 |
| 金屬 | Ti | Mg | Cu |
| 金屬表面現象 | 放出氣泡速度緩慢 | 放出氣泡速度快 | 無變化 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | H2O、HCOOH、Cu2(OH)2CO3均含有氧元素,都是氧化物 | |
| B. | HClO、H2SO4(濃)、HNO3均具有氧化性,都是氧化性酸 | |
| C. | HF、HClO、NH3都易溶于水,都是電解質 | |
| D. | C2H2、H2CO3、H2SO4分子中均含有兩個氫原子,都是二元酸 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 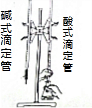 用HF標準溶液測定未知濃度的NaOH溶液 用HF標準溶液測定未知濃度的NaOH溶液 | |
| B. | 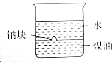 驗證密度:ρ(水)<ρ(鈉)<ρ(煤油) 驗證密度:ρ(水)<ρ(鈉)<ρ(煤油) | |
| C. | 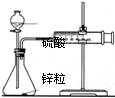 測定鋅與硫酸反應的速率 測定鋅與硫酸反應的速率 | |
| D. | 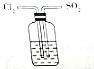 驗證SO2和Cl2等物質的量混合增強漂白效果 驗證SO2和Cl2等物質的量混合增強漂白效果 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com