
 .
. 分析 Ca(ClO)2+4HCl(濃)=CaCl2+2Cl2↑+2H2O中Cl元素的化合價由+1價降低為0,Cl元素的化合價由-1價升高為0,以此來解答.
解答 解:(1)濃鹽酸在反應中生成氯氣體現還原性,生成氯化鈣體現酸性,顯示出來的性質是B,故答案為:B;
(2)由反應可知生成2mol氯氣轉移2mol電子,則產生0.3mol Cl2,則轉移的電子的物質的量為0.3mol,
故答案為:0.3;
(3)此反應的離子反應方程式為ClO-+Cl-+2H+=Cl2↑+H2O,故答案為:ClO-+Cl-+2H+=Cl2↑+H2O;
(4)該反應轉移電子為2e-,用雙線橋法表示該氧化還原反應中電子轉移的方向和數目為 ,
,
故答案為: .
.
點評 本題考查氧化還原反應,為高頻考點,把握反應中元素的化合價變化為解答的關鍵,側重分析與應用能力的考查,注意電子轉移表示方法,題目難度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:解答題
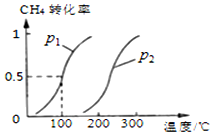 甲烷廣泛存在于天然氣、沼氣、煤礦坑氣之中,是優質的氣體燃料,更是制造許多化工產品的重要原料.
甲烷廣泛存在于天然氣、沼氣、煤礦坑氣之中,是優質的氣體燃料,更是制造許多化工產品的重要原料.查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
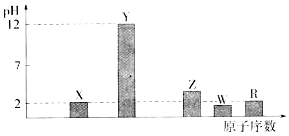
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
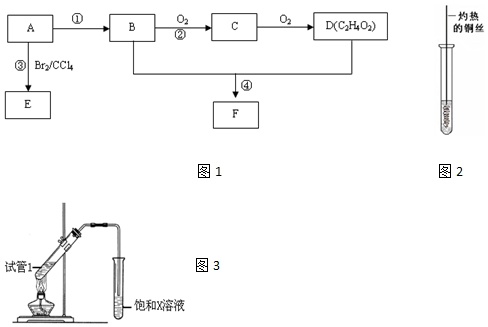
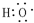 ,D中官能團為羧基(-COOH).
,D中官能團為羧基(-COOH). CH3COOCH2CH3+H2O.
CH3COOCH2CH3+H2O.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 稀硝酸與氫氧化鉀溶液反應:H++OH-=H2O | |
| B. | 鋁與稀鹽酸反應:Al+2H+=Al3++H2↑ | |
| C. | 三氯化鐵溶液與氫氧化鈉溶液反應:FeCl3+3OH-=Fe(OH)3↓+3Cl- | |
| D. | 足量二氧化碳與澄清石灰水反應:CO2+2OH-=CO32-+H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 電解NaCl飽和溶液,可制得金屬鈉 | |
| B. | 在海輪外殼上鑲入鋅塊,可減緩船體的腐蝕速率 | |
| C. | 尋找高效催化劑,利用太陽能分解水是制取氫氣的較理想方法 | |
| D. | MgO的熔點很高,可用于制作耐高溫材料 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 混合氣體的顏色不再改變 | B. | 混合氣體的密度不再改變 | ||
| C. | 混合氣體的壓強不再改變 | D. | 混合氣體的平均分子質量不再改變 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com