
【題目】實驗室中有一未知濃度的稀鹽酸,某同學為測定該鹽酸的濃度,在實驗室中進行了如下實驗。
(1)配制100 mL 0.10 mol/L NaOH標準溶液。
①主要操作步驟:計算→稱量→溶解→冷卻→轉移→洗滌(并將洗滌液移入容量瓶)→振蕩→_________→__________→裝瓶→貼標簽。
②稱量________g氫氧化鈉固體粉末,所需儀器有:托盤天平(帶砝碼和鑷子)、___________、小燒瓶。
(2)取20.00 mL待測鹽酸溶液放入錐形瓶中,并滴加2~3滴酚酞作指示劑,用自己配制的標準液NaOH溶液進行滴定。重復上述滴定操作2~3次,記錄數據如下:
實驗 編號 | NaOH溶液的濃度(mol/L) | 滴定完成時,NaOH溶液滴入的體積(mL) | 待測鹽酸溶液的體積(mL) | |
1 | 0.10 | 29.80 | 20.00 | |
2 | 0.10 | 30.00 | 20.00 | |
3 | 0.10 | 30.20 | 20.00 |
①滴定達到終點的標志是___________________________。
②根據上述數據,可計算出該鹽酸的濃度約為_______(保留兩位有效數字)。
③排去堿式滴定管中氣泡的方法應采用如圖所示操作中的____________(選擇甲、乙、丙填空),然后輕輕擠壓玻璃球使尖嘴部分充滿堿液。
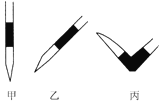
④在上述實驗中,下列操作(其他操作正確)會造成測定結果偏高的有_______。
A.滴定終點讀數時俯視讀數
B.酸式滴定管使用前,水洗后未用待測鹽酸溶液潤洗
C.錐形瓶水洗后未干燥
D.滴定過程中,有少量標準液濺出錐形瓶外
E.堿式滴定管尖嘴部分有氣泡,滴定后消失
【答案】定容 搖勻 0.4 藥匙 最后加入一滴NaOH溶液,溶液由無色恰好變成淺紅色且半分鐘內淺紅色不褪去 0.15mol/L 丙 DE
【解析】
(1)溶液配制主要操作步驟:計算→稱量→溶解→冷卻→轉移→洗滌(并將洗滌液移入容量瓶)→振蕩→定容→搖勻→裝瓶→貼標簽;根據![]() 來計算;根據稱量氫氧化鈉固體所需儀器進行解答;
來計算;根據稱量氫氧化鈉固體所需儀器進行解答;
(2)①如溶液顏色變化且半分鐘內不變色,可說明達到滴定終點;
②根據滴定消耗的標準液的體積判斷數據的有效性,然后計算出標準液的平均體積,最后根據標![]() 計算出該鹽酸的濃度;
計算出該鹽酸的濃度;
③堿式滴定管的氣泡通常橡皮管內,只要將滴定玻璃頭朝上,并擠橡皮管中的玻璃珠就可以將氣泡沖排出;
④根據![]() 分析不當操作對V(標準)的影響,以此判斷濃度的誤差。
分析不當操作對V(標準)的影響,以此判斷濃度的誤差。
(1)①配制100mL 0.10mol/L NaOH標準溶液的步驟為:計算→稱量→溶解→(冷卻后)轉移→洗滌(并將洗滌液移入容量瓶)→定容→搖勻→將配制好的溶液倒入試劑瓶中,貼上標簽,
故答案為:定容;搖勻;
②需要的氫氧化鈉的質量m=nM=cVM=0.1L×0.10molL-1×40g/mol=0.4g;稱量0.4g氫氧化鈉固體所需儀器,需要稱量儀器天平(帶砝碼、鑷子),氫氧化鈉具有腐蝕性,應該放在燒杯中稱量,還需要取氫氧化鈉的儀器藥匙;
故答案為:0.4;藥匙;
(2)①滴定結束前鹽酸中滴入酚酞,溶液為無色,滴定結束時氫氧化鈉過量,溶液變成紅色,所以滴定終點現象為:最后一滴氫氧化鈉溶液加入,溶液由無色恰好變成淺紅色,且半分鐘內淺紅色不褪去;
故答案為:最后加入一滴NaOH溶液,溶液由無色恰好變成淺紅色且半分鐘內淺紅色不褪去;
②三次滴定數據都是有效的,消耗標準液的平均體積為:![]() ,該鹽酸的濃度為:
,該鹽酸的濃度為: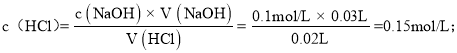
故答案為:0.15mol/L;
③堿式滴定管的氣泡通常橡皮管內,只要將滴定玻璃頭朝上,并擠橡皮管中的玻璃珠就可以將氣泡沖排出;
故答案為:丙;
④A.滴定終點讀數時俯視讀,造成V(標準)偏小,根據![]() 分析,可知c(待測)偏小,故A錯誤;
分析,可知c(待測)偏小,故A錯誤;
B.酸式滴定管使用前,水洗后未用待測鹽酸潤洗,待測液被稀釋,其物質的量偏小,造成V(標準)偏小,根據![]() 分析,可知c(待測)偏小,故B錯誤;
分析,可知c(待測)偏小,故B錯誤;
C.錐形瓶水洗后未干燥,待測液的物質的量不變,對V(標準)無影響,根據![]() 分析,可知c(待測)不變,故C錯誤;
分析,可知c(待測)不變,故C錯誤;
D. 滴定過程中,有少量標準液濺出錐形瓶外導致V(標準)偏大,根據![]() 分析,可知c(待測)偏大,故D正確;
分析,可知c(待測)偏大,故D正確;
E.滴定前滴定管尖嘴處有氣泡,滴定后氣泡消失,造成V(標準)偏大,根據![]() 分析,可知c(待測)偏大,故E正確;
分析,可知c(待測)偏大,故E正確;
故選DE。


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:
【題目】“太陽水”電池裝置如圖所示,該電池由三個電極組成,其中a為TiO2電極,b為Pt電極,c為WO3電極,電解質溶液為pH=3的Li2SO4-H2SO4溶液。鋰離子交換膜將電池分為A、B兩個區,A區與大 氣相通,B區為封閉體系并有N2保護。下列關于該電池的說法錯誤的是( )
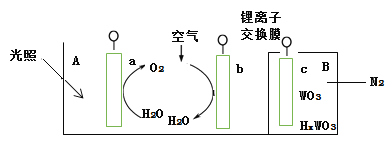
A.若用導線連接a、c,則a為負極,該電極附近pH減小
B.若用導線連接a、c,則c電極的電極反應式為HxWO3 - xe- =WO3 + xH+
C.若用導線先連接a、c,再連接b、c,可實現太陽能向電能轉化
D.若用導線連接b、c, b電極的電極反應式為O2+4H++4e-=2H2O
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】碳酸亞乙酯是一種重要的添加劑,其結構簡式為![]() 。用環氧乙烷合成碳酸亞乙酯的反應為:
。用環氧乙烷合成碳酸亞乙酯的反應為:![]() +CO2
+CO2![]() 。下列說法錯誤的是( )
。下列說法錯誤的是( )
A.上述反應屬于加成反應
B.碳酸亞乙酯的所有二氯代物中均存在手性碳原子
C.碳酸亞乙酯中的所有氧原子處于同一平面內
D.1mol碳酸亞乙酯最多可消耗2molNaOH
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知R-CH=CH2+HX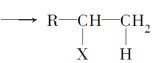 ,且CH3CH2OH
,且CH3CH2OH![]() CH2=CH2。A、B、C、D、E有如下轉化關系:
CH2=CH2。A、B、C、D、E有如下轉化關系:
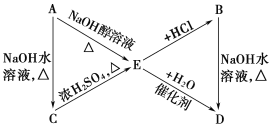
其中A、B是分子式均為C3H7Cl的兩種同分異構體。根據圖中各物質的轉化關系,填寫下列空白:
(1)A、B的結構簡式:A________、B________。
(2)完成下列反應的化學方程式:
①A→E_____________________;
②B→D____________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】我們利用物質的結構與性質對周期表進行研究,有助于我們更好地掌握同類知識。
(1)基態砷原子中,價電子占用__個原子軌道;雌黃分子式為As2S3,分子結構如圖,則砷原子的雜化方式為__。

(2)向CuSO4溶液中加入少量氨水生成藍色沉淀,繼續加入過量氨水沉淀溶解,得到深藍色透明溶液,最后向該溶液中加入一定量乙醇,析出[Cu(NH3)4]SO4·H2O晶體;該晶體所含的非金屬元素中,N、O、S第一電離能由大到小的順序是__(填元素符號),SO42-的空間構型為__,晶體中含有的化學鍵有__。加入乙醇后析出[Cu(NH3)4]SO4·H2O晶體的原因是__。
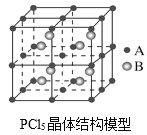
(3)常溫下PCl5是一種白色晶體,其立方晶系晶體結構模型如圖所示,由A、B兩種微粒構成。將其加熱至148℃熔化,形成一種能導電的熔體。已知A微粒與CCl4具有相同的空間構型和相似的化學鍵特征,則A為__,B為__。
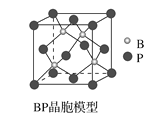
(4)磷化硼(BP)是一種超硬耐磨涂層材料,如圖為其立方晶胞。已知晶體中最近的硼原子和磷原子核間距為xcm,磷化硼的摩爾質量為bg·mol-1,阿伏加德羅常數為NA,則磷化硼晶體密度的表達式為__g·cm-3。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】20℃時,用0. 1mol/L 鹽酸滴定20mL 0. 1mol/L 氨水的圖像如圖所示,下列說法正確的是
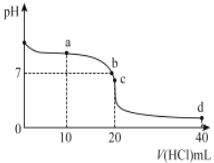
A.a點時2c(Cl-)=c(NH3H2O)+c (NH4+)
B.b點表示酸堿恰好完全反應
C.c點時c(NH4+)>c(Cl-)>c(H+ )>c(OH- )
D.a 、b、c、d均有c(NH4+)+c(H+) = c(Cl-)+c(OH-)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知:2H2O(l)=2H2(g)+O2(g) △H=+571.0 kJ/mol。以太陽能為熱源分解Fe3O4,經熱化學鐵氧化合物循環分解水制H2的過程如下:
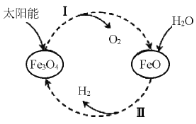
過程I:2Fe3O4(s)=6FeO(s)+O2(g) △H=+313.2 kJ/mol
過程II:……
下列說法不正確的是
A.過程I中每消耗232gFe3O4轉移2mol電子:
B.過程II熱化學方程式為:3FeO(s)+H2O(l)=H2(g)+Fe3O4(s) △H=+128.9 kJ/mol
C.過程I、II中能量轉化的形式依次是:太陽能→化學能→熱能
D.過程I中正反應的活化能大于逆反應的活化能
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】水是生命之源,萬物之基。不僅如此,水在化學中的作用也不可忽視。
I.常溫下,濃度均為0.l mol·L-1的下列五種水溶液的pH如下表:
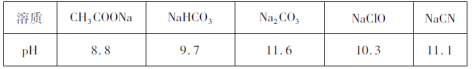
(1)上述鹽溶液中的陰離子,結合質子能力最強的是__________。
(2)根據表中數據判斷,濃度均為0.01 mol·L-1的下列四種物質的溶液中,酸性最弱的是__________;將各溶液分別加水稀釋100倍,pH變化最大的是__________(填字母)。
A.HCN B.HClO C.H2CO3 D.CH3COOH
(3)要增大氯水中HClO的濃度,可向氯水中加入少量的碳酸鈉溶液,反應的離子方程式為__。
II.已知水在25℃和95℃時,其電離平衡曲線如圖所示:
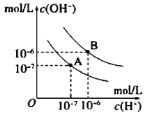
(1)95℃時水的電離平衡曲線應為__________(選填“A”或“B”);
(2)25℃時,將pH=10的NaOH溶液與pH=6的鹽酸溶液混合,若所得混合溶液的pH=7,則NaOH溶液與鹽酸溶液的體積比為__________;
(3)95℃時,若1體積pH=a的某強酸溶液與10x體積pH=b的某強堿溶液混合后溶液呈中性,則混合前,a與b之間應滿足的關系是__________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】以太陽能為熱源,熱化學硫碘循環分解水是一種高效、無污染的制氫方法,其流程如下圖所示。已知向反應中得到的產物中加過量I2會得到兩層溶液——含低濃度I2的H2SO4層和含高濃度I2的HI層,這兩層分別進行反應Ⅱ和Ⅲ,循環分解制氫。下列說法錯誤的是( )
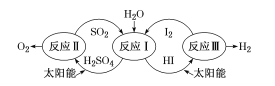
A.反應I的化學方程式為 SO2+2H2O+I2=H2SO4+2HI
B.該流程將太陽能轉化為化學能,且降低了水分解制氫的活化能
C.H2SO4層和HI層在加I2之前和加I2之后均分成兩層,且兩層密度、顏色均不相同
D.SO2和I2是反應 2H2O =2H2+O2的催化劑
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com