
二硫化亞鐵是Li/FeS2電池的正極活性物質,可用水熱法合成。FeSO4、Na2S2O3、S及H2O在200 ℃連續反應24 h,四種物質以等物質的量反應,再依次用CS2、H2O洗滌、干燥及晶化后得到。
(1)合成FeS2的離子方程式為_____________________________________。
(2)用水洗滌時,如何證明SO42—已除盡?________________________________________。
(3)已知1.20 g FeS2在O2中完全燃燒生成Fe2O3和SO2氣體放出8.52 kJ熱量,FeS2燃燒反應的熱化學方程式為__________________________。
(4)取上述制得的正極材料1.120 0 g(假定只含FeS一種雜質),在足量的氧氣流中充分加熱,最后得0.800 0 g紅棕色固體,試計算該正極材料中FeS2的質量分數(寫出計算過程)。
(1)Fe2++S2O32—+S+H2O FeS2+2H++SO42—
FeS2+2H++SO42—
(2)取少許最后一次洗滌濾液,先用足量鹽酸酸化,再向上述清液中滴加BaCl2溶液,若不出現白色渾濁,表示已洗滌干凈
(3)4FeS2(s)+11O2(g)=2Fe2O3(s)+8SO2(g) ΔH=-3 408 kJ·mol-1
[或FeS2(s)+ O2(g)=
O2(g)= Fe2O3(s)+2SO2(g)] ΔH=-852 kJ·mol-1
Fe2O3(s)+2SO2(g)] ΔH=-852 kJ·mol-1
(4)解:120n(FeS2)+88n(FeS)=1.120 0
n(FeS2)+n(FeS)=
n(FeS2)=0.007 5 mol
w(FeS2)= ≈0.803 6
≈0.803 6
【解析】 (1)由題中信息可寫出四種反應物,再由原子守恒和電荷守恒寫出產物,Na2S2O3中一個S顯+6價,一個S顯-2價,其中-2的S與單質S發生歸中反應,根據得失電子守恒配出反應。(2)檢驗SO42—,需要先用鹽酸除去干擾離子,以防生成除BaSO4以外的鋇鹽沉淀。(3)0.01 mol FeS2完全燃燒放出8.52 kJ的熱量。寫熱化學方程式要標注物質的狀態,同時ΔH應與化學計量系數成比例。(4)由質量關系,列出120n(FeS2)+88n(FeS)=1.120 0,由鐵原子守恒列出n(FeS2)+n(FeS)= mol,聯合解得FeS2的物質的量,進而求出其含量。
mol,聯合解得FeS2的物質的量,進而求出其含量。


科目:高中化學 來源:2013-2014學年高考化學二輪復習江蘇專用 第8講電化學練習卷(解析版) 題型:選擇題
下圖是某同學設計的原電池裝置,下列敘述中正確的是( )。

A.電極Ⅰ上發生還原反應,做原電池的正極
B.電極Ⅱ的電極反應式為Cu2++2e-=Cu
C.該原電池的總反應式為2Fe3++Cu=Cu2++2Fe2+
D.鹽橋中裝有含氯化鉀的瓊脂,其作用是傳遞電子
查看答案和解析>>
科目:高中化學 來源:2013-2014學年高考化學二輪復習江蘇專用 第5講化學反應與能量練習卷(解析版) 題型:選擇題
已知下列反應的熱化學方程式:
6C(s)+5H2(g)+3N2(g)+9O2(g)=2C3H5(ONO2)3(l) ΔH1
2H2(g)+O2(g)=2H2O(g) ΔH2
C(s)+O2(g)=CO2(g) ΔH3
則反應4C3H5(ONO2)3(l)=12CO2(g)+10H2O(g)+O2(g)+6N2(g)的ΔH為( )。
A.12ΔH3+5ΔH2-2ΔH1 B.2ΔH1-5ΔH2-12ΔH3
C.12ΔH3-5ΔH2-2ΔH1 D.ΔH1-5ΔH2-12ΔH3
查看答案和解析>>
科目:高中化學 來源:2013-2014學年高考化學二輪復習江蘇專用 第3講兩種重要的化學反應練習卷(解析版) 題型:填空題
某廠的酸性工業廢水中含有一定量的Na+、Al3+、 Fe3+、Cu2+、Cl-。該廠利用如圖所示的工藝流程圖,利用常見的氣體氧化物、酸、堿和工業生產中的廢鐵屑,從廢水中生產出了氯化鐵、氧化鋁、NaCl晶體和金屬銅,產生了很好的社會經濟效益。

請填寫下列空白:
(1)圖中試劑1是________,試劑2是________。
(2)步驟1和步驟2所用到的玻璃儀器是________。
(3)步驟1反應的離子方程式為_______________________________________。
(4)步驟3反應的離子方程式為_______________________________________。
(5)從節約藥品和環保方面考慮,步驟5所發生反應的離子方程式應為__________________________________________________________。
查看答案和解析>>
科目:高中化學 來源:2013-2014學年高考化學二輪復習江蘇專用 第3講兩種重要的化學反應練習卷(解析版) 題型:選擇題
在水溶液中能大量共存的一組離子是( )。
A.Na+、Ba2+、Cl-、NO3— B.Pb2+、Hg2+、S2-、SO42—
C.NH4+、H+、S2O32—、PO43— D.Ca2+、Al3+、Br-、CO32—
查看答案和解析>>
科目:高中化學 來源:2013-2014學年高考化學二輪復習江蘇專用 第2講化學常用計量練習卷(解析版) 題型:選擇題
用固體樣品配制一定物質的量濃度的溶液,需經過稱量、溶解、轉移溶液、定容等操作。下列圖示對應的操作規范的是( )。
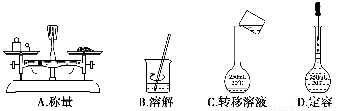
查看答案和解析>>
科目:高中化學 來源:2013-2014學年高考化學二輪復習江蘇專用 第1講物質的組成性質和分類練習卷(解析版) 題型:填空題
分類法是學習化學的重要方法,人們在認識事物時可采用多種分類方法。下表各組歸類
序號分類標準歸類
AFeSO4、NO2、MnO2、NaClO、Cu3P、Na2O2H2SO3
BCH3COOH、HOOC—COOH、HClO、H2SHF
C復分解反應、電解反應、放熱反應、離子反應焰色反應
D(NH4)2SO4、NH4Cl、NH4NO3、NH3·H2ONH4HCO3
(1)A中分類標準是_____________________,H2SO3________(填“是”或“否”)可歸為此類。
(2)B中分類標準是_________________________,HF________(填“是”或“否”)可歸為此類。
(3)C中分類標準是__________________,焰色反應屬于________變化。
(4)D中分類標準是__________________,NH4HCO3________(填“是”或“否”)可歸為此類。
查看答案和解析>>
科目:高中化學 來源:2013-2014學年高考化學二輪復習江蘇專用 第14講物質結構與性質練習卷(解析版) 題型:填空題
Ⅰ.下列化合物中,含有非極性共價鍵的離子化合物是( )。
A.CaC2 B.N2H4 C.Na2S2 D.NH4NO3
Ⅱ.圖A所示的轉化關系中(具體反應條件略),a、b、c和d分別為四種短周期元素的常見單質,其余均為它們的化合物,i的溶液為常見的酸,a的一種同素異形體的晶胞如圖B所示。

回答下列問題:
(1)圖B對應的物質名稱是________,其晶胞中的原子數為________,晶體類型為________。
(2)d中元素的原子核外電子排布式為________。
(3)圖A中由二種元素組成的物質中,沸點最高的是________,原因是________________________________________________________________________,該物質的分子構型為________,中心原子的雜化軌道類型為________。
(4)圖A中的雙原子分子中,極性最大的分子是________。
(5)k的分子式為________,中心原子的雜化軌道類型為________,屬于________分子(填“極性”或“非極性”)。
查看答案和解析>>
科目:高中化學 來源:2013-2014學年高考化學二輪復習江蘇專用 第10講金屬元素及其化合物練習卷(解析版) 題型:選擇題
下列轉化關系在給定條件下不能實現的是( )。

A.①②③ B.②③⑤ C.③④⑤ D.①②③④
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com