
【題目】下列對實驗事實的解釋錯誤的是( )
選項 | 實驗事實 | 解釋 |
A | 實驗室用粗鋅與稀鹽酸反應制H2比純鋅快 | 粗鋅與稀鹽酸構成原電池 |
B | 濃硝酸保存在棕色試劑瓶中 | 4HNO3 |
C | 向10mL0.2mol·L-1ZnSO4,溶液中加入10mL0.4mol·L-1Na2S溶液,產生白色沉淀,再滴加CuSO4溶液,沉淀變黑 | Ksp(CuS)<Ksp(ZnS) |
D | 做過銀鏡反應的試管可用鐵鹽溶液洗滌,加入稀鹽酸,清洗效果更好 | Fe3++Ag |
A.AB.BC.CD.D
【答案】C
【解析】
A. 實驗室用粗鋅與稀鹽酸反應制H2比純鋅快,粗鋅與稀鹽酸構成原電池,原電池加快反應速率,故A正確;
B. 濃硝酸保存在棕色試劑瓶中,主要是濃硝酸在光照或加熱條件下反應生成H2O、NO2和O2,故B正確;
C. 向10mL 0.2 molL1 ZnSO4溶液中加入10mL 0.4 molL1 Na2S溶液,產生白色沉淀,溶液中剩余Na2S溶液,再滴加CuSO4溶液,生成CuS黑色沉淀,不能得出Ksp(CuS)<Ksp(ZnS),故C錯誤;
D. 做過銀鏡反應的試管可用鐵鹽溶液洗滌,Fe3++Ag![]() Fe2++Ag+,加入鹽酸,Ag+與Cl-結合成氯化銀沉淀,平衡右移,因此清洗效果更好,故D正確。
Fe2++Ag+,加入鹽酸,Ag+與Cl-結合成氯化銀沉淀,平衡右移,因此清洗效果更好,故D正確。
綜上所述,答案為C。


 53隨堂測系列答案
53隨堂測系列答案科目:高中化學 來源: 題型:
【題目】現有某鐵碳合金,某化學興趣小組為了測定鐵碳合金中鐵的質量分數,并探究濃硫酸的還原產物,設計了如圖所示的實驗裝置和實驗方案(夾持儀器已省略),請你參與此項活動并回答相應問題:
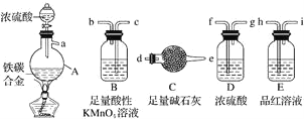
(1)該裝置的連接順序a___(填接口字母),連接好裝置后,首先應進行的操作是____。
(2)mg鐵碳合金中加入濃H2SO4,點燃酒精燈一段時間后,用滴管吸取A中的溶液滴入到適量水中作為試樣,試樣中所含金屬離子的成分有以下三種可能:A:只含有Fe3+;B:只含有Fe2+;C:____,若為A,則A中反應的化學方程式為___,驗證C種可能的實驗方法___。
(3)待A中不再逸出氣體時,停止加熱,拆下C并稱重,C增重bg。鐵碳合金中鐵的質量分數____(寫表達式)。
(4)某同學認為利用此裝置測得鐵的質量分數偏大,請你寫出可能的原因:_____。
(5)隨著反應的進行,A中還可能發生某些離子反應。寫出相應的離子方程式____。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在沸水中逐滴加入5~6滴FeCl3飽和溶液,繼續煮沸至溶液呈紅褐色。下列正確的是
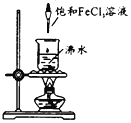
A.在暗處用激光筆照射液體,會出現一條光亮的通路
B.可用濾紙分離提純得到氫氧化鐵膠體
C.所得膠體中分散質的粒子直徑大于100nm
D.取適量液體置于U型管,并通直流電,陽極顏色加深
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某實驗小組同學為了測定工業純堿的純度,進行了一系列實驗。
(1)和索氏制堿法相比,侯氏制堿法的優勢有___________________________________;
(2)工業純堿中常含有少量NaCl雜質,解釋原因__________________________,檢驗是否含有氯化鈉雜質的方法為__________________________________________________________;
(3)使用重量法測定純堿的純度,用到的試劑有__________________________________;
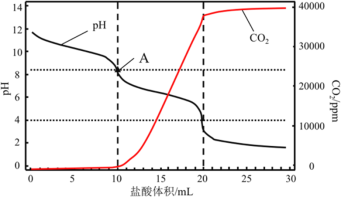
(4)使用滴定法測定純堿的純度,用_________________(填儀器名稱)稱量1.200g工業純堿樣品,溶解,用1mol/L鹽酸做標準液,滴定過程中溶液pH變化和生成CO2的量如圖所示,A點溶液呈堿性的原因______________________________________________________,計算該工業純堿樣品的質量分數_______________。(計算結果保留兩位小數)
 。
。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】體NH4Br置于密閉容器中,在某溫度下,發生反應:NH4Br(s)![]() NH3(g)+HBr(g),2HBr(g)
NH3(g)+HBr(g),2HBr(g)![]() Br2(g)+H2(g),2 min后,測知H2的濃度為0.5 mol·L-1,HBr的濃度為4 mol·L-1,若上述反應速率用v(NH3)表示,則下列速率正確的是( )
Br2(g)+H2(g),2 min后,測知H2的濃度為0.5 mol·L-1,HBr的濃度為4 mol·L-1,若上述反應速率用v(NH3)表示,則下列速率正確的是( )
A. 0.5 mol·L-1·min-1B. 2.5 mol·L-1·min-1
C. 2 mol·L-1·min-1D. 1.25 mol·L-1·min-1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知A為淡黃色固體,T為生活中使用最廣泛的金屬單質,D是具有磁性的黑色晶體,C是無色無味的氣體,H是白色沉淀。
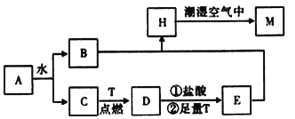
(1)物質D的化學式為 ________。
(2)A和水反應生成B和C的離子方程式為____________________,列出A的一種重要用途_________________。
(3)H在潮濕空氣中變成M的實驗現象是______________________。
(4)反應①的離子方程式為_______________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】我國許多城市為了減少燃煤造成的大氣污染,對煤做了多方面的改進:
(1)為了除去煤中的含硫化合物,采用FeCl3脫硫,即用FeCl3溶液浸洗煤粉,發生反應如下:FeS2+14FeCl3+8H2O====2FeSO4+13FeCl2+16HCl(已知FeS2中硫元素的化合價為-1價)。
①該反應的氧化劑是____,若有1 mol FeS2被除去,則發生轉移的電子的物質的量是___________。
②為了充分利用Fe2+并減少酸(HCl)污染,本方法中可利用工業廢鐵屑和Cl2讓廢液重新生成FeCl3。請寫出這一過程中有關的離子方程式:______________;_____________________。
(2)“保護環境,就是保護人類自己”。飄塵是物質燃燒時產生的粒狀漂浮物,顆粒很小,不易沉降,它與空氣的污染物二氧化硫(SO2)接觸時,二氧化硫(SO2)會部分轉化為三氧化硫(SO3),其污染更加嚴重。
①飄塵所起的作用可能是______________.
A. 氧化劑B.還原劑C.催化劑D.載體
發生反應的化學方程式為________________________________________________.(如果是氧化還原反應,請用雙線橋標出電子轉移的方向和數目)
②冶金工業中常用高壓電對氣溶膠作用,以除去飄塵,減少對空氣的污染,這種做法的依據是___.
A. 布朗運動 B.丁達爾現象 C. 滲析 D. 電泳。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】CO2的資源化利用能有效減少CO2排放,又能緩解能源危機。實現CO2資源化再利用的研究工作正在不斷進行中。
(1)CO2和H2,合成CH3OH,用非金屬催化劑實現CO2電催化還原制備甲醇的反應歷程如圖所示:
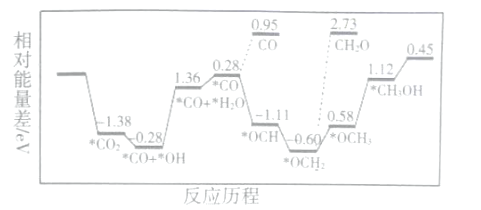
上述合成甲醇的反應速率較慢,要使反應速率加快,主要降低下列變化中___ (填字母)的能量變化。
A.*CO+*OH→*CO+*H2O B.*CO→*OCH
C. *OCH2→*OCH3 D.*OCH3→*CH3OH
(2)CO2和H2合成甲酸(HCOOH)其反應為:H2(g)+CO2(g)![]() HCOOH(g)。一定溫度下,恒容密閉容器中進行上述反應,測得v正(CO2)隨反應時間(t)的變化如圖所示。
HCOOH(g)。一定溫度下,恒容密閉容器中進行上述反應,測得v正(CO2)隨反應時間(t)的變化如圖所示。
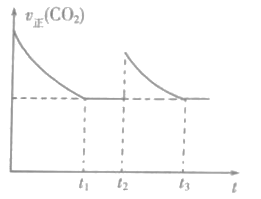
①t2時,改變的條件是充入amolCO2,同時___。
②下列關于t1、t3時刻的說法,正確的是___。
a.平衡常數:K1>K3
b.混合氣的平均分子量:![]() <
<![]()
c.混合氣中HCOOH的體積分數:V1=V3
③標準平衡常數Kθ=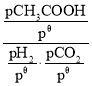 ,其中pθ為標準壓強(1×105Pa),pH2、pCO2和pHCOOH為各組分的平衡分壓,如pCO2=pxCO2,p為平衡總壓,xCO2為平衡系統中CO2的物質的量分數。在標準壓強下,向上述容器充入等物質的量的H2和CO2進行反應,測得HCOOH的平衡產率為w,則K=___(用含w字母表示)。
,其中pθ為標準壓強(1×105Pa),pH2、pCO2和pHCOOH為各組分的平衡分壓,如pCO2=pxCO2,p為平衡總壓,xCO2為平衡系統中CO2的物質的量分數。在標準壓強下,向上述容器充入等物質的量的H2和CO2進行反應,測得HCOOH的平衡產率為w,則K=___(用含w字母表示)。
(3)O2輔助的Al~CO2電池工作原理如圖所示。該電池電容量大,能有效利用CO2,電池反應產物Al2(C2O4)3是重要的化工原料。
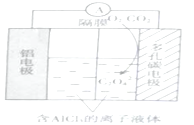
電池正極區發生的反應:①O2+e-=O2-;②___,O2的作用是___。
(4)CH4超干重整CO2得到的CO經偶聯反應可制得草酸(H2C2O4)。常溫下,向某濃度的草酸溶液中加入一定濃度的KOH溶液,所得溶液的pH=3,則![]() =___。
=___。
(已知常溫下H2C2O4的Ka1=6×10-2,Ka2=6×10-5)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】二氧化氯(ClO2)是一種黃綠色到橙黃色的氣體,是國際上公認的安全、無毒的綠色消毒劑。已知:工業上制備二氧化氯的方法之一是用甲醇在酸性介質中與氯酸鈉反應。二氧化氯能與許多化學物質發生爆炸性反應,遇水則生成次氯酸、氯氣和氧氣。
完成下列填空:
(1)將二氧化氯通入品紅試液中,看到的現象是__;理由是__。
(2)請配平下列反應的化學方程式(CH3OH中H為+1價,O為-2價):
___CH3OH+__NaClO3+__→__CO2↑+__C1O2↑+__Na2SO4+__□__
(3)該反應中,被氧化的元素是__。還原產物與氧化產物的物質的量之比是__。
(4)根據上述反應可推知__。
a.氧化性:C1O2>NaClO3 b.氧化性:NaClO3>CH3OH
c.還原性:CH3OH>ClO2 d.還原性:CH3OH>Na2SO4
(5)若轉移的電子數目為0.3NA(NA為阿伏加德羅常數),則反應產生氣體(標準狀況)為__升。
(6)消毒效率常以單位質量的消毒劑得到的電子數表示。ClO2的消毒效率是Cl2的__倍。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com