

分析 (1)二氧化錳與濃鹽酸在加熱條件下反應生成氯氣、氯化錳、水;
(2)A中濃鹽酸和二氧化錳在加熱條件下發生反應生成Cl2,Ⅰ中b瓶是用來貯存Cl2的,則應選用一種Cl2在其中溶解度非常小的液體,一般選用飽和食鹽水;
(3)Ⅱ與Ⅰ原理相同,而Ⅲ中因c瓶口密封,不能氣體流通;
(4)①a依據氯氣黃綠色的物理性質判斷;
②b氯氣具有強的氧化性與氫硫酸反應生成硫單質;與溴化亞鐵反應生成溴單質和氯化鐵;與碘化鉀反應生成單質碘;與二氧化硫反應生成硫酸和鹽酸,硫酸根與鋇離子反應生成硫酸鋇沉淀;氯氣通入紫色的石蕊試液反應生成鹽酸和次氯酸,鹽酸具有酸性,次氯酸具有漂白性;
(5)氯氣通過F裝置帶出水蒸氣,進入G中,碳、水蒸氣、氯氣發生反應生成二氧化碳和氯化氫;
解答 解:(1)二氧化錳與濃鹽酸在加熱條件下反應生成氯氣、氯化錳、水,化學方程式:MnO2+4HCl(濃)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O;
故答案為:MnO2+4HCl(濃)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O;
(2)A中濃鹽酸和二氧化錳在加熱條件下發生反應生成Cl2,Ⅰ中b瓶是用來貯存Cl2的,則應選用一種Cl2在其中溶解度非常小的液體,一般選用飽和食鹽水;
故答案為:飽和食鹽水;
(3)Ⅱ與Ⅰ原理相同,而Ⅲ中因c瓶口密封,不能氣體流通;
故答案為:Ⅱ可行,Ⅲ不行.Ⅱ與Ⅰ原理相同,而Ⅲ中因c瓶口密封,體積不能改變,增大壓強會有危險;
(4)a氯氣是黃綠色氣體,觀察當整個裝置內充滿黃綠色氣體時,說明氯氣已充滿整個裝置;
故答案為:觀察當整個裝置內充滿黃綠色氣體時,說明氯氣已充滿整個裝置;
b氯氣通過C溴化亞鐵溶液氧化亞鐵離子和溴離子為鐵離子,溶液由淺綠色變為深紅棕色;通入D碘化鉀淀粉溶液生成碘單質遇淀粉變藍;通入E混有二氧化硫的氯化鋇溶液,氧化二氧化硫為硫酸,生成白色沉淀;氯氣通入水中形成氯水,溶液呈現淺黃綠色;
故答案為:溶液由淺綠色變為深紅棕色;溶液變藍;生成白色沉淀;溶液呈現淺黃綠色;
(5)G裝置的硬質玻璃管內盛有碳粉,發生氧化還原反應,其產物為二氧化碳和氯化氫,結合原子守恒寫出化學方程式為:C+2H2O+2Cl2$\frac{\underline{\;加熱\;}}{\;}$CO2↑+4HCl↑;F為G提供水蒸氣的作用;
故答案為:C+2H2O+2Cl2$\frac{\underline{\;加熱\;}}{\;}$CO2↑+4HCl↑;向G中提供反應所需的水蒸氣;
點評 本題考查了氯氣實驗室制備、氯氣性質的驗證、反應產物的判斷,準確分析實驗過程、熟悉氯氣性質是解題關鍵,題目難度中等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:解答題
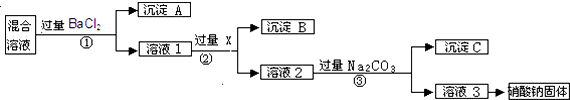
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
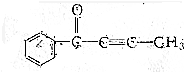 的有機化合物分子中:
的有機化合物分子中:查看答案和解析>>
科目:高中化學 來源: 題型:解答題
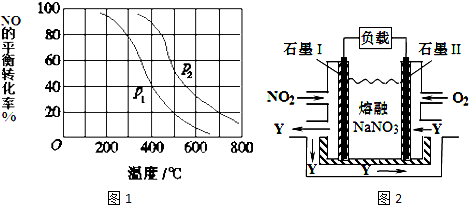
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
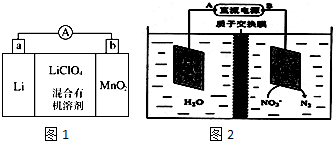
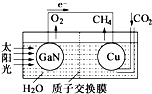 人工光合作用能夠借助太陽能,用CO2和H2O制備化學原料.科學家用氮化鎵材料與銅組裝如圖的人工光合系統,成功地實現了以CO2和H2O合成CH4,下列說法不正確的是( )
人工光合作用能夠借助太陽能,用CO2和H2O制備化學原料.科學家用氮化鎵材料與銅組裝如圖的人工光合系統,成功地實現了以CO2和H2O合成CH4,下列說法不正確的是( )| A. | 該過程是將太陽能轉化為化學能的過程 | |
| B. | GaN表面發生氧化反應,有O2產生 | |
| C. | 電解液中的H+從質子交換膜右側向左側遷移 | |
| D. | Cu表面的電極反應式 CO2+8e-+8H+═CH4+2H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 配制溶液時,如果試樣是液體,用量筒量取試樣后直接倒入容量瓶中,緩慢加入蒸餾水到接近標線1cm~2cm處,用滴管滴加蒸餾水到標線 | |
| B. | 容量瓶用蒸餾水洗凈后,再用待配溶液潤洗 | |
| C. | 配制溶液時,如果試樣是固體,把稱好的試樣用紙條小心倒入容量瓶中,緩慢加入蒸餾水到接近標線1cm~2cm處,用滴管滴加蒸餾水到標線 | |
| D. | 使用容量瓶前檢查它是否漏水 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
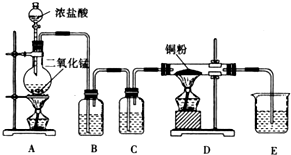 某實驗學習小組用MnO2和濃鹽酸制取純凈干燥的氯氣,并讓氯氣與銅粉反應制取純凈的無水CuCl2,裝置如圖所示.
某實驗學習小組用MnO2和濃鹽酸制取純凈干燥的氯氣,并讓氯氣與銅粉反應制取純凈的無水CuCl2,裝置如圖所示.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
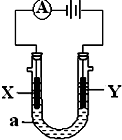 電解原理在化學工業中有廣泛應用.如圖表示一個電解池,裝有電解液a;X、Y是兩塊電極板,通過導線與直流電源相連.請回答以下問題:
電解原理在化學工業中有廣泛應用.如圖表示一個電解池,裝有電解液a;X、Y是兩塊電極板,通過導線與直流電源相連.請回答以下問題:查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com