

分析 廢舊鍍鋅鐵皮加入氫氧化鈉溶液中反應,鋅溶解生成偏鋅酸鈉和氫氣,鐵不溶解,過濾得到濾液A為Na2ZnO2,不溶物為Fe,溶液A調節pH使溶液中ZnO22-轉化為Zn(OH)2沉淀,再經過抽濾、洗滌、干燥,灼燒得到ZnO.不溶物Fe中加入硫酸,反應生成硫酸亞鐵,調節溶液PH=1~2,并加入適量過氧化氫,氧化部分亞鐵離子為鐵離子,得到含Fe2+、Fe3+的B溶液,再加入氫氧化鈉溶液,加熱分解生成四氧化三鐵膠體粒子.
(1)Zn也能和氫氧化鈉溶液反應,氫氧化鈉溶液起到溶解鍍鋅層和去除油污作用;
(2)調節溶液A的pH可產生Zn(OH)2沉淀,抽濾就可以得到氫氧化鋅沉淀,高溫灼燒氫氧化鋅分解得到ZnO;
(3)持續通入N2,防止Fe2+被氧化;
(4)根據m=cVM計算m(K2Cr2O7);
根據溶液濃度的精度,應選擇電子天平用于稱量固體質量,燒杯用于溶解固體,玻璃棒用于攪拌和引流操作,用250mL容量瓶用于配置溶液,膠頭滴管用于加水定容.
解答 解:廢舊鍍鋅鐵皮加入氫氧化鈉溶液中反應,鋅溶解生成偏鋅酸鈉和氫氣,鐵不溶解,過濾得到濾液A為Na2ZnO2,不溶物為Fe,溶液A調節pH使溶液中ZnO22-轉化為Zn(OH)2沉淀,再經過抽濾、洗滌、干燥,灼燒得到ZnO.不溶物Fe中加入硫酸,反應生成硫酸亞鐵,調節溶液PH=1~2,并加入適量過氧化氫,氧化部分亞鐵離子為鐵離子,得到含Fe2+、Fe3+的B溶液,再加入氫氧化鈉溶液,加熱分解生成四氧化三鐵膠體粒子.
(1)根據Zn及化合物的性質與Al及化合物的性質相似,Zn也能和氫氧化鈉溶液反應,氫氧化鈉溶液起到溶解鍍鋅層和去除油污作用,
故答案為:AB;
(2)調節溶液A的pH可產生Zn(OH)2沉淀,抽濾就可以得到氫氧化鋅沉淀,洗滌除去附著的離子,高溫灼燒氫氧化鋅分解得到ZnO,
故答案為:抽濾、洗滌、灼燒;
(3)持續通入N2,防止Fe2+被氧化,故答案為:在N2氣氛下,防止Fe2+被氧化;
(4)m(K2Cr2O7)=0.01000mol•L-1×0.250 L×294.0 g•mol-1=0.7350g;
根據溶液濃度的精度,應選擇電子天平用于稱量固體質量,燒杯用于溶解固體,用玻璃棒攪拌,恢復室溫,用玻璃棒引流,移入250mL容量瓶中,繼續加水至離刻度線1-2cm處,改用膠頭滴管加水定容,故用不到的儀器為量筒和移液管,
故答案為:0.7350g;③⑦.
點評 本題以“廢舊鍍鋅鐵皮可制備磁性Fe3O4膠體粒子及副產物ZnO”為載體,考查實驗基本操作和技能,涉及標準溶液的配制、對信息的利用、實驗條件的控制等,試題難度中等,是對學生綜合能力的考查,需要學生基本知識的基礎與分析問題、解決問題的能力.


 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源: 題型:解答題
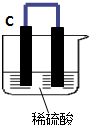 如圖所示,將鋅、銅通過導線相連置于稀硫酸中.
如圖所示,將鋅、銅通過導線相連置于稀硫酸中.查看答案和解析>>
科目:高中化學 來源: 題型:填空題
| 滴定次數 | 待測液體積(mL) | 標準鹽酸體積(mL) 滴定前讀數(mL)滴定后讀數(mL) | |
| 第一次 | 10.00 | 0.50 | 20.40 |
| 第二次 | 10.00 | 4.00 | 24.10 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:解答題

| 氫氧化物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
| 開始沉淀pH | 1.5 | 3.3 | 9.4 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
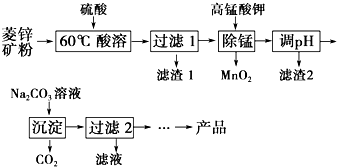 以菱鋅礦(主要成分為ZnCO3,同時含有MnO、FeO、Fe2O3、SiO2等雜質)為原料生產堿式碳酸鋅[ZnCO3•2Zn(OH)2•H2O]的工藝流程如圖.已知Fe2+、Fe3+、Zn2+生成氫氧化物沉淀的pH見表:
以菱鋅礦(主要成分為ZnCO3,同時含有MnO、FeO、Fe2O3、SiO2等雜質)為原料生產堿式碳酸鋅[ZnCO3•2Zn(OH)2•H2O]的工藝流程如圖.已知Fe2+、Fe3+、Zn2+生成氫氧化物沉淀的pH見表:| 待沉淀離子 | Fe2+ | Fe3+ | Zn2+ |
| 開始沉淀時pH | 5.8 | 1.1 | 5.9 |
| 完全沉淀時pH | 8.8 | 3.2 | 8.0 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 實驗室中有一未知濃度的稀鹽酸,某學生為測定鹽酸的濃度在實驗室中進行如下實驗:請完成下列填空:
實驗室中有一未知濃度的稀鹽酸,某學生為測定鹽酸的濃度在實驗室中進行如下實驗:請完成下列填空:| 實驗編號 | NaOH溶液的濃度 (mol/L) | 滴定完成時,NaOH溶液滴入的體積(mL) | 待測鹽酸溶液的體積 (mL) |
| 1 | 0.10 | 22.62 | 20.00 |
| 2 | 0.10 | 22.72 | 20.00 |
| 3 | 0.10 | 22.80 | 20.00 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | NaAlO2溶液中通入過量的CO2:2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32- | |
| B. | 向FeCl3溶液中滴加KSCN溶液:Fe3++3SCN-═Fe(SCN)3↓ | |
| C. | 向NaHCO3溶液中加過量Ca(OH)2溶液:Ca2++HCO3-+OH-═CaCO3↓+H2O | |
| D. | 向BaCO3固體中加入過量的稀H2SO4:BaCO3+2H+═Ba2++CO2↑+H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 乙酸乙酯(乙酸):加飽和碳酸鈉溶液,充分振蕩靜置后,分液 | |
| B. | 乙醇(水):加入新制生石灰,蒸餾 | |
| C. | 溴苯(溴):加入CCl4溶液,充分振蕩靜置后,分液 | |
| D. | 苯中混有苯酚,加入氫氧化鈉溶液,再用分液漏斗分液 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com