
| A. | △H2>△H1,△H4>△H3 | B. | △H1>△H2,△H4>△H3 | C. | △H1>△H2,△H3>△H4 | D. | △H2>△H1,△H3>△H4 |
分析 同種物質的氣態比固體能量高,同種物質的氣態比液態能量高,燃燒反應均為放熱反應,且焓變為負,以此來解答.
解答 解:由S(s)+O2(g)═SO2(g)△H1、S(g)+O2(g)═SO2(g)△H2可知,產物相同,S的狀態不同,S(g)能量高,放出熱量多,焓變小,即△H1>△H2;
由2H2(g)+O2(g)═2H2O(g)△H3、2H2(g)+O2(g)═2H2O(l)△H4可知,反應物相同,生成物的狀態不同,氣態水的能量高,則放出熱量少,焓變大,即△H3>△H4,
故選C.
點評 本題考查反應熱與焓變,為高頻考點,把握反應中能量變化、能量與物質狀態的關系為解答的關鍵,側重分析與應用能力的考查,注意燃燒反應的焓變為負,題目難度不大.


科目:高中化學 來源: 題型:解答題
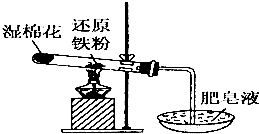 常溫下沒有氧氣存在時,鐵與水幾乎不反應,但高溫下,鐵與水蒸氣能反應.小明設計如下實驗探究鐵粉與水蒸氣反應后的氣體產物.
常溫下沒有氧氣存在時,鐵與水幾乎不反應,但高溫下,鐵與水蒸氣能反應.小明設計如下實驗探究鐵粉與水蒸氣反應后的氣體產物.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
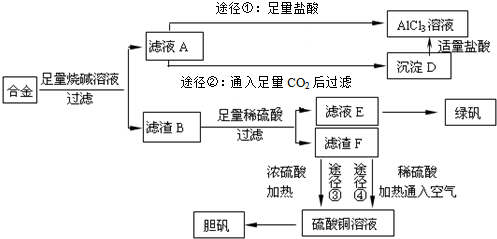
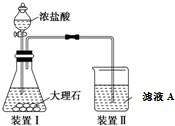
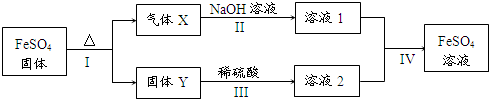
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 因為焓變和熵變都與反應的自發性有關,因此焓變或熵變均可以單獨作為反應自發性的判據 | |
| B. | 對于能夠自發進行的吸熱反應,其原因是體系有自發地向混亂度增加的方向轉變的傾向 | |
| C. | △H<0、△S>0的反應在溫度低時不能自發進行 | |
| D. | 在其他外界條件不變的情況下,使用催化劑,可以改變化學反應進行的方向 |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
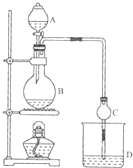 某課外小組設計的實驗室制取乙酸乙酯的裝置如圖所示,A中放有濃硫酸,B中放有乙醇、無水醋酸鈉,D中放有飽和碳酸鈉溶液. 已知
某課外小組設計的實驗室制取乙酸乙酯的裝置如圖所示,A中放有濃硫酸,B中放有乙醇、無水醋酸鈉,D中放有飽和碳酸鈉溶液. 已知| 試劑 | 乙醚 | 乙醇 | 乙酸 | 乙酸乙酯 |
| 沸點/℃ | 34.7 | 78.5 | 118 | 77.1 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
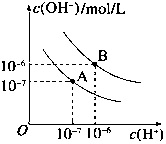 已知水在25℃和95℃時,其電離平衡曲線如圖所示:
已知水在25℃和95℃時,其電離平衡曲線如圖所示:查看答案和解析>>
科目:高中化學 來源: 題型:實驗題

查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com