

分析 (1)①根據燃燒熱的概念以及蓋斯定律來計算化學反應的焓變;
②依據原料的利用率和對環境的影響分析判斷;
(2)①化學反應達到平衡的標志是正逆反應速率相同,個組分含量保持不變,及其衍生出的各種物理量不變分析判斷;
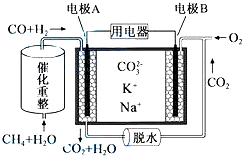
②甲烷和水經催化重整生成CO和H2,反應中C元素化合價有-4價升高到+2價,H元素化合價由+1價降低到0價,原電池工作時,CO和H2為負極反應,被氧化生成二氧化碳和水,正極為氧氣得電子生成CO32-,以此解答該題;
(3)根據關系式2Na2S2O3~I2,計算硫代硫酸鈉溶液吸收所產生的碘后剩余的Na2S2O3物質的量,進而計算CO還原出的I2消耗Na2S2O3的物質的量,再根據關系式:2Na2S2O3~I2~5CO,計算CO的物質的量,據此計算CO的濃度.
解答 解:(1)①由H2(g)的燃燒熱△H為-285.8kJ•mol-1知,1molH2(g)完全燃燒生成1molH2O(l)放出熱量285.8kJ,
即a、H2(g)+$\frac{1}{2}$O2(g)=H2O(l)△H=-285.8kJ•mol-1;
b、CO(g)+$\frac{1}{2}$O2(g)=CO2(g)△H=-283.0kJ•mol-1
c、CH3OH(l)+$\frac{1}{2}$O2(g)=CO2(g)+2 H2O(l)△H=-726.5kJ•mol-1,
由蓋斯定律可知,a×2+b-c得:CO (g)+2H2(g)═CH3OH (l)△H=-128.1kJ/mol,
故答案為:CO (g)+2H2(g)═CH3OH (l)△H=-128.1kJ/mol;
②煤進行氣化和液化的優點是原料全部被產品消納(或原料全部轉化為產品,或原子利用率100%等),實現“零排放”或不對環境造成污染等,
故答案為:利用率高,污染小;
(2)①天然氣催化重整也可生成CO和H2,500℃,向一體積可變的密閉容器中充入一定量CH4和水蒸氣進行催化重整,反應的化學方程式為CH4+H2O=CO+3H2,是氣體體積增大的反應,
A.體積可變的密閉容器,氣體質量不變,體積若不變化,則混合氣體的密度不隨時間變化 說明反應達到平衡狀態,故A正確;
B.CO和H2的體積分數之比不隨時間變化一氧化碳和氫氣生成物質的量之比始終相同,不能說明反應達到平衡狀態,故B錯誤;
C.反應速率之比等于化學方程式計量數之比,為正反應速率之比,當3V正(CH4)=v逆(H2)時反應達到平衡狀態,所以V正(CH4)=3v逆(H2)不能說明反應達到平衡狀態,故C錯誤;
D.反應前后氣體質量不變,氣體物質的量變化,若混合氣體的平均相對分子質量不隨時間變化,說明反應達到平衡狀態,故D正確;
故答案為:AD;
②電解質沒有OH-,負極反應為:H2+CO32--2e-=H2O+CO2 ,CO-2e-+CO32-=2CO2,或H2+2CO+CO32--2e-=H2O+2CO2,
故答案為:H2+CO32--2e-=H2O+CO2,CO-2e-+CO32-=2CO2,或H2+2CO+CO32--2e-=H2O+2CO2;
(3)CO與I2O5反應生成CO2和I2,碳元素化合價由+2價升高為+4價,共升高2價,碘元素化合價由+5價降低為0價,共降低10價,化合價升降最小公倍數為10,故CO系數為5,I2O5系數為1.由原子守恒可知CO2系數為5,I2系數為1,反應方程式為5CO+I2O5=5CO2+I2.
關系式:2Na2S2O3~I2~5CO
2mol 5mol
0.030.0L×5.00×10-3mol/L y
解得:y=3.75×10-4mol
CO的濃度為$\frac{3.75×1{0}^{-4}mol×28g/mol}{2L}$=5.25×10-3g/L=5.25mg/L.
故答案為:5.25 mg/L;
點評 本題考查熱化學方程式書寫,化學平衡狀態分析判斷方法,原電池原理的理解應用,氧化還原反應的滴定計算等,難度中等,對于多步反應計算通常利用關系式解答,理解關系式并熟練運用.


科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | CH3CH(NO2)COOH分子中含有“手性碳原子” | |
| B. | HS-和HC1均是含一個極性鍵的18電子粒子 | |
| C. | 當用帶有靜電的玻璃棒接近CH2Cl2和CC14液體細流時,細流都不發生偏轉 | |
| D. | 1mol己烷含有的共價鍵數目為19NA(NA代表阿伏加德羅常數) |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
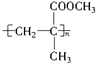 關于它的敘述不正確的是( )
關于它的敘述不正確的是( )| A. | 該有機玻璃的化學名稱為聚甲基丙烯酸甲酯 | |
| B. | 該有機玻璃可用2-甲基丙烯酸和甲醇為原料,通過酯化反應、加聚反應制得 | |
| C. | 它在一定條件下發生水解反應時,可得到另外一種高分子化合物 | |
| D. | 等物質的量的有機玻璃和2-甲基丙烯酸甲酯耗氧量相同 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 實驗事實 | 結論 | |
| A | 鐵與硫單質生成FeS,與Cl2生成FeCl3 | 氧化性:Cl2>S |
| B | 將CO2通入到Na2SiO3溶液中產生白色渾濁(H2SiO3) | 酸性:H2CO3>H2SiO3 |
| C | 將燃燒的鎂條放入CO2中能繼續燃燒 | 還原性:Mg>C |
| D | 某無色溶液加入鹽酸酸化的氯化鋇溶液產生白色沉淀 | 原溶液一定有SO${\;}_{4}^{2-}$ |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | As2O3中As元素為+3價 | B. | 維生素C能將+5價砷還原成As2O3 | ||
| C. | 致人中毒過程中砷發生氧化反應 | D. | 維生素C具有氧化性 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 金屬性:Na>Mg>Al | B. | 原子半徑:Cl>Si>O | ||
| C. | 熔點:SiO2>NaCl>SO2 | D. | 酸性:HClO4>H2SO4>H2CO3 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ⅤB族 | B. | ⅢB族 | C. | Ⅷ族 | D. | ⅤA族 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com