
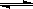 2SO3(g)
2SO3(g) 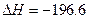 kJ·mol
kJ·mol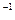 )
)| 容器 | 甲 | 乙 | 丙 |
| 反應物投入量 | 2mol SO2、1mol O2 | 2mol SO3 | 4mol SO3 |
SO3的濃度(mol· L L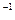 ) ) | c1 | c2 | c3 |
| 反應的能量變化 | 放出akJ | 吸收bkJ | 吸收ckJ |
| 體系壓強(Pa) | p1 | p2 | p3 |
| 反應物轉化率 |  | 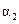 | 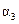 |
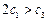 B.
B.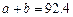 C.
C.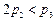 D.
D.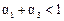
 2SO3(g)下列說法正確的是
2SO3(g)下列說法正確的是 SO2的轉化率為12. 5%,O2的轉化率為25%, 開始充入容器中的SO2、O2物質的量之比為4∶1
SO2的轉化率為12. 5%,O2的轉化率為25%, 開始充入容器中的SO2、O2物質的量之比為4∶1 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源:不詳 題型:填空題
 2NO2 (g) △H> 0,反應過程中各物質的物質的量濃度(c)隨時間(t)的變化關系如下圖所示。
2NO2 (g) △H> 0,反應過程中各物質的物質的量濃度(c)隨時間(t)的變化關系如下圖所示。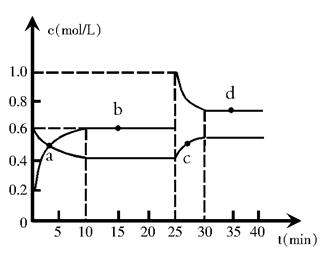
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
 2M(g)+N(g) △H>0,平衡狀態時(P1>P2)圖中y軸是指
2M(g)+N(g) △H>0,平衡狀態時(P1>P2)圖中y軸是指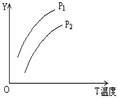
| A.L的體積分數 |
| B.混合氣體的總物質的量 |
| C.混合氣體的平均分子量 |
| D.氣體混合物的密度 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
 2SO3(g)+Q,下列敘述中,不正確的是:
2SO3(g)+Q,下列敘述中,不正確的是:| A.礦石粉碎的目的是使原料充分利用,并增大接觸面使反應速率加快 |
| B.接觸室中采用常壓的主要原因是常壓下SO2的轉化率已經很高 |
| C.沸騰爐中出來的混合氣需要洗滌,目的是防止催化劑中毒 |
| D.接觸室采用450℃的溫度是使催化劑活性最佳,提高平衡混和氣中SO3的含量 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
 2SO3(g);△H= -197.74 kJ·mol-1,4min后達到平衡,這時c(SO2)="0.2mol" L-1,且SO2和O2的轉化率相等。下列說法中,不正確的是( )
2SO3(g);△H= -197.74 kJ·mol-1,4min后達到平衡,這時c(SO2)="0.2mol" L-1,且SO2和O2的轉化率相等。下列說法中,不正確的是( )| A.2min時,c(SO2)="0.6mol" L-1 |
| B.用O2表示4min內的反應速率為0.1mol·(L·min)-1 |
| C.再向容器中充入1mol SO3,達到新平衡,n(SO2):n(SO3)=2:1 |
| D.4min后,若升高溫度,平衡向逆方向移動,平衡常數K增大 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
 cC(g)+dD(g),反應達到平衡后,將氣體體積壓縮到原來的一半,當再次達到平衡時,D的濃度為原平衡的1.8倍,下列敘述正確的是
cC(g)+dD(g),反應達到平衡后,將氣體體積壓縮到原來的一半,當再次達到平衡時,D的濃度為原平衡的1.8倍,下列敘述正確的是| A.A的轉化率變小 | B.平衡向正反應方向移動 |
| C.D的體積分數變大 | D.a < c+d |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:計算題
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題

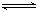 4NO(g)+6H2O(g);⊿H= -808.7KJ/mol
4NO(g)+6H2O(g);⊿H= -808.7KJ/mol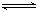 NO2(g)+NO(g);⊿H= +41.8kJ/mol
NO2(g)+NO(g);⊿H= +41.8kJ/mol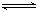 2HNO3(l)+NO(g);⊿H= -261.3kJ/mol
2HNO3(l)+NO(g);⊿H= -261.3kJ/mol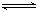 2CO(g);⊿H= +171.4kJ/mol
2CO(g);⊿H= +171.4kJ/mol查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題
 CH3OH(g)
CH3OH(g)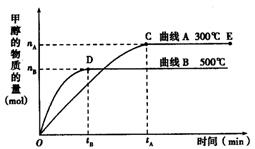
| A.H2的轉化率一定增大 | B.v正一定增大,v逆一定減小 |
| C.CH3OH的質量分數一定增加 | D.v逆一定小于v正 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com