
已知甘油(C3H8O3)通常是無色液體,易溶于水,密度比水大,沸點約為290.9℃。要從甘油、水的混合物中分別得到甘油與水,最佳方法是
A.分液 B.過濾 C.蒸發 D.蒸餾
科目:高中化學 來源:2015-2016學年江蘇省高一上第二次月考化學試卷(解析版) 題型:填空題
下圖所示為含Cr化合物在一定條件下的轉化:
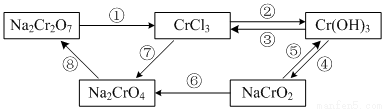
(1)①~⑧所示轉化中,需要加入氧化劑才能實現的是_______(填寫序號)。
(2)在上述轉化中,既能與強酸反應又能與強堿反應的兩性物質是______(填化學式)。
(3)轉化①可通過下列反應實現:
①完成并配平的化學方程式:
__Na2Cr2O7+__KI+__H2SO4——__Cr2(SO4)3+__Na2SO4+__K2SO4+__I2+__H2O
②用單線橋表示電子轉移的方向和數目
③反應中每轉移0.4mol電子,生成I2的物質的量為______mol。
查看答案和解析>>
科目:高中化學 來源:2016屆黑龍江省高三上期末理綜化學試卷(解析版) 題型:實驗題
某研究小組利用下圖裝置探究溫度對CO還原Fe2O3的影響(固定裝置略)

(1)MgCO3的分解產物為 。
(2)裝置C的作用是 ,處理尾氣的方法為 。
(3)將研究小組分為兩組,按圖裝置進行對比實驗,甲組用酒精燈、乙組用酒精噴燈對裝置D加熱,反應產物均為黑色粉末(純凈物),兩組分別用產物進行以下實驗。(Fe2+ 遇K3[Fe(CN)6]溶液會生成藍色沉淀)
步驟 | 操作 | 甲組現象 | 乙組現象 |
1 | 取黑色粉末加入稀鹽酸 | 溶解,無氣泡 | 溶解,有氣泡 |
2 | 取步驟1中溶液,滴加K3[Fe(CN)6]溶液 | 藍色沉淀 | 藍色沉淀 |
3 | 取步驟1中溶液,滴加KSCN溶液 | 變紅 | 無現象 |
4 | 向步驟3溶液中滴加新制氯水 | 紅色褪去 | 先變紅,后褪色 |
①乙組得到的黑色粉末是 。
②甲組步驟1中反應的離子方程式為 。
③乙組步驟4中,溶液變紅的原因為 ;溶液褪色可能的原因為 。
④從實驗安全考慮,題圖裝置還可采取的改進措施是 。
查看答案和解析>>
科目:高中化學 來源:2016屆陜西省高三上12月模擬化學試卷(解析版) 題型:填空題
一氧化碳是一種用途廣泛的化工基礎原料。
(l)在高溫下CO可將SO2還原為單質硫。已知:2CO(g)+O2(g) 2CO2(g) △H1=-566.0kJ·mol-1;S(s)+O2(g)
2CO2(g) △H1=-566.0kJ·mol-1;S(s)+O2(g) SO2(g) △H2=-296.0kJ·mol-1;
SO2(g) △H2=-296.0kJ·mol-1;
請寫出CO還原SO2的熱化學方程式______________________。
(2)工業上用一氧化碳制取氫氣的反應為:CO(g)+H2O(g) CO2(g)+H2(g),已知420℃時,該反應的化學平衡常數K=9。如果反應開始時,在2L的密閉容器中充入CO和H2O的物質的量都是0.60mol,5min末達到平衡,則此時CO的轉化率為 ,H2的平均生成速率為 mol·L-1·min-1。
CO2(g)+H2(g),已知420℃時,該反應的化學平衡常數K=9。如果反應開始時,在2L的密閉容器中充入CO和H2O的物質的量都是0.60mol,5min末達到平衡,則此時CO的轉化率為 ,H2的平均生成速率為 mol·L-1·min-1。
(3)CO與H2反應還可制備CH3OH,CH3OH可作為燃料使用,用CH3OH和O2組合形成的質子交換膜燃料電池的結構示意圖:
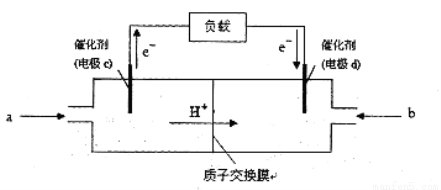
電池總反應為:2CH3OH+3O2=2CO2+4H2O,則c電極是 (填“正極”或“負極”),c電極的反應方程式為 。若用該電池電解精煉銅(雜質含有Ag和Fe),粗銅應該接此電源的________極(填“c”或“d”),反應過程中析出精銅64g,則上述CH3OH燃料電池,消耗的O2在標況下的體積為 L。
查看答案和解析>>
科目:高中化學 來源:2015-2016學年江蘇省高一上學期期中考試化學試卷(解析版) 題型:選擇題
下列實驗裝置或操作正確的是

A.轉移溶液 B.除去氯氣中氯化氫 C.點燃 D.稱量NaOH固體
查看答案和解析>>
科目:高中化學 來源:2015-2016學年四川省高一上學期12月月考化學試卷(解析版) 題型:選擇題
若NA代表阿伏伽德羅常數,則下列有關阿伏伽德羅常數的說法正確的是
A、1molNa與足量氧氣充分反應轉移電子數目為NA
B、1L0.1mol/LHCl溶液中含0.1NAHCl分子
C、100ml 1mol/L鹽酸與0.1molNa2CO3無論如何滴加都產生0.05 NA 的CO2分子
D、0.1mol/L的AlCl3中Cl-的物質的量為0.3NA
查看答案和解析>>
科目:高中化學 來源:2015-2016學年浙江省高二上學期第一次質檢化學試卷(解析版) 題型:實驗題
I、某學生實驗小組用50mL0.50mol•L—1的鹽酸與50mL0.50mol•L—1的NaOH溶液在右圖所示的裝置中進行中和反應反應熱的測定
(1)圖中裝置缺少的一種儀器,該儀器名稱為 。

(2)將反應混合液的 溫度記為反應的終止溫度。
(3)下列說法正確的是
A.小燒杯內殘留有水,會使測得的反應熱數值偏小
B.可用相同濃度和體積的醋酸代替稀鹽酸溶液進行實驗
C.燒杯間填滿碎紙條的作用是固定小燒杯
D.酸、堿混合時,應把量筒中的溶液緩緩倒入燒杯的溶液中,以防液體外濺
II、某實驗小組以H2O2分解為例,研究濃度、催化劑、溶液酸堿性對反應速率的影響。在常溫下按照如下方案完成實驗。
實驗編號 | 反應物 | 催化劑 |
① | 10mL2% H2O2溶液 | 無 |
② | 10mL5% H2O2溶液 | 無 |
③ | 10mL5% H2O2溶液 | 1mL0.1mol·L-1FeCl3溶液 |
④ | 10mL5% H2O2溶液+少量HCl溶液 | 1mL0.1mol·L-1FeCl3溶液 |
⑤ | 10mL5% H2O2溶液+少量NaOH溶液 | 1mL0.1mol·L-1FeCl3溶液 |
(1)催化劑能加快化學反應速率的原因是__________________。
(2)實驗①和②的目的是____________________________。實驗時由于較長時間沒有觀察到明顯現象而無法得出結論。資料顯示,通常條件下H2O2穩定,不易分解。為了達到實驗目的,你對原實驗方案的改進是____________________。
(3)寫出實驗③的化學反應方程式 。
(4)實驗③、④、⑤中,測得生成氧氣的體積隨時間變化的關系如下圖。

分析上圖能夠得出的實驗結論是_______________________。
查看答案和解析>>
科目:高中化學 來源:2015-2016學年浙江省桐鄉市高二上期中(實驗班)化學試卷(解析版) 題型:選擇題
下列說法正確的是
A.增大反應物濃度可以增大活化分子百分數,從而使反應速率增大
B.汽車尾氣的催化轉化裝置可將尾氣中的NO和CO等有害氣體快速地轉化為N2和CO2,其原因是催化劑可增大NO和CO反應的活化能
C.在“反應熱的測量實驗”中測定反應后溫度的操作方法:將量筒中的NaOH溶液經玻璃棒引流緩緩倒入盛有鹽酸的簡易量熱計中,立即蓋上蓋板,并用環形玻璃攪拌棒不斷攪拌,準確讀出并記錄反應體系的最高溫度
D.研制性能優良的催化劑既可以提高化學反應速率,又能起到很好的節能效果
查看答案和解析>>
科目:高中化學 來源:2015-2016學年甘肅省高二上期末考試化學試卷(解析版) 題型:填空題
下面幾組物質,請將合適組號填寫在下表中。
①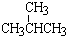 和
和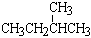 ;②
;②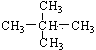 和
和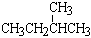 ;③CH4和CH3CH2CH3;④金剛石與石墨;⑤氕、氘與氚;⑥16O、17O和18O;⑦乙醇(CH3CH2OH)和二甲醚(CH3OCH3);⑧氧氣(O2)與臭氧(O3)。
;③CH4和CH3CH2CH3;④金剛石與石墨;⑤氕、氘與氚;⑥16O、17O和18O;⑦乙醇(CH3CH2OH)和二甲醚(CH3OCH3);⑧氧氣(O2)與臭氧(O3)。
類別 | 同位素 | 同系物 | 同素異形體 | 同分異構體 |
組號 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com