
【題目】氧化鐵是一種重要的無機材料,化學性質穩(wěn)定,催化活性高,具有良好的耐光性、耐熱性和對紫外線的屏蔽性,從某種工業(yè)酸性廢液(主要含Na+、Fe2+、Fe3+、Mg2+、Al3+、Cl-、SO42-)中回收氧化鐵流程如下:

已知:常溫下Ksp[Mg(OH)2]=1.2×10-11;Ksp[Fe(OH)2]=2.2×10-16;Ksp[Fe(OH)3]=3.5×10-38;Ksp[Al(OH)3]=1.0×10-33
(1)寫出在該酸性廢液中通入空氣時發(fā)生的離子反應方程式:___________,指出使用空氣的優(yōu)點是:_________。
(2)已知Fe3+(aq)+3OH-(aq)===Fe(OH)3(s)ΔH=-Q1kJ·mol-1,題(1)中每生成1 mol含鐵微粒時,放熱Q2,請你計算1 mol Fe2+全部轉化為Fe(OH)3(s)的熱效應ΔH=_________。
(3)常溫下,根據(jù)已知條件計算在pH=5的溶液中,理論上下列微粒在該溶液中可存在的最大濃度c(Fe3+)=___________,c(Mg2+)=___________。
(4)有人用氨水調節(jié)溶液pH,在pH=5時將Fe(OH)3沉淀出來,此時Fe(OH)3沉淀中可能混有的雜質是______ (填化學式,下同),用_______試劑可將其除去。
【答案】4Fe2++O2+4H+=4Fe3++2H2O 耗費少且無污染 -(Q2+Q1) kJ·mol-1 3.5×10-11mol·L-1 1.2×107mol·L-1 Al(OH)3 NaOH
【解析】
(1)酸性廢液中通入空氣時,Fe2+被空氣中的氧氣所氧化,離子方程式為4Fe2++O2+4H+=4Fe3++2H2O,該方法的優(yōu)點是耗費少且無污染;
(2)根據(jù)蓋斯定律計算;
(3)溶液pH=5,則c(OH-)=10-9mol/L,根據(jù)Ksp[Fe(OH)3]=3.5×10-38,Ksp[Mg(OH)2]=1.2×10-11,可計算;
(4)根據(jù)Ksp[Al(OH)3]=1.0×10-33,可計算出溶液pH=5時,c(Al3+)<1.0×10-5,Al3+也幾乎完全沉淀,故可能混有的雜質是Al(OH)3,Al(OH)3溶于強堿,而Fe(OH)3不溶,故可用NaOH溶液除去。
(1)酸性廢液中通入空氣時,Fe2+被空氣中的氧氣所氧化,離子方程式為4Fe2++O2+4H+=4Fe3++2H2O,該方法的優(yōu)點是耗費少且無污染;
(2)根據(jù)蓋斯定律由Fe3+(aq)+3OH-(aq)=Fe(OH)3(s);△H=-Q1 kJ/mol,題(1)中每生成1mol含鐵微粒時,放熱Q2,則1 mol Fe2+全部Fe3+放熱為Q2,Fe3+轉化為Fe(OH)3(s)的放熱為Q1,所以1 mol Fe2+全部轉化為Fe(OH)3(s)的熱效應△H=-(Q2+Q1)kJ/mol;
(3)溶液pH=5,則c(OH-)=10-9mol/L,根據(jù)Ksp[Fe(OH)3]=3.5×10-38,Ksp[Mg(OH)2]=1.2×10-11,
則c(Fe3+)=![]() =3.5×10-11mol/L、c(Mg2+)=
=3.5×10-11mol/L、c(Mg2+)=![]() =1.2×107mol/L;
=1.2×107mol/L;
(4)根據(jù)Ksp[Al(OH)3]=1.0×10-33,可計算出溶液pH=5時,c(Al3+)<1.0×10-5,Al3+也幾乎完全沉淀,故可能混有的雜質是Al(OH)3,Al(OH)3溶于強堿,而Fe(OH)3不溶,故可用NaOH溶液除去。故答案為:Al(OH)3,NaOH溶液。


科目:高中化學 來源: 題型:
【題目】將CO2氣體緩緩地通入到含KOH、Ba(OH)2和K[Al(OH)4]的混合溶液中直至過量,生成沉淀的物質的量與所通CO2的體積關系如圖所示。下列關于整個反應進程中的各種描述不正確的是
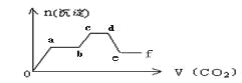
A. o—a段反應的化學方程式是:Ba(OH)2 + CO2 = BaCO3↓+ H2O
B. b—c段反應的離子方程式是:2[Al(OH)4]-+ CO2 = 2Al(OH)3↓ +CO32-+ H2O
C. a—b段與c—d段所發(fā)生的反應相同
D. d—e段沉淀的減少是由于碳酸鋇固體的消失所致
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】 (1)一塊表面已被氧化為Na2O的鈉塊10.8 g,將其投入100 mL水中,產生標準狀況下2.24 L氣體(假設溶液體積變化可忽略)。則這塊鈉塊中所含單質鈉的質量分數(shù)是_________(保留小數(shù)點后一位)。所得溶液中溶質的物質的量濃度為_________。
(2)已知實驗室也可用KMnO4和濃鹽酸反應制備氯氣,化學方程式為2KMnO4+16HCl=2KCl+5Cl2↑+2MnCl2+8H2O,請用雙線橋法表示出電子轉移的方向和數(shù)目______________。該反應中還原產物為______________。
(3)碳酸氫鈉俗稱小蘇打,請寫出碳酸氫鈉的電離方程式_______________________。碳酸氫鈉既能與酸反應又能與堿反應,請寫出碳酸氫鈉溶液與NaOH溶液反應的離子方程式
_______________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖為實驗室蒸餾自來水得到少量蒸餾水的裝置示意圖,請根據(jù)圖示回答下列問題:
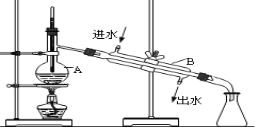
(1)裝置中儀器A、B的名稱是_____________________ 、 ______________________。
(2)請指出上圖中的兩處明顯錯誤:____________________、_____________________。
(3)實驗時A中除加入少量自來水外,還需加入少量的沸石,其作用是_____________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知下列反應的熱化學方程式為
①CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l) ΔH1=-870.3 kJ·mol-1
②C(s)+O2(g)=CO2(g) ΔH2=-393.5 kJ·mol-1
③H2(g)+![]() O2(g)=H2O(l) ΔH3=-285.8 kJ·mol-1
O2(g)=H2O(l) ΔH3=-285.8 kJ·mol-1
則反應2C(s)+2H2(g)+O2(g)=CH3COOH(l)的ΔH為( )
A. -488.3 kJ·mol-1 B. -191 kJ·mol-1
C. -476.8 kJ·mol-1 D. -1 549.6 kJ·mol-1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氨氣(NH3)是一種重要的化工原料,廣泛應用于制氮肥、制藥、合成纖維等。請回答下列問題:
(1)2molNH3在標準狀況下的體積是___。
(2)2molNH3的質量是___,其中所含氫元素的質量是___。
(3)2molNH3所含的氨分子數(shù)為___,電子數(shù)為___。
(4)工業(yè)上用反應N2+3H2 ![]() 2NH3來合成氨氣,則若制得2molNH3,標準狀況下參與反應的H2的體積為___;14克N2參與反應可得NH3物質的量為___。
2NH3來合成氨氣,則若制得2molNH3,標準狀況下參與反應的H2的體積為___;14克N2參與反應可得NH3物質的量為___。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】工業(yè)生產純堿的工藝流程示意圖如下:

完成下列填空:
(1)粗鹽水加入沉淀劑A、B除雜質(沉淀劑A來源于石灰窯廠),寫出A、B的化學式。
A__________________________________B__________________________________
(2)實驗室提純粗鹽的實驗操作依次為:
取樣、______、沉淀、______、______、冷卻結晶、______、烘干。
(3)工業(yè)生產純堿工藝流程中,碳酸化時產生的現(xiàn)象是____________________________。
碳酸化時沒有析出碳酸鈉晶體,其原因是_______________________________________。
(4)碳酸化后過濾,濾液D最主要的成分是_____________________________(填寫化學式),檢驗這一成分的陰離子的具體方法是:________________________________________。
(5)氨堿法流程中氨是循環(huán)使用的,為此,濾液D加入石灰水產生氨。加石灰水后所發(fā)生的反應的離子方程式為:_________________________________________________________
濾液D加石灰水前先要加熱,原因是_____________________________________________。
(6)產品純堿中含有碳酸氫鈉。如果用加熱分解的方法測定純堿中碳酸氫鈉的質量分數(shù),純堿中碳酸氫鈉的質量分數(shù)可表示為:
_____________________________________________________________________________
(注明你的表達式中所用的有關符號的含義)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】用下列實驗裝置進行相應實驗,能達到實驗目的且操作正確的是( )
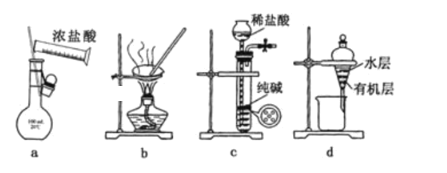
A.用圖a所示裝置配制l00mL0.100mo1L-1稀鹽酸
B.用圖b所示裝置蒸發(fā)NaCl溶液制備NaCl固體
C.用圖c所示裝置制取少量CO2氣體
D.用圖d所示裝置分離用苯萃取碘水后已分層的有機層和水層
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】向 0.1mo1·L-1 的 H2SO4 溶液中滴入 0.1mo1·L-1 過量的 Ba(OH)2 溶液,溶液的導電能力發(fā)生變化,其電流強度 (I) 隨加入 Ba(OH)2 溶液的體積 (V) 的變化曲線正確的是
A.  B.
B. 
C.  D.
D. 
查看答案和解析>>
湖北省互聯(lián)網違法和不良信息舉報平臺 | 網上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com