
| A. | 常溫下,pH=5的NaHC2O4溶液中:c(C2O42-)>c(H2C2O4) | |
| B. | 在0.1mol•L-1 CH3COONa溶液中:n(OH-)+0.1mol>n(CH3COOH)+n(H+)+n(Na+) | |
| C. | 向AgBr的飽和溶液中加入NaCl固體,有白色固體析出,說明AgCl比AgBr更難溶 | |
| D. | 10mL 0.01mol•L-1 H2SO4溶液與10mL 0.01mol•L-1 NaOH溶液充分混合,若混合后溶液的體積為20mL,則溶液的pH=7 |
分析 A.常溫下,NaHC2O4溶液的pH=5,說明草酸氫根離子電離程度大于水解程度;
B.任何電解質溶液中都存在電荷守恒和物料守恒,根據電荷守恒和物料守恒判斷;
C.濃度積大于溶度積常數時,該物質能產生沉淀;
D.等濃度等體積的硫酸和NaOH混合,二者反應生成硫酸鈉和水,但只有一半的硫酸參加反應,一半的硫酸剩余,溶液中溶質為等物質的量濃度的硫酸和硫酸鈉.
解答 解:A.常溫下,NaHC2O4溶液的pH=5,說明草酸氫根離子電離程度大于水解程度,所以c(C2O42-)>c(H2C2O4),故A正確;
B.任何電解質溶液中都存在電荷守恒和物料守恒,根據電荷守恒n(OH-)+n(CH3COO-)=n(H+)+n(Na+),根據物料守恒得n(Na+)=n(CH3COO-)+n(CH3COOH),
則存在n(OH-)=n(CH3COOH)+n(H+),因為溶液體積未知,無法計算鈉離子物質的量,故B錯誤;
C.濃度積大于溶度積常數時,該物質能產生沉淀,向AgBr的飽和溶液中加入NaCl固體,AlCl的濃度商大于其溶度積常數,所以有白色固體析出,但不能說明AgCl比AgBr更難溶,故C錯誤;
D.等濃度等體積的硫酸和NaOH混合,二者反應生成硫酸鈉和水,但只有一半的硫酸參加反應,一半的硫酸剩余,溶液中溶質為等物質的量濃度的硫酸和硫酸鈉,溶液呈酸性,pH<7,故D錯誤;
故選A.
點評 本題考查離子濃度大小比較、難溶物的溶解平衡等知識點,為高頻考點,明確溶液中溶質及其性質是解本題關鍵,注意B中不能計算出具體物質的量,但該溶液中存在c(OH-)+0.1mol/L=c(CH3COOH)+c(H+)+c(Na+),易錯選項是BC.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:解答題
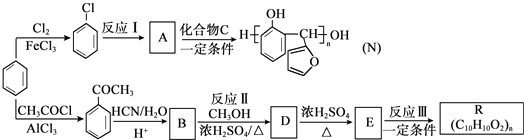

 .
. 生成
生成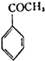 的反應類型是取代反應,D生成E的過程中,濃硫酸的作用催化劑和吸水劑.
的反應類型是取代反應,D生成E的過程中,濃硫酸的作用催化劑和吸水劑. .
.查看答案和解析>>
科目:高中化學 來源: 題型:填空題
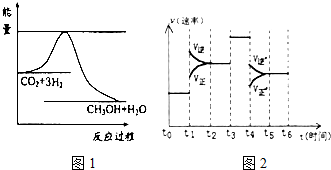 煤化工是以煤為原料,經過化學加工使煤轉化為氣體、液體、固體燃料以及各種化工產品的工業過程.
煤化工是以煤為原料,經過化學加工使煤轉化為氣體、液體、固體燃料以及各種化工產品的工業過程.| 實驗組 | 溫度/℃ | 起始量/mol | 平衡量/mol | 達到平衡所需時間/min | ||
| CO | H2O | H2 | CO2 | |||
| 1 | 650 | 2 | 4 | 1.6 | 1.6 | 5 |
| 2 | 900 | 1 | 2 | 0.4 | 0.4 | 3 |
| 3 | 900 | a | b | c | d | t |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
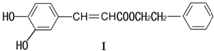
| A. | 遇FeCl3溶液可能顯紫色 | |
| B. | 可發生酯化反應和銀鏡反應 | |
| C. | 能與溴發生取代和加成反應 | |
| D. | 1mol化合物I最多能與2molNaOH反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
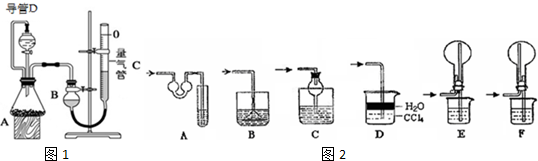
| 實驗 | 藥品 | 制取氣體 | 量氣管中的液體 |
| Ⅰ | Cu、稀HNO3 | H2O | |
| Ⅱ | NaOH固體、濃氨水 | NH3 | |
| Ⅲ | 鎂鋁合金、足量NaOH溶液 | H2 | H2O |
| 編號 | 鎂鋁合金質量 | 量氣管第一次讀數 | 量氣管第二次讀數 |
| ① | 1.0g | 10.0mL | 376.6mL |
| ② | 1.0g | 10.0mL | 364.7mL |
| ③ | 1.0g | 10.0mL | 377.0mL |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 高溫下,16.8g Fe與足量水蒸氣完全反應失去電子數為0.8NA | |
| B. | 一定條件下Fe粉與足量的濃硫酸反應,轉移電子數為3NA | |
| C. | 在1L的碳酸鈉溶液中,若c(CO32- )=1mol•L-1,則溶液中Na+的個數為2NA | |
| D. | 含4NA個離子的固體Na2O2溶于水配成1L溶液,所得溶液中c(Na+)=2mol•L-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 赤鐵礦:Fe3O4 | B. | 銅綠:Cu2(OH)2CO3 | C. | 磁鐵礦:Fe2O3 | D. | 明礬:2KAl(SO4)2 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com