
| A. | ①③⑤ | B. | ②⑥ | C. | ④⑤ | D. | ④⑥⑦ |
分析 根據化學平衡狀態的特征解答,當反應達到平衡狀態時,正逆反應速率相等,各物質的濃度、百分含量不變,以及由此衍生的一些量也不發生變化,解題時要注意,選擇判斷的物理量,隨著反應的進行發生變化,當該物理量由變化到定值時,說明可逆反應到達平衡狀態.
解答 解:①單位時間內生成n mol H2的同時生成2n mol HI時,反應達到平衡狀態,故錯誤;
②反應過程中有一個H-H鍵斷裂的同時有兩個H-I鍵斷裂,說明正逆反應速率相等,證明反應達到平衡狀態,故正確;
③各組分多少,與開始加入的物質的量多少有關,與平衡無關,故錯誤;
④無論反應是否達到平衡狀態,反應速率之比都等于其化學計量數之比,所以v(H2)=V(I2)=$\frac{1}{2}$v(HI)不能說明反應達到平衡狀態,故錯誤;
⑤當體系達平衡狀態時,[HI]:[H2]:[I2]可能等于2:1:1,也可能不等,與各物質的初始濃度及轉化率有關,故錯誤;
⑥v(HI)分解=v(HI)生成,正逆反應速率相等,故正確;
⑦兩邊計量數相等,所以壓強始終不變,故錯誤;所以②⑥正確;
故選B.
點評 本題考查了化學平衡狀態的判斷,難度不大,注意平衡是各組分濃度不變,正逆反應速率相等是平衡的關鍵.


 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源: 題型:選擇題
 已知難溶性物質K2SO4•MgSO4•2CaSO4在水中存在如下平衡:K2SO4•MgSO4•2CaSO4(s)═2Ca2++2K++Mg2++4SO42-,不同溫度下,K+的浸出濃度與溶浸時間的關系如圖所示,則下列說法錯誤的是( )
已知難溶性物質K2SO4•MgSO4•2CaSO4在水中存在如下平衡:K2SO4•MgSO4•2CaSO4(s)═2Ca2++2K++Mg2++4SO42-,不同溫度下,K+的浸出濃度與溶浸時間的關系如圖所示,則下列說法錯誤的是( )| A. | 向該體系中加入飽和NaOH溶液,溶解平衡向右移動 | |
| B. | 向該體系中加入飽和碳酸鈉溶液,溶解平衡向右移動 | |
| C. | 該平衡的Ksp=c(Ca2+)•c(K+)•c(Mg2+)•c(SO42-) | |
| D. | 升高溫度,反應速率增大,平衡向正反應方向移動 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 從結構上推斷,木糖分子中有多個羥基,因而能溶于水 | |
| B. | 木糖屬于單糖 | |
| C. | 木糖屬還原性糖,1mol木糖與足量的銀氨溶液完全反應可生成108g銀 | |
| D. | 木糖能發生酯化、氧化、加成等反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
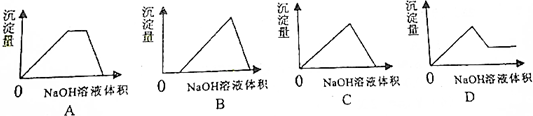
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 電力 | B. | 核能 | C. | 太陽能 | D. | 氫能 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 微粒符號 | 化學鍵類型 | 化合物類型 |
| HCl | 共價鍵 | 共價鍵化合物 |
| NaCl | 離子鍵 | 離子化合物 |
| NaOH | 離子鍵和共價鍵 | 離子化合物 |
| NH4Cl | 離子鍵和共價鍵 | 離子化合物 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 稀硫酸滴在銅片上:Cu+2H+=Cu2++H2↑ | |
| B. | 氫氧化鋇與稀硫酸混合:SO42-+H++OH-+Ba2+=H2O+BaSO4↓ | |
| C. | 用稀硫酸洗去鐵銹:Fe2O3+6H+=2 Fe3++3H2O | |
| D. | 石灰乳與Na2CO3溶液混合:Ca2++CO32-=CaCO3↓ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 平衡狀態是一種靜止的狀態,因為反應物和生成物的濃度已經不再改變 | |
| B. | 化學反應的限度不可以通過改變條件而改變 | |
| C. | 當一個可逆反應達到平衡狀態時,這就是這個反應所能達到的限度 | |
| D. | 當一個可逆反應達到平衡狀態時,那么這個反應的正反應速率和逆反應速率為零 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com