
| A、熱穩定性:HCl>PH3>H2S |
| B、堿性:NaOH<Mg(OH)2<Al(OH)3 |
| C、原子半徑:O>S>Na |
| D、結合氫離子能力:CO32->HCO3->SO42- |


科目:高中化學 來源: 題型:
| A、1.8g的NH4+離子中含有的電子數為0.1NA | ||
| B、常溫常壓下,48gO3和O2的混合物含有的氧原子數為3NA | ||
| C、11.2L氧氣中所含有的氧原子數為NA | ||
D、標準狀況下,1L水所含分子數為
|
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、氯水和SO2使品紅溶液褪色及SO2可使酸性高錳酸鉀溶液褪色的原理不同 |
| B、向某溶液中加入氯化鋇溶液生成白色沉淀,再加稀硝酸,白色沉淀不消失該原溶液一定含有SO42- |
| C、用KSCN溶液鑒別FeCl2溶液、FeCl3溶液 |
| D、用氫氟酸雕刻玻璃,是由于氫氟酸能與二氧化硅反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| 選項 | 實驗操作 | 實驗現象 | 結 論 | ||
| A | 測定等濃度的Na2CO3和Na2SO3溶液的pH | 前者pH比后者的大 | 非金屬性:S>C | ||
| B | SO2通入酸性高錳酸鉀溶液 | 高錳酸鉀溶液褪色 | SO2具有漂白性 | ||
| C | 向某溶液中滴加稀NaOH溶液,將濕潤紅色石蕊試紙置于試管口 | 試紙不變藍 | 原溶液中無N
| ||
| D | 向等濃度的KCl、KI混合液中滴加AgNO3溶液 | 先出現黃色沉淀 | Ksp(AgCl)>Ksp(AgI) |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化學 來源: 題型:
 (1)硫酸是重要的化工材料,二氧化硫生成三氧化硫是工業制硫酸的重要反應之一.
(1)硫酸是重要的化工材料,二氧化硫生成三氧化硫是工業制硫酸的重要反應之一.查看答案和解析>>
科目:高中化學 來源: 題型:
| A、①②⑤ | B、②③④ |
| C、②③⑥ | D、全部 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| ||
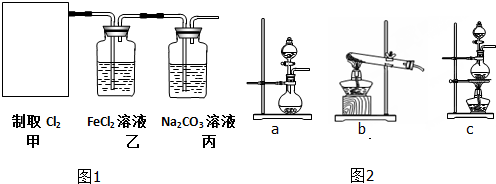
查看答案和解析>>
科目:高中化學 來源: 題型:
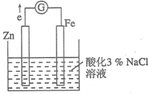 某化學興趣小組對電化學問題進行了實驗探究.利用如圖裝置探究金屬的防護措施,實驗現象是鋅電極不斷溶解,鐵電極表面有氣泡產生.
某化學興趣小組對電化學問題進行了實驗探究.利用如圖裝置探究金屬的防護措施,實驗現象是鋅電極不斷溶解,鐵電極表面有氣泡產生.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com