
元素周期表中鉍元素的數據見下圖,下列說法正確的是

A. Bi元素的質量數是83 B. Bi元素的相對原子質量是209.0
C. Bi原子6p能級有一個未成對電子 D. Bi原子最外層有5個能量相同的電子
 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源:2017屆貴州省凱里市高三3月聯考理綜化學試卷(解析版) 題型:選擇題
化學與生產、生活、社會密切相關,下列有關說法正確的是
A. 汽車尾氣污染物中含有氮的氧化物,是汽油不完全燃燒造成的
B. 為了防止月餅等富酯食品氧化變質,延長食品的保質期,常在包裝袋中放入生石灰
C. 魚、蝦等海鮮用福爾馬林防腐保鮮
D. 干電池即使不用,放置過久,也可能漏液失效,其原因是電解質溶液NH4Cl顯酸性和外殼鋅反應
查看答案和解析>>
科目:高中化學 來源:2017屆江蘇省南通市高三高考全真模擬(二)化學試卷(解析版) 題型:選擇題
探究濃硫酸和銅的反應,下列裝置或操作正確的是( )
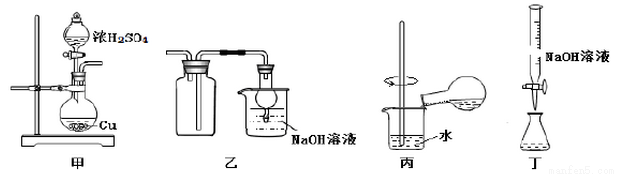
A.用裝置甲進行銅和濃硫酸的反應
B.用裝置乙收集二氧化硫并吸收尾氣
C.用裝置丙稀釋反應后的混合液
D.用裝置丁測定余酸的濃度
查看答案和解析>>
科目:高中化學 來源:2016-2017學年安徽省淮北市高二下學期第一次月考化學試卷(解析版) 題型:選擇題
化學中常用圖像直觀地描述化學反應的進程或結果,下列圖像描述正確的是
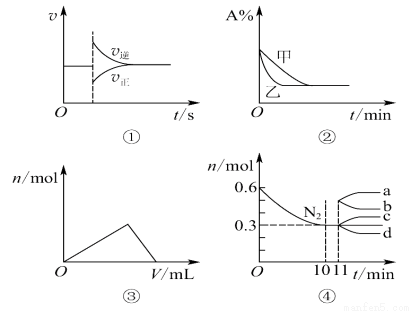
A.圖①可以表示對某化學平衡體系改變溫度后反應速率隨時間的變化
B.圖②表示壓強對可逆反應2A(g)+2B(g)  3C(g)+D(g)的影響,且甲的壓強大
3C(g)+D(g)的影響,且甲的壓強大
C.圖③表示向Al2(SO4)3和MgSO4的混合液中滴加NaOH溶液,生成沉淀的量與滴入NaOH溶液體積的關系
D.圖④表示在2 L的密閉容器中發生合成氨反應時N2的物質的量隨時間的變化曲線,0~10 min內該反應的平均速率v(H2)=0.045 mol·L-1·min-1,從11 min起其他條件不變,壓縮容器的體積為1 L,則n(N2)的變化曲線為d
查看答案和解析>>
科目:高中化學 來源:2016-2017學年安徽省淮北市高二下學期第一次月考化學試卷(解析版) 題型:選擇題
工業廢氣H2S經資源利用后可回收能量并得到單質硫。反應原理如圖所示。下列說法不正確的是
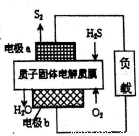
A. 電極a為電池的負極
B. 電極b上發生的電極反應為O2+4H++4e-=2H2O
C. 若電路中通過2mol電子,則電池內部釋放632kJ熱量
D. 若有17gH2S參與反應,則會有1molH+經質子膜進入正極區
查看答案和解析>>
科目:高中化學 來源:2017屆內蒙古包頭市高三下學期第一次模擬考試理綜化學試卷(解析版) 題型:實驗題
直接排放含SO2的煙氣會形成酸雨,危害環境。某化學興趣小組進行如下有關SO2性質和含量測定的探究活動。
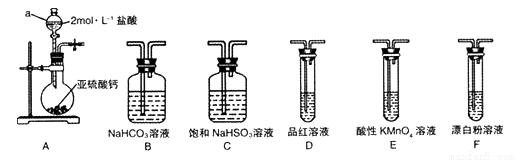
(1)裝置A中儀器a的名稱為__________。若利用裝置A中產生的氣體證明+4價的硫元素具有氧化性,試用化學方程式表示該實驗方案的反應原理________________。
(2)選用圖4中的裝置和藥品探究亞硫酸與次氯酸的酸性強弱:
①甲同學認為按A→C→F→尾氣處理順序連接裝置可以證明亞硫酸和次氯酸的酸性強弱,乙同學認為該方案不合理,其理由是_________________。
②丙同學設計的合理實驗方案為:按照A→C→_________→F→尾氣處理(填字母) 順序連接裝置。證明亞硫酸的酸性強于次氯酸的酸性的實驗現象是_____________________。
③其中裝置C的作用是__________。常溫下,測得裝置C中飽和NaHSO3溶液的pH≈5,則該溶液中所有離子的濃度由大到小的順序為__________________。(已知0.1mol/L的H2SO3溶液pH >1)
(3)為了測定裝置A殘液中SO2的含量,量取10.00 mL殘液于圓底燒瓶中,加熱使SO2 全部蒸出,用20.00 mL0.0500 mol/L的KMnO4溶液吸收。充分反應后,再用0.2000mol/L的KI標準溶液滴定過量的KMnO4 ,消耗KI溶液15.00 mL。
已知:5SO2+2MnO4-+2H2O=2Mn2++5SO42-+4H+
10I-+2MnO4-+16H+=2Mn2++5I2+8H2O
①殘液中SO2的含量為_______g·L-1。
②若滴定過程中不慎將KI標準溶液滴出錐形瓶外少許,使測定結果_______(填“偏高”、“偏低”或“無影響”)。
查看答案和解析>>
科目:高中化學 來源:2017屆內蒙古包頭市高三下學期第一次模擬考試理綜化學試卷(解析版) 題型:選擇題
短周期主族元素甲、乙、丙、丁、戊的原子序數依次增大,甲和乙形成的氣態化合物的水溶液呈堿性,甲和丙同主族,丁原子最外層電子數與電子層數相等,在中學常見的酸中戊的最髙價氧化物對應的水化物的酸性最強。下列敘述錯誤的是( )
A. 氧元素與甲、乙、丙形成的二元化合物均只有兩種
B. 簡單離子半徑:戊 >乙>丙>丁
C. 甲、乙、戊三種元素可形成含有共價鍵的離子化合物
D. 丙、丁、戊三種元素的最高價氧化物對應的水化物兩兩之間均能發生反應
查看答案和解析>>
科目:高中化學 來源:2016-2017學年江西省高一下學期第一次月考化學試卷(解析版) 題型:選擇題
下面是元素周期表的一部分(表中數字和X代表原子序數),其中X為53的是
A. 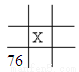 B.
B. 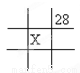 C.
C. 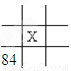 D.
D. 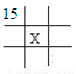
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com