
【題目】實驗室以工業(yè)鈷渣為原料制取CoSO4溶液和ZnSO4·7H2O晶體,其實驗流程如下:
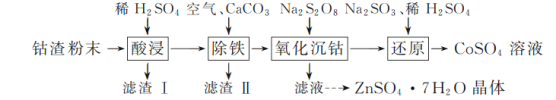
已知:①“酸浸”所得溶液中主要含CoSO4、ZnSO4,另含少量FeSO4、NiSO4。②金屬活動性:Ni介于Fe、Cu之間。③下表是相關金屬離子生成氫氧化物沉淀的pH(開始沉淀的pH按金屬離子濃度1 mol·L-1計算,pH>11時Zn(OH)2能溶于NaOH溶液生成[Zn(OH)4]2-):
金屬離子 | 開始沉淀的pH | 完全沉淀的pH |
Co2+ | 7.6 | 9.4 |
Zn2+ | 5.9 | 8.9 |
(1)“酸浸”時所加稀硫酸不宜過量太多的原因是________。
(2)“除鐵”時,向溶液中持續(xù)鼓入空氣的作用是________。
(3)流程中需將濾渣Ⅰ、濾渣Ⅱ的洗滌液與“除鐵”后所得濾液合并,目的是________。
(4)寫出“還原”過程中Na2SO3、稀H2SO4與Co(OH)3反應的離子方程式:________。
(5)實驗所得CoSO4溶液可用于制備CoCO3,制備時CoSO4飽和溶液與Na2CO3飽和溶液的混合方式為________。
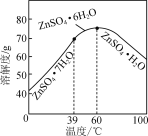
(6)請結合如圖硫酸鋅晶體的溶解度曲線,設計從“氧化沉鈷”后的濾液(含ZnSO4、Na2SO4、NiSO4等)中獲取ZnSO4·7H2O的實驗方案:取適量濾液,____________________________,過濾,用少量冰水洗滌,低溫干燥得ZnSO4·7H2O晶體。(實驗中須使用的試劑有:Zn粉、1.0 mol·L-1 NaOH、1.0 mol·L-1 H2SO4)
【答案】避免除鐵時消耗過多的CaCO3 將Fe2+氧化,攪拌溶液,加快反應速率 為提高Co、Zn的回收率 SO![]() +2Co(OH)3+4H+=2Co2++SO
+2Co(OH)3+4H+=2Co2++SO![]() +5H2O 將Na2CO3飽和溶液緩慢滴加到CoSO4飽和溶液中,并不斷攪拌 向其中加入過量的Zn粉后過濾,向所得濾液中滴加1.0 mol·L-1 NaOH,控制pH約為10(8.9~11)使Zn2+完全沉淀,所得沉淀洗凈后用1.0 mol·L-1 H2SO4完全溶解,將所得溶液蒸發(fā)濃縮至有晶膜出現(xiàn),冷卻至0 ℃(39 ℃以下)結晶
+5H2O 將Na2CO3飽和溶液緩慢滴加到CoSO4飽和溶液中,并不斷攪拌 向其中加入過量的Zn粉后過濾,向所得濾液中滴加1.0 mol·L-1 NaOH,控制pH約為10(8.9~11)使Zn2+完全沉淀,所得沉淀洗凈后用1.0 mol·L-1 H2SO4完全溶解,將所得溶液蒸發(fā)濃縮至有晶膜出現(xiàn),冷卻至0 ℃(39 ℃以下)結晶
【解析】
鈷渣中加稀硫酸將可溶于酸的物質轉變成硫酸鹽,難溶于硫酸的進入濾渣1,得到溶液中主要含CoSO4、ZnSO4,另含少量FeSO4、NiSO4,濾液中通入氧氣亞鐵離子氧化成三價鐵離子,加碳酸鈣中和硫酸調節(jié)pH值將鐵沉淀除去,過濾后濾液中加Na2S2O8,氧化沉淀鈷,過濾得鈷的沉淀物加亞硫酸鈉和稀硫酸還原的得到硫酸鈷,濾液中主要是硫酸鋅,除去雜質后經(jīng)過蒸發(fā)濃縮、冷卻結晶、過濾得到ZnSO4·7H2O晶體,據(jù)此分析解答。
(1)“酸浸”時所加稀硫酸不宜過量太多,因后續(xù)步驟中要加碳酸鈣調節(jié)溶液pH值,硫酸過多會增加碳酸鈣的用量,故答案為:避免除鐵時消耗過多的CaCO3;
(2)因為原溶液中的鐵是二價鐵,二價鐵直接沉淀時需要調控的pH較大且會使其他金屬陽離子沉淀,因此以溶解度更小的氫氧化鐵形式除鐵更合理,需通入空氣將亞鐵離子氧化,同時持續(xù)鼓入空氣可以起到攪拌溶液加快速率的作用,故答案為:將Fe2+氧化,攪拌溶液,加快反應速率;
(3)流程中需將濾渣Ⅰ、濾渣Ⅱ的洗滌液與“除鐵”后所得濾液合并可以減少鈷和鋅的損失,提高兩者的回收率,故答案為:為提高Co、Zn的回收率;
(4)還原”過程中Na2SO3、稀H2SO4與Co(OH)3反應產物為硫酸鈷和硫酸鈉,可得方程式為:SO![]() +2Co(OH)3+4H+=2Co2++SO
+2Co(OH)3+4H+=2Co2++SO![]() +5H2O,故答案為:SO
+5H2O,故答案為:SO![]() +2Co(OH)3+4H+=2Co2++SO
+2Co(OH)3+4H+=2Co2++SO![]() +5H2O;
+5H2O;
(5)實驗所得CoSO4溶液可用于制備CoCO3,制備時CoSO4飽和溶液與Na2CO3飽和溶液的混合方式為將Na2CO3飽和溶液緩慢滴加到CoSO4飽和溶液中,并不斷攪拌,故答案為:將Na2CO3飽和溶液緩慢滴加到CoSO4飽和溶液中,并不斷攪拌;
(6)氧化沉鈷”后的濾液(含ZnSO4、Na2SO4、NiSO4等)中有雜質直接結晶得不到純凈的晶體,因此要先加足量的鋅粉置換出鎳,之后加氫氧化鈉調節(jié)溶液pH將鋅轉變成沉淀后過濾的到氫氧化鋅固體,再將固體溶于硫酸,蒸發(fā)濃縮再冷卻至39 ℃以下結晶,具體操作:向其中加入過量的Zn粉后過濾,向所得濾液中滴加1.0 mol·L-1 NaOH,控制pH約為10(8.9~11)使Zn2+完全沉淀,所得沉淀洗凈后用1.0 mol·L-1 H2SO4完全溶解,將所得溶液蒸發(fā)濃縮至有晶膜出現(xiàn),冷卻至0 ℃(39 ℃以下)結晶,故答案為:向其中加入過量的Zn粉后過濾,向所得濾液中滴加1.0 mol·L-1 NaOH,控制pH約為10(8.9~11)使Zn2+完全沉淀,所得沉淀洗凈后用1.0 mol·L-1 H2SO4完全溶解,將所得溶液蒸發(fā)濃縮至有晶膜出現(xiàn),冷卻至0 ℃(39 ℃以下)結晶。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:
【題目】可逆反應:A(g)+B(g) ![]() C(s)+2D(g)的ΔH>0,下圖所示為正逆反應速率(v)與時間(t)的關系,如果在t1時刻改變以下條件:①加入A;②加入催化劑;③加壓;④升溫;⑤移走C,符合圖示的條件是( )。
C(s)+2D(g)的ΔH>0,下圖所示為正逆反應速率(v)與時間(t)的關系,如果在t1時刻改變以下條件:①加入A;②加入催化劑;③加壓;④升溫;⑤移走C,符合圖示的條件是( )。
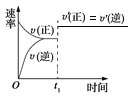
A. ②③B. ①②C. ③④D. ④⑤
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(I)請根據(jù)官能團的不同對下列有機物進行分類。
①CH3CH2OH ②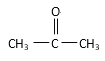 ③CH3CH2Br ④CH3COOCH2CH3 ⑤
③CH3CH2Br ④CH3COOCH2CH3 ⑤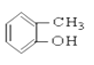 ⑥
⑥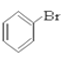 ⑦CH3CHO ⑧HCOOH ⑨
⑦CH3CHO ⑧HCOOH ⑨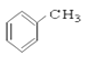 ⑩
⑩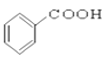
(1)芳香烴:____________
(2)鹵代烴:______________
(3)醇:__________
(4)酚:______________
(5)醛:______________
(6)酮:_______________
(7)羧酸:___________________
(8)酯:______________________
(Ⅱ)![]() 的分子式為________________,
的分子式為________________,![]() 中含有的官能團的名稱為________________ 。
中含有的官能團的名稱為________________ 。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】實驗室利用如下裝置制取氯化鐵粉末,已知氯化鐵粉末很容易吸水生成結晶化合物FeCl3+6H2O = FeCl3·6H2O
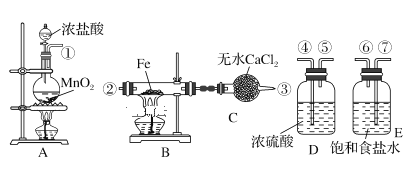
(1)按照氣體流向從左到右順序連接儀器應是(填儀器接口順序,各接口序號間用“—”連接):①—_____。
(2)燒瓶A中反應的離子方程式為________,其中,氧化劑是________(填物質名稱)。
(3)B中反應的化學方程式是_____________。
(4)裝置C的作用是_______________。
(5)A、B中的酒精燈應先點燃____處(填“A”或“B”)的酒精燈,理由是__________。
(6)小明同學認為這套實驗裝置不完整,還須補充________裝置。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】苯酚是一種很有價值的化工原料,年產量可達幾百萬噸。苯酚可合成著名的解熱鎮(zhèn)痛藥——阿司匹林,也可合成聚碳酸酯,其合成路線如下:

(1)阿司匹林分子中的含氧官能團名稱為_______;G的化學名稱是____。
(2)E為飽和一元酮,其結構簡式為________;H和K合成聚碳酸酯的反應類型是_____。
(3)鑒別G和阿司匹林的一種顯色試劑為___________
(4)已知K的相對分子質量為99,其分子式為____________
(5)寫出阿司匹林與足量NaOH溶液反應的化學方程式_________
(6)寫出能同時滿足以下條件的阿司匹林的兩種異構體的結構簡式_______________
①苯環(huán)上只有兩種一氯代物;②含有羧基;③水解產生酚。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列指定反應的離子方程式正確的是( )
A.Na與水反應:Na+2H2O=Na++2OH-+H2↑
B.用NaOH溶液吸收NO2:2NO2+Na++2OH-=NaNO3+NO2-+H2O
C.用MnO2和濃鹽酸反應制備Cl2:MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O
Mn2++Cl2↑+2H2O
D.NaHCO3溶液中加足量Ba(OH)2溶液:2HCO3-+Ba2++2OH-=BaCO3↓+CO32-+2H2O
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】N2H4、N2O4常用作火箭發(fā)射的推進劑。推進劑發(fā)生反應:2N2H4(l)+N2O4(l)=3N2(g)+4H2O(g)。下列有關說法正確的是( )
A.反應每生成0.3 mol N2,轉移電子的數(shù)目為1.6×6.02×1023
B.充有N2O4的密閉容器中存在:N2O4(g)![]() 2NO2(g),當c(N2O4)∶c(NO2)=1∶2時,該可逆反應到達限度
2NO2(g),當c(N2O4)∶c(NO2)=1∶2時,該可逆反應到達限度
C.堿性N2H4—空氣燃料電池工作時,正極電極反應式為O2+2H2O+4e-=4OH-
D.N2H4的水溶液中存在:N2H4+H2O![]() N2H
N2H![]() +OH-,向稀溶液中加水稀釋,
+OH-,向稀溶液中加水稀釋, ![]() 的值變大
的值變大
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】Ⅰ.按要求寫出下列反應的方程式
(1)鋁與足量氫氧化鈉溶液反應的離子方程式 ______
(2)過氧化鈉與水反應的化學方程式 ____
(3) 實驗室制氫氧化鋁的離子方程式 ________
Ⅱ. 請補充完整,配平方程式并用單線橋標出電子轉移方向和數(shù)目
(1)KI+KIO3+H2SO4═I2+K2SO4+H2O:________________________
(2)MnO4-+NO2-+ ═Mn2++NO3-+H2O:_________________________
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在Al2(SO4)3和MgSO4的混合溶液中,滴加NaOH溶液,生成沉淀的量與滴入NaOH溶液的體積關系如下圖所示,則原混合液中Al2(SO4)3與MgSO4的物質的量濃度之比為
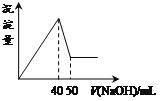
A.1:3B.1:2C.1:1D.2:1
查看答案和解析>>
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com