
分析 ①N2(g)+2O2(g)=2NO2(g)△H1=+67.7kJ/mol
②N2H4(g)+O2(g)=N2(g)+2H2O(l)△H2=-622kJ/mol
③H2O(l)=H2O(g)△H3=+44kJ•mol-1
依據蓋斯定律:②×2-①+③×4計算焓變書寫熱化學方程式.
解答 解:①N2(g)+2O2(g)=2NO2(g)△H1=+67.7kJ/mol
②N2H4(g)+O2(g)=N2(g)+2H2O(l)△H2=-622kJ/mol
③H2O(l)=H2O(g)△H3=+44kJ•mol-1
依據蓋斯定律:②×2-①+③×4得到:2N2H4(g)+2NO2(g)=3N2(g)+4H2O(g)△H=-622×2-67.7+44×4=-1135.7KJ/mol;
故答案為:2N2H4(g)+2NO2(g)=3N2(g)+4H2O(g)△H=-1135.7KJ/mol.
點評 本題考查了熱化學方程式的書寫方法和蓋斯定律的計算應用,題目較簡單.


科目:高中化學 來源: 題型:選擇題
| A. | 硫元素既被氧化又被還原 | |
| B. | 氧化劑與還原劑的物質的量之比為1:2 | |
| C. | 每生成1molNa2S2O3,轉移4mol電子 | |
| D. | 相同條件下,每吸收10m3SO2就會放出5m3CO2 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
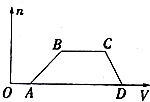 某混合溶液中可能含有H2SO4、MgCl2、Al2(SO4)3、NH4Cl、NaCl中的幾種物質,往該溶液中逐漸加入NaOH溶液,產生沉淀的物質的量(n)與加入的NaOH溶液體積(V)的關系如圖所示.回答下列問題:
某混合溶液中可能含有H2SO4、MgCl2、Al2(SO4)3、NH4Cl、NaCl中的幾種物質,往該溶液中逐漸加入NaOH溶液,產生沉淀的物質的量(n)與加入的NaOH溶液體積(V)的關系如圖所示.回答下列問題:查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 0.1mol/L鹽酸和0.1mol/L醋酸分別與0.2mol/L氫氧化鈉溶液反應的速率相同 | |
| B. | 0.1mol/L鹽酸和0.1mol/L硝酸分別與大小相同的大理石反應的速率相同 | |
| C. | 鋁和鐵分別與0.1mol/L硫酸的反應速率相同 | |
| D. | 大理石塊與大理石粉末分別與0.1mol/L鹽酸反應的速率相同 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
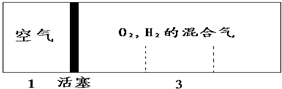
| A. | 2:7 | B. | 5:4 | C. | 1:1 | D. | 7:2 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 制CuSO4時先將Cu氧化成CuO后再與稀硫酸反應 | |
| B. | 采用銀作催化劑,乙烯和氧氣制取環氧乙烷,原子利用率100% | |
| C. | 用乙醇代替汽油作汽車燃料 | |
| D. | 用稀硝酸和銅制取Cu(NO3)2 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 有質子的微粒一定有中子 | |
| B. | 通常所說的氫元素是指${\;}_{1}^{1}$H | |
| C. | 16O中的“16”表示氧元素的近似相對原子質量 | |
| D. | 根據反應K35ClO3+6H37Cl=KCl+3Cl2↑+3H2O得到的Cl2,其相對分子質量為73.3 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 .
.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com