
| A. | 取少量溶液X,向其中加入適量新制氯水,再加幾滴KSCN溶液,溶液變紅,說明X溶液中一定含有Fe2+ | |
| B. | 向1 mL 1%的NaOH溶液中加入2 mL 2%的CuSO4溶液,振蕩后再加入0.5 mL有機物X,加熱后未出現磚紅色沉淀,說明X中不含有醛基 | |
| C. | 向CuSO4溶液中加入KI溶液,有白色沉淀生成,再加入四氯化碳振蕩,四氯化碳層呈紫色,說明白色沉淀可能為CuI | |
| D. | 向濃度均為0.1 mol•L-1的MgCl2、CuCl2混合溶液中逐滴加入氨水,首先生成藍色沉淀,說明Ksp[Cu(OH)2]>Ksp[Mg(OH)2] |
分析 A.驗證亞鐵離子的存在,首先應排除鐵離子干擾,正確順序是先加入硫氰化鉀觀察現象后再滴加氯水;
B.NaOH不足,反應后溶液不為堿性;
C.發生氧化還原反應生成CuI和碘單質;
D.逐滴加入氨水,首先生成藍色沉淀,則溶度積小的Cu(OH)2先沉淀.
解答 解:A.驗證亞鐵離子的存在,首先應排除鐵離子干擾,正確順序是先加入硫氰化鉀觀察現象后再滴加氯水,故A錯誤;
B.向1 mL 1%的NaOH溶液中加入2 mL 2%的CuSO4溶液,NaOH不足,反應后溶液不為堿性,則不能發生醛基被氧化的反應,故B錯誤;
C.向CuSO4溶液中加入KI溶液,有白色沉淀生成,再加入四氯化碳振蕩,四氯化碳層呈紫色,則發生氧化還原反應生成白色沉淀CuI和碘單質,故C正確;
D.逐滴加入氨水,首先生成藍色沉淀,則溶度積小的Cu(OH)2先沉淀,則Ksp[Cu(OH)2]<Ksp[Mg(OH)2],故D錯誤;
故選C.
點評 本題考查化學實驗方案的評價,為高頻考點,涉及氧化還原反應、離子檢驗、沉淀的生成等,把握物質的性質、化學反應原理為解答的關鍵,側重分析與實驗能力的考查,題目難度不大.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
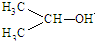 可簡寫為
可簡寫為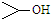 .達菲是世界衛生組織推薦的抗禽流感藥物,其結構簡式如圖(
.達菲是世界衛生組織推薦的抗禽流感藥物,其結構簡式如圖(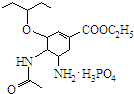 ),有關它的說法錯誤的是( )
),有關它的說法錯誤的是( )| A. | 達菲是一種磷酸鹽 | |
| B. | 達菲分子中含有肽鍵 | |
| C. | 達菲的分子式為C16H31N2O8P | |
| D. | 1mol達菲可與2mol H2發生加成反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
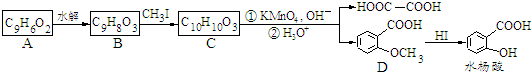
 .
.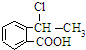 合成
合成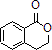 ,寫出相關化學反應方程式
,寫出相關化學反應方程式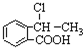 +NaOH$→_{△}^{醇}$
+NaOH$→_{△}^{醇}$ +H2O+NaCl、
+H2O+NaCl、 +HBr$\stackrel{過氧化物}{→}$
+HBr$\stackrel{過氧化物}{→}$ 、
、 +NaOH$\stackrel{△}{→}$
+NaOH$\stackrel{△}{→}$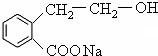 ++NaBr+H2O、2
++NaBr+H2O、2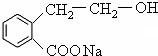 +H2SO4$\stackrel{△}{→}$2
+H2SO4$\stackrel{△}{→}$2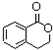 +2H2O+Na2SO4.
+2H2O+Na2SO4.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 28g N2、N2O、N2O4的混合氣體含有氮原子數為2NA | |
| B. | 質量均為7.8 g Na2S、Na2O2的固體中含有的陰離子數均為0.1NA | |
| C. | 0.5 mol•L-1的乙酸溶液中,乙酸分子的數目小于0.5NA | |
| D. | 78g苯分子中含有碳碳雙鍵數為3 NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 序號 | 氧化劑 | 還原劑 | 其他反應物 | 氧化產物 | 還原產物 |
| ① | Cl2 | FeI2 | I2 | ||
| ② | KClO3 | 濃鹽酸 | Cl2 | ||
| ③ | KMnO4 | H2O2 | O2 | Mn2+ |
| A. | 表中①組的反應中氧化產物一定是I2 | |
| B. | 氧化性強弱的比較:KClO3>Cl2>Fe3+>I2 | |
| C. | 表中②組每生成1molCl2,轉移1mol電子 | |
| D. | 表中③組其他反應物可以為濃鹽酸 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
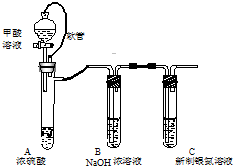 銀氨溶液可用于檢測CO氣體,實驗室研究的裝置如圖:
銀氨溶液可用于檢測CO氣體,實驗室研究的裝置如圖:查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com