
| A. | 標準狀況下,3.36L氧氣與2.4g碳反應,生成CO2分子數為0.2NA | |
| B. | 標準狀況下,1.12LCl2發生反應轉移的電子數一定為0.1NA | |
| C. | lL0.lmol•L-1氨水中NH3•H2O分子數為0.1NA | |
| D. | 10g46%酒精(C2H5OH)中含氧原子總數大于0.1NA |
分析 A.依據n=$\frac{V}{Vm}$=$\frac{m}{M}$計算氧氣、碳的物質的量,結合C+O2$\frac{\underline{\;\;△\;\;}}{\;}$CO2解答;
B.氯氣參加反應轉移電子數與氯氣表現性質有關;
C.一水合氨為弱電解質,部分電離;
D.水溶液中水中也含氧原子.
解答 解:A.標準狀況下,3.36L氧氣物質的量為:$\frac{3.36L}{22.4L/mol}$=0.15mol,與2.4g碳物質的量為$\frac{2.4g}{12g/mol}$=0.2mol反應,依據C+O2$\frac{\underline{\;\;△\;\;}}{\;}$CO2可知氧氣不足,所以生成二氧化碳分子數小于0.2NA,故A錯誤;
B.氯氣參加反應轉移電子數與氯氣表現性質有關,例如氯氣與鐵反應生成氯化鐵,1mol氯氣反應失去2mol電子,1mol氯氣與氫氧化鈉反應生成氯化鈉、次氯酸鈉,氯氣既做氧化劑又做還原劑,反應轉移1mol電子,故B錯誤;
C.一水合氨為弱電解質,部分電離,所以lL0.lmol•L-1氨水中NH3•H2O分子數小于0.1NA,故C錯誤;
D.溶劑水中含有氧原子,10g46%酒精水溶液含氧原子總數大于0.1NA,故D正確;
故選:D.
點評 本題考查阿伏加德羅常數的有關計算和判斷,熟練掌握以物質的量為中心的各化學量與阿伏加德羅常數的關系,注意氣體摩爾體積使用條件和對象,題目難度不大.


科目:高中化學 來源: 題型:選擇題
| A. | 乙苯和鄰二甲苯屬于同分異構體 | |
| B. | 苯和苯乙烯屬于同系物 | |
| C. | 糖類和蛋白質都屬于天然高分子化合物 | |
| D. | 植物油和礦物油都屬于油脂 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
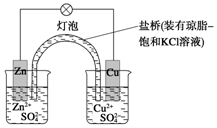 銅鋅原電池(如圖)工作時
銅鋅原電池(如圖)工作時查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 6:1 | B. | 5:1 | C. | 3:1 | D. | 2:1 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
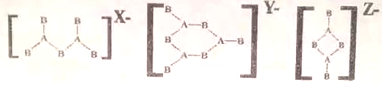
| A. | 4、4、2 | B. | 4、3、2 | C. | 3、3、2 | D. | 4、2、2 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
 一定條件下,體積為10L的密閉容器中,1molX和1mol Y進行反應:2X(g)+2Y(g)?Z(g),經60s達到平衡,生成0.3molZ.下列說法正確的是( )
一定條件下,體積為10L的密閉容器中,1molX和1mol Y進行反應:2X(g)+2Y(g)?Z(g),經60s達到平衡,生成0.3molZ.下列說法正確的是( )| A. | 若升高溫度,X的體積分數增大,則正反應的△H>0 | |
| B. | 將容器體積變為20L,Z的平衡濃度變為原來的$\frac{1}{2}$ | |
| C. | 以X濃度變化表示的反應速率為0.001mol/(L•s) | |
| D. | 若圖縱坐標是正反應速率,則反應應該在絕熱條件下進行,圖象最高點為平衡點 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com