
| A. | 標準狀況下,2.24LSO3含有的分子數等于0.1NA | |
| B. | 1 mol Na2O2所含陰離子數為2NA | |
| C. | 常溫常壓下,16gO2 和O3的混合氣體含有的氧原子數為NA | |
| D. | 常溫常壓和光照條件下,33.6 LCl2與3.0g H2反應,生成的HCl分子數目為3NA |
分析 A、標況下,三氧化硫為固體;
B、過氧化鈉由2個鈉離子和1個過氧根構成;
C、氧氣和臭氧均由氧原子構成;
D、常溫常壓下,氣體摩爾體積大于22.4L/mol.
解答 解:A、標況下,三氧化硫為固體,故不能根據其體積來計算其物質的量,故A產物;
B、過氧化鈉由2個鈉離子和1個過氧根構成,故1mol過氧化鈉中含1mol陰離子即NA個,故B錯誤;
C、氧氣和臭氧均由氧原子構成,故16g混合物中含有的氧原子的物質的量n=$\frac{16g}{16g/mol}$=1mol,即NA個,故C正確;
D、常溫常壓下,氣體摩爾體積大于22.4L/mol,故33.6L氯氣的物質的量小于1.5mol,則生成的HCl分子個數小于3NA個,故D錯誤.
故選C.
點評 本題考查了阿伏伽德羅常數的有關計算,熟練掌握公式的使用和物質的結構是解題關鍵,難度不大.


 精英口算卡系列答案
精英口算卡系列答案科目:高中化學 來源: 題型:解答題
| 元素編號 | 元素性質與原子(或分子)結構 |
| T | 最外層電子數是次外層電子數的3倍 |
| X | 常溫下單質分子為雙原子分子,分子中含有3對共用電子對 |
| Y | M層比K層少1個電子 |
| Z | 第三周期元素的金屬離子中半徑最小 |
 .
.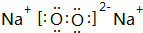 .
.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 煤燃燒時將化學能全部轉化為熱能 | |
| B. | 原電池將化學能轉化為電能 | |
| C. | 二次電池充電時將電能轉化為化學能 | |
| D. | 鎂條燃燒時將部分化學能轉化為光能 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ | ⑩ |
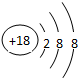 .元素⑩名稱為溴單質與水反應化學方程式Br2+H2O=HBr+HBrO.
.元素⑩名稱為溴單質與水反應化學方程式Br2+H2O=HBr+HBrO.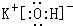 .
.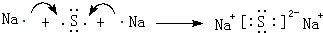 ,該化合物屬于離子(填“共價”或“離子”)化合物.
,該化合物屬于離子(填“共價”或“離子”)化合物.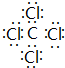 、
、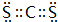 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 純凈的乙酸又稱為冰醋酸 | B. | 乙酸能與金屬鈉反應放出氫氣 | ||
| C. | 乙酸的酸性比碳酸強 | D. | 乙酸與乙醇不互溶 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
 E的氫化物的分子式H2O.
E的氫化物的分子式H2O. .
.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 如圖表示一個電解池,裝有電解液a;X、Y是兩塊電極板,通過導線與直流電源相連.請回答以下問題:
如圖表示一個電解池,裝有電解液a;X、Y是兩塊電極板,通過導線與直流電源相連.請回答以下問題:查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com