
| 選項 | 實驗操作 | 現象 | 結論 |
| A | 溶液中加入鹽酸,再滴加BaCl2溶液 | 先無現象,后產生白色沉淀 | 原溶液中有SO42- |
| B | 向兩份蛋白質溶液中分別滴加飽和Na2SO4溶液和CuSO4溶液 | 均有固體析出 | 蛋白質均發生變性 |
| C | 將Mg、Al與NaOH溶液組成原電池 | Mg電極溶解 | Mg比Al金屬活動性強 |
| D | 向稀HNO3溶液中加入過量鐵粉充分反應后,滴入KSCN溶液 | 溶液變為血紅色 | 和HNO3具有氧化性,能將Fe氧化成Fe3+ |
| A. | A | B. | B | C. | C | D. | D |
分析 A.先加入鹽酸,可排除陰離子的干擾;
B.蛋白質與Na2SO4溶液發生鹽析;
C.將Mg、Al與NaOH溶液組成原電池,鋁為負極;
D.向稀HNO3溶液中加入過量鐵粉充分反應生成Fe2+.
解答 解:A.先加入鹽酸,可排除陰離子的干擾,再加入氯化鋇生成沉淀,可證明原溶液中有SO42-,故A正確;
B.蛋白質與Na2SO4溶液發生鹽析,硫酸銅溶液可使蛋白質變性,故B錯誤;
C.將Mg、Al與NaOH溶液組成原電池,鋁為負極,鋁溶解,故C錯誤;
D.向稀HNO3溶液中加入過量鐵粉充分反應生成Fe2+,滴入KSCN溶液,溶液不變為血紅色,故D錯誤.
故選A.
點評 本題考查較為綜合,涉及物質的檢驗以及元素化合物知識,側重于學生的分析能力和實驗能力的考查,為高考常見題型,難度大不,注意把握實驗操作的原理和實驗方法.


 學練快車道快樂假期寒假作業系列答案
學練快車道快樂假期寒假作業系列答案科目:高中化學 來源: 題型:選擇題
| A. | 某溫度下,0.1mol•L-1的醋酸溶液PH=3,則其電離常數Ka≈1.0×10-4 | |
| B. | Ka、Kb、Kh均隨溫度升高而增大 | |
| C. | 弱酸HA的電離平衡常數為Ka,則A-的水解平衡常數為Kh=Ka•Kw | |
| D. | 因為Ksp(AgCl)<Ksp(AgOH),所以AgCl不溶于稀硝酸 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 30gNO含有的原子數目為NA | |
| B. | 常溫常壓下,22.4LH2含有的分子數目為NA | |
| C. | 5.6g鐵與足量氯氣完全反應失去的電子數目為0.2NA | |
| D. | 1L1mol•L-1Na2SO4溶液中含有的鈉離子數目為2NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Ag是還原劑 | B. | O2被還原 | C. | H2S發生氧化反應 | D. | Ag2S是氧化產物 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
 | 甲 | 乙 | 丙 |
| A | NaHCO3 | HCl | Ca(OH)2 |
| B | O2 | SO2 | NaOH |
| C | NH3 | NO2 | H2O |
| D | H2SO4(濃) | Fe | S |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
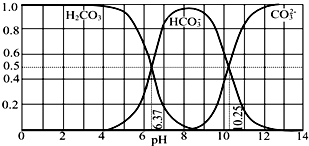
| A. | pH=10.25時,c(Na+)═c(CO32-)+c(HCO3-) | |
| B. | 為獲得盡可能純的NaHCO3,宜控制溶液的pH為7~9之間 | |
| C. | 根據圖中數據,可以計算得到H2CO3第一步電離的平衡常數K1(H2CO3)=10-6.37 | |
| D. | 若是0.1mol NaOH 反應后所得的1L溶液,pH=10時,溶液中存在以下關系:c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+) |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com