
下列與化學反應能量變化相關的敘述正確的是( )
A.生成物總能量一定小于反應物總能量
B.放熱反應的反應速率總是大于吸熱反應的反應速率
C.應用蓋斯定律,可計算某些難以直接測量的反應焓變
D.同溫同壓下,H2(g)+Cl2(g) 2HCl(g)在光照和點燃條件下的ΔH不同
2HCl(g)在光照和點燃條件下的ΔH不同
 第1卷單元月考期中期末系列答案
第1卷單元月考期中期末系列答案科目:高中化學 來源:2015-2016學年江蘇省高一下期末化學試卷(解析版) 題型:選擇題
下列化學用語表示正確的是
A.硫原子的結構示意圖: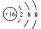
B.HCl的電子式: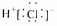
C.乙酸的結構式:C2H4O2
D.硫酸鈉的電離方程式:Na2SO4=2Na++SO42-
查看答案和解析>>
科目:高中化學 來源:2015-2016學年云南省高二下學期期中化學試卷(解析版) 題型:填空題
下圖是一個簡易測量物質反應是吸熱還是放熱的實驗裝置,利用此裝置可以很方便地測得某反應是放熱反應還是吸熱反應。請根據裝置回答下列問題:

(1)將鋁片加入小試管內,然后注入足量的鹽酸,有關反應的離子方程式是_____________________,試管中看到的現象是_______________________。
(2)彎管中A端液面________(填“上升”或“下降”),原因是_________________;說明此反應是________(填“放熱”或“吸熱”)反應。
查看答案和解析>>
科目:高中化學 來源:2015-2016學年云南省高二下學期期中化學試卷(解析版) 題型:選擇題
有如下4種碳架的烴,則下列判斷正確的是( )

A.a和d是同分異構體
B.b和c不是同系物
C.a和d都能發生加成反應
D.只有b和c能發生取代反應
查看答案和解析>>
科目:高中化學 來源:2015-2016學年云南省高二下學期期中化學試卷(解析版) 題型:選擇題
化學實驗必須注意安全,下列做法不存在安全隱患的是( )
A. 制取乙酸乙酯時,先將1體積的酒精倒入3體積的濃硫酸中
B. 配制銀氨溶液時,將稀氨水滴加到硝酸銀溶液中至白色沉淀恰好溶解為止
C. 實驗室做鈉與乙醇的實驗時,余下的鈉投入廢液缸中
D. 制乙烯時,用量程為100 ℃的溫度計代替量程為300 ℃的溫度計,測反應液的溫度
查看答案和解析>>
科目:高中化學 來源:2015-2016學年新疆農業大學附中高一下學期期中化學試卷(解析版) 題型:填空題
據圖回答下列問題:
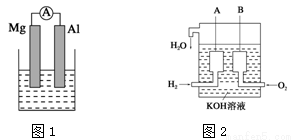
(1)若燒杯中溶液為稀硫酸,則圖1裝置中觀察到的現象是 ;
(2)美國阿波羅宇宙飛船上使用了一種新型裝置,其構造如上圖2所示:A、B兩個電極均由多孔的碳塊組成。該電池中A極發生 反應(填“氧化”或“還原”);如果將上述裝置中通入的H2改成甲烷(CH4),也可以組成一個原電池裝置,則該電池的負極反應式為 。
查看答案和解析>>
科目:高中化學 來源:2015-2016學年新疆農業大學附中高一下學期期中化學試卷(解析版) 題型:選擇題
甲醇燃料電池(DMFC)可用于筆記本電腦、汽車等,它一極通入甲醇;電解質是質子交換膜,它能傳導氫離子。電池工作時,甲醇被氧化為二氧化碳和水。下列敘述中,不正確的是
A.負極的反應式為: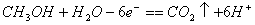
B. 氧氣在電極上的反應是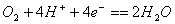
C. 通入甲醇的一極為負極,通入氧氣的一極為正極
D. 燃料電池的能量轉化率能達到100%
查看答案和解析>>
科目:高中化學 來源:2015-2016學年新疆農業大學附中高二下學期期中化學試卷(解析版) 題型:填空題
請仔細觀察下列五種裝置的構造示意圖,完成下列問題。
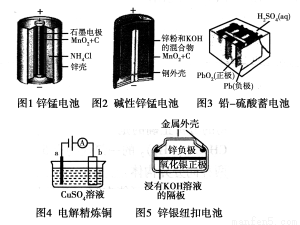
(1)鋅錳電池存在自放電現象,主要原因是鋅與NH4Cl反應,請結合離子方程式與文字說明原因:
。
(2)堿性鋅錳電池的總反應式:Zn+2MnO2+2H2O===2MnOOH+Zn(OH)2,則負極的電極反應式:________________。
(3)鉛-硫酸蓄電池放電的總反應式:Pb+PbO2+2H2SO4=2PbSO4+2H2O,充電過程中,陽極附近c(SO42-)濃度將________(填“變大”、“變小”或“不變”),充電時陰極的電極反應式為:________________。
(4)電解精煉銅時,a極是________(填“純銅”或“粗銅”)。鋅銀紐扣電池在工作過程中________(填物質名稱)被還原。
查看答案和解析>>
科目:高中化學 來源:2015-2016學年湖南省高一下期末化學試卷(解析版) 題型:填空題
在一定溫度下,發生如下反應:N2(g)+3H2(g)  2NH3(g),起始時,充入的N2和H2的物質的量分別是3.0 mol和6.0 mol,2min后反應達到平衡,平衡時NH3的物質的量與H2的物質的量相等,已知容器的容積為5.0 L且不可變,試回答下列問題:
2NH3(g),起始時,充入的N2和H2的物質的量分別是3.0 mol和6.0 mol,2min后反應達到平衡,平衡時NH3的物質的量與H2的物質的量相等,已知容器的容積為5.0 L且不可變,試回答下列問題:
(1) 其達到平衡狀態的標志是____________________。
①氨的生成速率與氨的分解速率相等
②斷開1個N≡N鍵的同時有6個N—H鍵生成
③N2、H2、NH3的體積分數不再變化
④氣體的總壓強不變
⑤N2、H2、NH3分子數之比為1:3:2
⑥N2、H2和NH3的濃度相等
⑦v(N2)=1/3v(H2)
⑧v正(N2)=1/3v逆(H2)
⑨混合物的密度不變
⑩混合物的平均相對分子質量不變
A.①③④⑤⑦⑩ B.①③④⑧⑩
C.①③④⑤⑧⑩ D.全部
(2)從反應開始到達到平衡用N2表示該反應的速率為: mol·L-1·min-1。
(3)平衡時H2的物質的量濃度為 mol·L-1。
(4)H2的轉化率是____________。
(5)平衡時混合氣體中NH3的體積分數是_______%(保留一位小數)。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com