
 下圖中的字母分別代表一種常見的物質或其溶液,相互之間的轉化關系如圖所示(部分產物及反應條件已略去).已知A、B為氣態單質,F是地殼中含量最多的金屬元素的單質;E、H、I為氧化物,E為黑色固體,I為紅棕色氣體;M為紅褐色沉淀.
下圖中的字母分別代表一種常見的物質或其溶液,相互之間的轉化關系如圖所示(部分產物及反應條件已略去).已知A、B為氣態單質,F是地殼中含量最多的金屬元素的單質;E、H、I為氧化物,E為黑色固體,I為紅棕色氣體;M為紅褐色沉淀. .
.分析 F是地殼中含量最多的金屬元素的單質,則F為Al;轉化關系中X電解得到三種物質,為電解電解質與水型,A、B為氣態單質,二者為氫氣和氯氣,二者反應生成D,D為HCl,E為黑色固體,為氧化物,和HCl反應又生成B氣體,A為H2,B為Cl2,E為MnO2,電解X是電解氯化鈉溶液,所以X為NaCl,C為NaOH,與Al反應生成G,G為NaAlO2;M為紅褐色沉淀為Fe(OH)3,所以J是含三價鐵離子的物質,是H和D反應生成,證明J為FeCl3,H、I為氧化物判斷H為Fe2O3,I為紅棕色氣體為NO2,結合轉化故選可知,N為HNO3,Y為Fe(NO3)3,結合物質的性質來解答.
解答 解:F是地殼中含量最多的金屬元素的單質,則F為Al;轉化關系中X電解得到三種物質,為電解電解質與水型,A、B為氣態單質,二者為氫氣和氯氣,二者反應生成D,D為HCl,E為黑色固體,為氧化物,和HCl反應又生成B氣體,A為H2,B為Cl2,E為MnO2,電解X是電解氯化鈉溶液,所以X為NaCl,C為NaOH,與Al反應生成G,G為NaAlO2;M為紅褐色沉淀為Fe(OH)3,所以J是含三價鐵離子的物質,是H和D反應生成,證明J為FeCl3,H、I為氧化物判斷H為Fe2O3,I為紅棕色氣體為NO2,結合轉化故選可知,N為HNO3,Y為Fe(NO3)3,
(1)B為Cl2中所含元素位于周期表第三周期第ⅦA族,故答案為:第三周期第ⅦA族;
(2)X為NaCl,NaCl的電子式為 ,
,
故答案為: ;
;
(3)J為FeCl3,檢驗J中陰離子即氯離子的常用試劑是HNO3、AgNO3,故答案為:HNO3、AgNO3;
(4)G(NaAlO2)+J(FeCl3)→M(Fe(OH)3)的反應是在水溶液中發生的雙水解反應,反應離子方程式是:3AlO2-+Fe3++6H2O=3Al(OH)3↓+Fe(OH)3↓,
故答案為:3AlO2-+Fe3++6H2O=3Al(OH)3↓+Fe(OH)3↓;
(5)依據分析推斷可知Y為Fe(NO3)3,受熱分解生成二氧化氮和氧化鐵,依據原子守恒配平書寫的化學方程式是:4Fe(NO3)3$\frac{\underline{\;\;△\;\;}}{\;}$2Fe2O3+12NO2↑+3O2↑,
故答案為:4Fe(NO3)3$\frac{\underline{\;\;△\;\;}}{\;}$2Fe2O3+12NO2↑+3O2↑.
點評 本題考查了物質轉化關系和物質性質的應用,主要考查離子方程式的書寫、鹽類水解的應用等,物質顏色與反應特點是解題關鍵,對學生的分析思維能力有較高的要求,題目難度中等.


科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 密閉容器中,9.6 g硫粉與11.2 g鐵粉混合加熱生成17.6 g硫化亞鐵時,放出19.12 kJ熱量.則Fe(s)+S(s)═FeS(s)△H=-95.6 kJ•mol-1 | |
| B. | 稀醋酸與0.1 mol•L-1 NaOH溶液反應:H+(aq)+OH-(aq)═H2O(l)△H=-57.3 kJ•mol-1 | |
| C. | 已知1 mol氫氣完全燃燒生成液態水所放出的熱量為285.5 kJ,則水分解的熱化學方程式為2H2O(l)═2H2(g)+O2(g)△H=+285.5 kJ•mol-1 | |
| D. | 已知2C(s)+O2(g)═2CO(g)△H=-221 kJ•mol-1,則可知C的燃燒熱△H=-110.5 kJ•mol-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 組成元素相同,組成元素的質量分數也對應相等的不同化合物,一定互為同分異構體 | |
| B. | 組成元素相同,相對分子質量相同的幾種化合物,互為同分異構體 | |
| C. | 摩爾質量相同,各元素質量分數也對應相等的不同化合物,一定是同分異構體 | |
| D. | 凡是分子組成相差一個或幾個CH2原子團的物質,彼此一定是同系物 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 制飯勺、高壓鍋等的不銹鋼是純鐵 | B. | 鋁制品可以長期用作餐具 | ||
| C. | Al(OH)3可用于制胃酸中和劑 | D. | 醫用酒精濃度是95% |
查看答案和解析>>
科目:高中化學 來源: 題型:推斷題
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
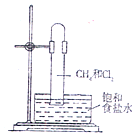 取一支硬質大試管,通過排飽和食鹽水的方法先后收集半試管甲烷和半試管氯氣(如圖),下列對于試管內發生的反應及現象的說法正確的是( )
取一支硬質大試管,通過排飽和食鹽水的方法先后收集半試管甲烷和半試管氯氣(如圖),下列對于試管內發生的反應及現象的說法正確的是( )| A. | 此反應無光照也可發生 | |
| B. | 甲烷和Cl2反應后的產物只有CH3Cl和HCl | |
| C. | 盛放飽和食鹽水的水槽底部會有少量晶體析出 | |
| D. | CH4和Cl2完全反應后液面上升,液體充滿試管 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com