
【題目】垃圾分類正在全國逐漸推廣,垃圾資源化是可持續、綠色發展的重要途徑。由金屬廢料(主要含鐵、銅和它們的氧化物)制得堿式碳酸銅和摩爾鹽[(NH4)2SO4·FeSO4·xH2O]的工藝流程如圖所示:

已知:Ksp[Fe(OH)3]=1×10-38,Ksp[Cu(OH)2]=2.2×10-20,一般認為某離子濃度小于或等于10-5mol/L時,該離子轉化或去除完全。
請回答下列問題:
(1)熱純堿的作用是__,H2O2的電子式為__。
(2)調pH步驟可選用的試劑為__。
A.CuO B.Cu(OH)2 C.Fe2O3 D.Fe(OH)3
(3)若所得溶液中c(Cu2+)=0.22mol·L-1,則需要調節的pH范圍是__。
(4)溶液1經過加熱、蒸發至__時,自然冷卻即可得到晶體,然后抽濾,用酒精洗滌晶體,酒精洗滌的目的是__。
(5)寫出該流程中生成堿式碳酸銅的離子方程式__。
(6)取3.92g摩爾鹽產品,在隔絕空氣的條件下加熱至135°C時完全失去結晶水,此時固體質量為2.84g,則該摩爾鹽結晶水個數x=__。
【答案】去除廢料表面的油污 ![]() AB 3~4.5 溶液表面出現晶膜(或溶液中出現晶體) 除去晶體表面水分 2Cu2++3CO32-+2H2O=Cu2(OH)2CO3↓+2HCO3-(或2Cu2++2CO32-+H2O=Cu2(OH)2CO3↓+CO2↑) 6
AB 3~4.5 溶液表面出現晶膜(或溶液中出現晶體) 除去晶體表面水分 2Cu2++3CO32-+2H2O=Cu2(OH)2CO3↓+2HCO3-(或2Cu2++2CO32-+H2O=Cu2(OH)2CO3↓+CO2↑) 6
【解析】
加入熱的純堿液,金屬廢料(主要含鐵、銅和它們的氧化物)中的主要成分都不發生反應,所以熱的純堿液的作用只能是去除油污;加入H2SO4、H2O2,鐵及氧化物溶解并轉化為Fe3+,銅及氧化物溶解生成Cu2+;調pH將Fe3+轉化為Fe(OH)3沉淀,用硫酸溶解生成硫酸鐵,再加入還原鐵粉轉化為硫酸亞鐵,加入硫酸銨最后得摩爾鹽。濾液中含有Cu2+,加入Na2CO3溶液發生雙水解反應生成Cu2(OH)2CO3。
(1)由以上分析可知,利用熱的純堿溶液水解使溶液呈較強的堿性,從而達到去除油污的目的,其作用是去除廢料表面的油污,H2O2為共價化合價,既存在O-H共價鍵,又存在O-O共價鍵,其電子式為![]() 。答案為:去除廢料表面的油污;
。答案為:去除廢料表面的油污;![]() ;
;
(2)調pH的目的,是將Fe3+轉化為Fe(OH)3沉淀,同時不引入新的雜質,可選擇CuO、Cu(OH)2,所以可選用的試劑為AB。答案為:AB;
(3) Ksp[Fe(OH)3]=1×10-38,c(Fe3+)=10-5mol/L,c(OH-)=10-11mol/L,pH=3;若所得溶液中c(Cu2+)=0.22mol·L-1,利用Ksp[Cu(OH)2]=2.2×10-20,可求得c(OH-)=![]() =
=![]() mol/L,pH=-lg(
mol/L,pH=-lg(![]() ×10-5)=4.5,則需要調節的pH范圍是3~4.5。答案為:3~4.5;
×10-5)=4.5,則需要調節的pH范圍是3~4.5。答案為:3~4.5;
(4)從溶液1中獲得摩爾鹽晶體,需經過加熱、蒸發至溶液表面出現晶膜(或溶液中出現晶體)時;自然冷卻即可得到晶體,然后抽濾,為防烘干時晶體失去結晶水,所以不能采用烘干的方法,而應用酒精洗滌晶體,酒精洗滌的目的是除去晶體表面水分。答案為:溶液表面出現晶膜(或溶液中出現晶體);除去晶體表面水分;
(5)該流程中Cu2+,加入Na2CO3溶液,利用部分離子發生雙水解反應生成Cu2(OH)2CO3,離子方程式為2Cu2++3CO32-+2H2O=Cu2(OH)2CO3↓+2HCO3-(或2Cu2++2CO32-+H2O=Cu2(OH)2CO3↓+CO2↑)。答案為:2Cu2++3CO32-+2H2O=Cu2(OH)2CO3↓+2HCO3-(或2Cu2++2CO32-+H2O=Cu2(OH)2CO3↓+CO2↑);
(6)m[(NH4)2SO4·FeSO4]= 2.84g,n[(NH4)2SO4·FeSO4]=![]() =0.01mol,m(H2O)= 3.92g-2.84g=1.08g,n(H2O)=
=0.01mol,m(H2O)= 3.92g-2.84g=1.08g,n(H2O)=![]() =0.06mol,則該摩爾鹽結晶水個數x=
=0.06mol,則該摩爾鹽結晶水個數x=![]() =6。答案為:6。
=6。答案為:6。


科目:高中化學 來源: 題型:
【題目】實驗室用濃硝酸氧化C2H2制取H2C2O4·2H2O的裝置如圖所示(電石主要成分為CaC2,含少量CaS雜質),下列說法正確的是( )
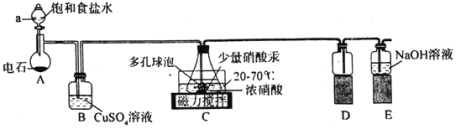
A.裝置A可作MnO2和濃鹽酸反應制備Cl2的發生裝置
B.裝置B的作用是除去C2H2中的H2S
C.裝置D的作用是收集草酸
D.裝置E中發生反應的離子方程式為3NO2+2OH-=2NO3-+NO+H2O
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】峨眉金頂攝身崖又稱舍身崖,因常現佛光而得名。“佛光”因攝入身之影像于其中,遂稱“攝身光”,為峨眉勝景之一。攝生崖下土壤中富含磷礦,所以在無月的黑夜可見到崖下熒光無數。
(1)“熒光”主要成分是 PH3(膦),其結構式為 __________ ,下列有關 PH3 的說法錯誤的是___________ 。
a.PH3 分子是極性分子
b.PH3 分子穩定性低于 NH3 分子,因為 N-H 鍵鍵能高
c.一個 PH3 分子中,P 原子核外有一對孤電子對
d.PH3 沸點低于 NH3 沸點,因為 P-H 鍵鍵能低
(2)PH3 的沸點比 NH3______填“高”或“低”) NH3 的水溶液堿性_____PH3 的水溶液堿性(填“大于”或“小于”);氯化鏻(PH4C1)與堿反應生成膦的離子方程式為 _______________________ 。
(3)PH3 是一種還原劑,其還原能力比 NH3 強,通常情況下能從Cu2+、Ag+、Hg2+等鹽溶液中還原出金屬, 而本身被氧化為最高氧化態。PH3 與 CuSO4 溶液反應的化學方程式為 ______________。
(4)“熒光”產生的原理是Ca3P2 在潮濕的空氣中劇烈反應,寫出該反應的化學方程式__________________。
(5)PH3 有毒,白磷工廠常用 Cu2+、Pd2+液相脫除 PH3:PH3+2O2![]() H3PO4,其他條件相同時, 溶解在溶液中O2 的體積分數與 PH3 的凈化效率與時間的關系如圖所示,回答下列問題:
H3PO4,其他條件相同時, 溶解在溶液中O2 的體積分數與 PH3 的凈化效率與時間的關系如圖所示,回答下列問題:
①由圖可知,富氧有利于______(選填“延長”或“縮短”)催化作用的持續時間。
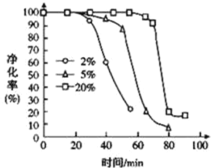
②隨著反應進行,PH3 的凈化效率急劇降低的原因可能為 _________________ 。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】電解法轉化CO2實現CO2資源化利用。電解CO2制甲酸鹽的裝置如圖所示。下列說法中正確的是( )
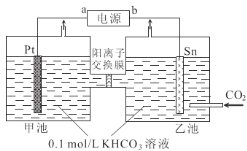
A.b是電源正極
B.K+由乙池向甲池遷移
C.甲池中KHCO3溶液濃度增大,乙池中KHCO3溶液濃度降低
D.乙池電極反應式為:CO2+HCO3-+2e-=HCOO-+CO32-
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某實驗小組用硫酸酸化的高錳酸鉀溶液與草酸溶液反應測定單位時間內生成CO2的量來探究影響反應速率的因素。設計實驗方案如表:
實驗序號 | A溶液 | B溶液 |
① | 20mL0.1mol·L-1H2C2O4溶液 | 30mL0.02mol·L-1酸性KMnO4溶液 |
② | 20mL0.2mol·L-1H2C2O4溶液 | 30mL0.02mol·L-1酸性KMnO4溶液 |
(1)圖1裝置中盛放A溶液的儀器名稱是_____,檢驗如圖1裝置氣密性的方法為_____。

(2)硫酸酸化的高錳酸鉀溶液與草酸溶液反應的化學反應方程式為_____。
(3)此實驗探究的是_____因素對化學反應速率的影響,若實驗②在40s末收集了22.4mLCO2(標準狀況下),則在40s內,v(MnO4-)=_____(忽略溶液混合前后體積的變化)。
(4)小組同學將圖1的氣體收集裝置改為圖2,實驗完畢冷卻后,讀數時發現量氣管液面高于干燥管液面,為得到準確數據,采取的操作是:____。
(5)除了通過測定單位時間內生成CO2的體積來比較反應速率,本實驗還可以通過測定____來比較化學反應速率。
(6)同學們在實驗中發現反應速率總是如圖3所示,探究t1~t2時間內速率變快的主要原因可能是:____。
A.該反應放熱 B.生成的Mn2+起催化作用 C.K2SO4濃度增大

查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】A、B、C均為短周期元素,它們在周期表中的位置如下圖所示。已知:B、C兩元素原子最外層電子數之和等于A元素原子最外層電子數的2倍;B.C兩元素的核電荷數之和是A元素原子序數的4倍。下列說法正確的是
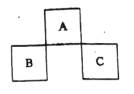
A.C位于元素周期表中第3周期第VA族
B.B的非金屬性比A強
C.C的氣態氫化物的穩定性比B的強
D.原子半徑:r(B)<r(C)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列有關說法正確的是
A.MgO(s)+C(s)=CO(g)+Mg(g)高溫下能自發進行,則該反應ΔH>0、ΔS>0
B.常溫下等物質的量濃度的CH3COOH溶液和HCl溶液中,水的電離程度相同
C.0.1 mol·L-1 NH4Cl溶液加水稀釋,![]() 的值增大
的值增大
D.對于反應2SO2+O22SO3,使用催化劑能加快反應速率并提高SO2的平衡轉化率
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】硼鐵混合精礦含有硼鎂石[MgBO2(OH)、磁鐵礦(Fe3O4)、磁黃鐵礦(FexS)、品質鈾礦(UO2)等,以該礦為原料制備MgSO4·H2O和硼酸(H3BO3)的工藝流程如下:
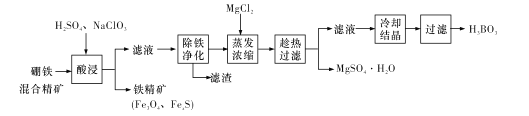
已知:![]() 在pH為4~5的溶液中生成UO2(OH)2沉淀。
在pH為4~5的溶液中生成UO2(OH)2沉淀。
回答下列問題:
(l)“酸浸”時,為了提高浸出率可采取的措施有:________ (至少答兩個措施),該步驟中NaC1O3可將UO2轉化為![]() ,則該反應的離子方程式為_____。
,則該反應的離子方程式為_____。
(2)“除鐵凈化”需要加入____(填化學式)把溶液pH調節至4~5,濾渣的成分是_______。
(3)“蒸發濃縮”時,加入固體MgC12的作用是 ___。
(4)鐵精礦(Fe3O4、FexS)經過一系列加工后,可用于制備氫氧化鐵固體。已知T℃,
![]() ,
,![]() ,
,![]() 回答下列問題:
回答下列問題:
①在T℃,假設Fe3+水解的離子方程式是:![]() ,則該條件下Fe3+水解反應的平衡常數K= __(用含以的字母表示)。
,則該條件下Fe3+水解反應的平衡常數K= __(用含以的字母表示)。
②在T℃向飽和Fe(OH)3、Fe(OH)2的混合溶液中,加入少量NaOH固體(忽略溶液體積變化),則溶液中的c(Fe2+)/c(Fe3+)會 __(填“變大”“變小”或“不變”),請結合相關數據推理說明:____。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】根據原電池的知識,下列反應可設計成原電池的是( )
A.CH3CH2OH+3O2![]() 2CO2+3H2O
2CO2+3H2O
B.Ba(OH)28H2O+2NH4Cl=BaCl2+2NH3↑+10H2O
C.H2SO4+2NaOH=Na2SO4+2H2O
D.CaO+H2O=Ca(OH)2
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com