
| A. | 氣態氫化物的穩定性:X>Y | |
| B. | 最高價氧化物對應的水化物的酸性:Y>X>W | |
| C. | Q可分別與X、Y、Z、W形成化學鍵類型相同的化合物 | |
| D. | Y的簡單離子半徑小于Z的簡單離子半徑 |
分析 短周期元素X、Y、Z、W、Q的原子序數依次增大,Z元素原子半徑在短周期中最大(稀有氣體除外),則Z為Na;Z、W、Q同周期,只有一種金屬元素,故W、Q最外層電子數都大于3,W、Z之間與W、Q之間原子序數之差相等,則W最外層電子數為4,Q最外層電子數為7,可推知W為Si、Q為Cl;X與W處于同一主族,則X為C元素;五種元素原子最外層電子數之和為21,則Y的最外層電子數=21-4-4-1-7=5,原子序數小于Na,故Y為N元素,據此解答.
解答 解:短周期元素X、Y、Z、W、Q的原子序數依次增大,Z元素原子半徑在短周期中最大(稀有氣體除外),則Z為Na;Z、W、Q同周期,只有一種金屬元素,故W、Q最外層電子數都大于3,W、Z之間與W、Q之間原子序數之差相等,則W最外層電子數為4,Q最外層電子數為7,可推知W為Si、Q為Cl;X與W處于同一主族,則X為C元素;五種元素原子最外層電子數之和為21,則Y的最外層電子數=21-4-4-1-7=5,原子序數小于Na,故Y為N元素,
A.元素的非金屬性越強,其氫化物越穩定,非金屬性:Y>X,則氣態氫化物的穩定性:Y>X,故A錯誤;
B.元素的非金屬性越強,最高價氧化物對應的水化物的酸性越強,則最高價氧化物對應的水化物的酸性:Y>X>W,故B正確;
C.Cl分別與C、N、Si形成的化合物含有共價鍵,與Na形成的NaCl含有離子鍵,化學鍵類型不相同,故C錯誤;
D.電子排布相同的離子,原子序數越大,離子半徑越小,所以N的簡單離子半徑大于Na的簡單離子半徑,故D錯誤;
故選B.
點評 本題考查結構性質位置關系應用,推斷元素是解題關鍵,注意充分利用非金屬元素最外層電子特點及W、Z之間與W、Q之間原子序數之差相等進行推斷,難度中等,側重于考查學生的分析能力.


 應用題作業本系列答案
應用題作業本系列答案科目:高中化學 來源: 題型:選擇題
| A. | 2-甲基-2-丁烯 | B. | 2,3-二甲基-1-丙烯 | ||
| C. | 3-甲基-1-丁烯 | D. | 2-甲基-1,3-丁二烯 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | NCl3分子是非極性分子 | |
| B. | 分子中的所有原于均達到8電子穩定結構 | |
| C. | NBr3的熔點比NCl3的熔點低 | |
| D. | 分子中N-C1鍵鍵長比CCl4分子中C-C1鍵鍵長長 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
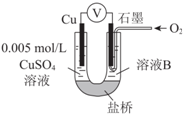 某小組同學利用原電池裝置探究物質的性質.
某小組同學利用原電池裝置探究物質的性質.| 裝置 | 編號 | 電極A | 溶液B | 操作及現象 |
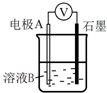 | Ⅰ | Fe | pH=2的 H2SO4 | 連接裝置后,石墨表面產生無色氣泡;電壓表指針偏轉 |
| Ⅱ | Cu | pH=2的H2SO4 | 連接裝置后,石墨表面無明顯現象;電壓表指針偏轉,記錄讀數為a |
| 編號 | 溶液B | 操作及現象 |
| Ⅲ | 經煮沸的pH=2的 H2SO4 | 溶液表面用煤油覆蓋,連接裝置后,電壓表指針微微偏轉,記錄讀數為b |
| Ⅳ | pH=2的H2SO4 | 在石墨一側緩慢通入O2并連接裝置,電壓表指針偏轉,記錄讀數為c;取出電極,向溶液中加入數滴濃Na2SO4溶液混合后,插入電極,保持O2通入,電壓表讀數仍為c |
| Ⅴ | pH=12的NaOH | 在石墨一側緩慢通入O2并連接裝置,電壓表指針偏轉,記錄讀數為d |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 苯酚和乙酸都能與NaOH溶液反應 | |
| B. | 甲酸可發生銀鏡反應,而乙酸不能 | |
| C. | 苯酚能與氫氧化鈉溶液反應 而乙醇不行 | |
| D. | 乙烯可發生加成反應,而乙烷不能 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | c(SO3)=0.15mol•L-1 | B. | c(SO3)=c(SO2)=0.075 mol•L-1 | ||
| C. | c(SO3)=0.2 mol•L-1 | D. | c(O2)=0.05 mol•L-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
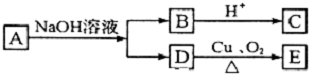
| A. | 5種 | B. | 4種 | C. | 3種 | D. | 2種 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 簡單離子半徑:Y>X>W | B. | 單質的氧化性:W>Y>Z | ||
| C. | 化合物ZW2具有強還原性 | D. | 化合物Y2Z2中只含共價鍵 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com