
【題目】將1 mL 0.10 mol/L 硫酸加水稀釋成 2 L 溶液,則溶液中由水電離產生的H+ 的濃度為( )
A.1×10-10 mol/L
B.1×10-8 mol/L
C.1×10-11 mol/L
D.1×10-4 mol/L
 能力評價系列答案
能力評價系列答案 唐印文化課時測評系列答案
唐印文化課時測評系列答案科目:高中化學 來源: 題型:
【題目】恒溫、恒容的條件下對于N2(g)+3H2(g) ![]() 2NH3(g) ΔH<0的反應,達到化學平衡狀態的標志為
2NH3(g) ΔH<0的反應,達到化學平衡狀態的標志為
A.斷開一個N≡N鍵的同時有6個N—H鍵生成
B.混合氣體的密度不變
C.混合氣體的平均相對分子質量不變
D.N2、H2、NH3分子數之比為1∶3∶2的狀態
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】2019年10月9日消息,諾貝爾化學獎頒給約翰●B.古迪納夫、M●斯坦利●威廷漢和吉野彰,以表彰他們“開發鋰離子電池”的貢獻。磷酸亞鐵鋰(化學式:LiFePO4)是鋰離子電池電極材料,主要用于動力鋰離子電池,作為正極活性物質使用,人們習慣也稱其為磷酸鐵鋰。
(1)基態鋰原子核外能量最高的電子電子云輪廓圖形狀為__;基態磷原子第一電離能比基態硫的__(填“大”或“小”),原因是__。
(2)實驗室中可用KSCN或K4[Fe(CN)6]來檢驗Fe3+。FeCl3與KSCN溶液混合,可得到配位數為5的配合物的化學式是__,其中硫、碳的雜化類型分別是__、__。
(3)磷酸和亞磷酸(H3PO3)是磷元素的兩種含氧酸。PO43-的空間構型為__;亞磷酸與NaOH反應只生成Na2HPO3和NaH2PO3兩種鹽,則H3PO3的結構式為__。
(4)磷酸分子間脫水可生成多磷酸,其某一鈣鹽的結構如圖所示:
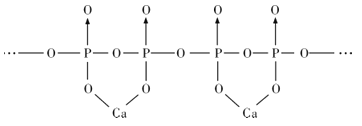
由圖推知該多磷酸鈣鹽的通式為__。
(5)氧化亞鐵晶體的晶胞如圖所示。已知:氧化亞鐵晶體的密度為ρg·cm-3,NA代表阿伏加德羅常數的值。在該晶胞中,與O2-緊鄰且等距離的Fe2+數目為__,Fe2+與O2-最短核間距為___pm。
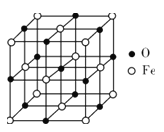
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】25℃時,向0.1mol/LCH3COOH溶液中逐漸加入NaOH固體,恢復至原溫度后溶液中的關系如圖所示(忽略溶液體積變化)。下列有關敘述不正確的是( )

A.CH3COOH的Ka=1.0×10-4.7
B.C點的溶液中:c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
C.B點的溶液中:c(Na+)+c(H+)=c(CH3COOH)+c(OH-)
D.A點的溶液中:c(CH3COO-)+c(H+)+c(CH3COOH)-c(OH-)=0.1mol/L
查看答案和解析>>
科目:高中化學 來源: 題型:
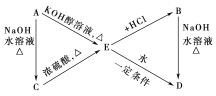
【題目】已知:R—CH=CH2+HX→![]() (主要產物)。下列轉化中A、B分別是分子式為C3H7Cl的兩種同分異構體,請根據轉化關系和反應條件,判斷并寫出:
(主要產物)。下列轉化中A、B分別是分子式為C3H7Cl的兩種同分異構體,請根據轉化關系和反應條件,判斷并寫出:
(1)A、B、C、D、E的結構簡式____、____、____、____、____。
(2)由E轉化為B、由A轉化為E的化學方程式____、____。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知: (1)Fe2O3(s)+![]() C(s)=
C(s)=![]() CO2(g)+2Fe(s),ΔH=+234.1kJmol-1
CO2(g)+2Fe(s),ΔH=+234.1kJmol-1
![]() 則
則![]() 的ΔH是( )
的ΔH是( )
A.-824.4 kJmol-1B.-627.6kJmol-1C.-744.7kJmol-1D.-169.4kJmol-1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】室溫下,用0.10 mol·L-1KOH溶液滴定10.00 mL 0.10 mol·L-1H2C2O4(二元弱酸)溶液所得滴定曲線如圖(混合溶液的體積可看成混合前溶液的體積之和)。請回答下列問題:
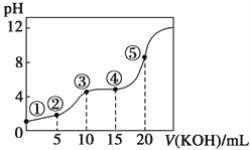
(1)點①所示溶液中,Kw=__________。
(2)點②所示溶液中的電荷守恒式為______________________________________。
(3)點③所示溶液中存在________種平衡。
(4)點④所示溶液中的物料守恒式為0.10 mol·L-1=___________________________。
(5)點⑤所示溶液中各離子濃度的大小順序為________________________________。
(6)上述5點所示溶液中,水的電離程度最大的是_______,最小的是________(用序號回答)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列選項中的原因或結論與現象不對應的是( )
選項 | 現象 | 原因或結論 |
A | 在H2O2中加入MnO2,能加速H2O2的分解速率 | MnO2降低了反應所需的活化能 |
B | 向5mL 0.005mol·L-1FeCl3溶液中加入5mL0.010mol·L-1KSCN溶液,溶液呈紅色,再滴加1ml1 mol·L-1KCl溶液,溶液顏色變淺 | 增大生成物濃度,平衡向逆反應方向移動 |
C | 將盛有NO2氣體的密閉容器浸泡在熱水中,容器內氣體顏色變深 | 2NO2(g) |
D | 在密閉容器中有反應:A+xB(g) | 若A為氣體、x>1 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】![]() 使
使![]() 和
和![]() 通過灼熱的炭層,生成HCl和
通過灼熱的炭層,生成HCl和![]() ,當有
,當有![]() 參與反應時釋放出145kJ熱量,寫出該反應的熱化學方程式________________.
參與反應時釋放出145kJ熱量,寫出該反應的熱化學方程式________________.
![]() 火箭和導彈表面的薄層是耐高溫物質
火箭和導彈表面的薄層是耐高溫物質![]() 將石墨、鋁粉和二氧化鈦按一定比例混合在高溫下煅燒,所得物質可作耐高溫材料
將石墨、鋁粉和二氧化鈦按一定比例混合在高溫下煅燒,所得物質可作耐高溫材料![]() ,則反應過程中,每轉移1mol電子放出的熱量為____________.
,則反應過程中,每轉移1mol電子放出的熱量為____________.
![]() 甲胺
甲胺![]() 是合成太陽能敏化劑的原料。工業合成甲胺原理:
是合成太陽能敏化劑的原料。工業合成甲胺原理:![]()
![]()
![]() 。
。
![]() 已知鍵能指斷開1mol氣態鍵所吸收的能量或形成1mol氣態鍵所釋放的能量。幾種化學鍵的鍵能如下表所示:
已知鍵能指斷開1mol氣態鍵所吸收的能量或形成1mol氣態鍵所釋放的能量。幾種化學鍵的鍵能如下表所示:
化學鍵 |
|
|
|
|
|
鍵能 | 413 | 351 | 463 | 393 | 293 |
則該合成反應的![]() ______________。
______________。
若![]() 的活化能為
的活化能為![]() ,由此計算
,由此計算![]()
![]() 的活化能
的活化能![]() ______。
______。
![]() 用
用![]() 將HCl轉化為
將HCl轉化為![]() ,可提高效益,減少污染,傳統上該轉化通過如圖所示的催化劑循環實現,
,可提高效益,減少污染,傳統上該轉化通過如圖所示的催化劑循環實現,
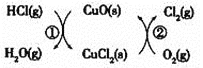
其中,反應![]() 為:
為:![]() 反應
反應![]() 生成
生成![]() 的反應熱為
的反應熱為![]() ,則總反應的熱化學方程式為_____________,
,則總反應的熱化學方程式為_____________,![]() 反應熱用
反應熱用![]() 和
和![]() 表示
表示![]() .
.
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com