
【題目】有下列八種基團:①苯基、②醛基、③羥基、④羧基、⑤乙基、⑥氯原子(-Cl),⑦硝基等基團兩兩結合,可形成化合物,寫出符合下列條件的化合物。
(1)分子內氧原子數不超過2個,具有酸性,但不能和碳酸氫鈉反應_______________
(2)分子內只含1個氧原子,能發生銀鏡反應的物質,除苯甲醛和甲酰氯(Cl-CHO)外還有(寫名稱)__________,寫出這種有機物發生銀鏡反應的化學方程式_________
(3)分子內只含1個氧原子,不能跟氫氧化鈉反應、但能夠發生酯化反應的有機物(寫名稱)________,寫出這種有機物跟另一種相對分子質量相等有機物發生酯化反應的化學方程式______________.
【答案】![]() ,HClO 丙醛 CH3CH2CHO+2Ag(NH3)2OH
,HClO 丙醛 CH3CH2CHO+2Ag(NH3)2OH![]() CH3CH2COONH4+2Ag↓+3NH3+H2O 乙醇 HCOOH+CH3CH2OH
CH3CH2COONH4+2Ag↓+3NH3+H2O 乙醇 HCOOH+CH3CH2OH![]() HCOOCH2CH3+H2O
HCOOCH2CH3+H2O
【解析】
(1)不能和碳酸氫鈉反應,說明不含有—COOH,且酸性比碳酸弱;
(2)能發生銀鏡反應,說明含有—CHO;
(3)分子內只含1個氧原子,能夠發生酯化反應、不能跟氫氧化鈉反應說明含醇羥基。
(1)分子內氧原子數不超過2個,不能和碳酸氫鈉反應,說明不含有—COOH,且酸性比碳酸弱,符合條件的有①③結合生成苯酚,③⑥結合為次氯酸,結構簡式分別為![]() 、HClO;
、HClO;
(2)能發生銀鏡反應,說明含有—CHO,分子內只含1個氧原子,除苯甲醛和甲酰氯(Cl-CHO)外,還有②⑤結合生成丙醛,丙醛發生銀鏡反應的化學方程式為CH3CH2CHO+2Ag(NH3)2OH![]() CH3CH2COONH4+2Ag↓+3NH3+H2O;
CH3CH2COONH4+2Ag↓+3NH3+H2O;
(3)分子內只含1個氧原子,能夠發生酯化反應、不能跟氫氧化鈉反應說明含醇羥基,符合條件的是③⑤結合成乙醇,和乙醇相對分子質量相等且能與乙醇發生酯化反應的物質為甲酸,發生的酯化反應的方程式為HCOOH+CH3CH2OH![]() HCOOCH2CH3+H2O。
HCOOCH2CH3+H2O。


 新課標快樂提優暑假作業陜西旅游出版社系列答案
新課標快樂提優暑假作業陜西旅游出版社系列答案 暑假銜接培優教材浙江工商大學出版社系列答案
暑假銜接培優教材浙江工商大學出版社系列答案科目:高中化學 來源: 題型:
【題目】某化學興趣小組對加碘食鹽中的KIO3進行研究,它是一種白色粉末,常溫下很穩定。在酸性條件下KIO3是一種較強的氧化劑,與HI、H2O2等作用,被還原為碘單質。 學生甲設計實驗測出加碘食鹽中碘元素的含量,步驟如下:
a.稱取mg加碘鹽,加適量蒸餾水溶解;
b.用稀硫酸酸化,再加入過量KI溶液;發生反應:IO3﹣+5I﹣+6H+=3I2+3H2O,將反應后的溶液加水稀釋至100.00 mL。
c.取10.00mL上述溶液到錐形瓶中,以淀粉為指示劑,用物質的量濃度為3.0molL﹣1的 Na2S2O3溶液滴定(滴定時的反應方程式:I2+2S2O32﹣═2I﹣+S4O62﹣)。
d.重復實驗2次,三次實驗分別記錄有關數據如下:
滴定次數 | 待測溶液的體積/mL | 1.00×10﹣3molL﹣1的 Na2S2O3溶液的體積(mL) | |
滴定前刻度 | 滴定后刻度 | ||
第一次 | 10.00 | 2.62 | 22.60 |
第二次 | 10.00 | 7.56 | 30.30 |
第三次 | 10.00 | 6.22 | 26.24 |
試回答:
(1)如下圖,是某次滴定時的滴定管中的液面,其讀數為___________mL。
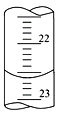
(2)判斷到達滴定終點的現象是:_______________________。
(3)滴定時,Na2S2O3溶液應放在______________ (填“酸式滴定管”或“堿式滴定管”)。
(4)根據實驗測定數據,計算加碘食鹽樣品中的碘元素百分含量是_______(以含m的代數式表示)。
(5)根據上述實驗對下列假定情況進行討論,導致測出待測液的濃度是(填“偏小”、“偏大”或“無影響”)
①標準液讀數時,若滴定前俯視,滴定后仰視,測出待測液的濃度__________
②盛標準液的滴定管,滴定前滴定管尖端有氣泡,滴定后氣泡消失,測出待測液的濃度___
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列有關平衡常數的說法中,正確的是 ( )
A. 改變條件,反應物的轉化率增大,平衡常數也一定增大
B. 反應2NO2(g)![]() N2O4(g) △H <0,升高溫度該反應平衡常數增大
N2O4(g) △H <0,升高溫度該反應平衡常數增大
C. 對于給定可逆反應,溫度一定時,其正、逆反應的平衡常數相等
D. CO2+H2 ![]() CO+H2O的平衡常數表達式為K==
CO+H2O的平衡常數表達式為K==![]()
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)已知SO2(g)+ 1/2 O2(g) ![]() SO3(g) △H = -98.30kJ/mol,現將4molSO2與一定量O2混合后充分反應,當放出314.56kJ熱量時,SO2的轉化率為_________________。
SO3(g) △H = -98.30kJ/mol,現將4molSO2與一定量O2混合后充分反應,當放出314.56kJ熱量時,SO2的轉化率為_________________。
(2)蓋斯定律在生產和科學研究中有很重要的意義。有些反應的反應熱雖然無法直接測得,但可通過間接的方法測定。現根據下列3個熱化學反應方程式:
Fe2O3(s)+3CO(g)= 2Fe(s)+3CO2(g) △H= ―24.8kJ/mol
3Fe2O3(s)+ CO(g)=2Fe3O4(s)+ CO2(g) △H= ―47.2kJ/mol
Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) △H= +640.5kJ/mol
寫出CO氣體還原FeO固體得到Fe固體和CO2氣體的熱化學反應方程式:_____________________________
(3)在一定條件下,CH4 和CO的燃燒的熱化學方程式分別為:
CH4 ( g ) + 2O2 ( g ) = 2H2O ( l ) + CO2 ( g ) △H = -890 kJ/mol
2CO ( g ) + O2 ( g ) = 2CO2 ( g ) △H = -566 kJ/mol
一定量的CH4和CO的混合氣體完全燃燒時,放出的熱量為262.9 kJ,生成的CO2用過量的飽和石灰水完全吸收,可得到50 g白色沉淀。求混合氣體中CH4 和CO的體積比_____________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】銨明礬[NH4Al(SO4)2·12H2O]是分析化學常用基準試劑,其制備過程如下。下列分析不正確的是( )

A.過程Ⅰ反應:2NH4HCO3+Na2SO4=2NaHCO3↓+(NH4)2SO4
B.檢驗溶液B中陰離子的試劑僅需BaCl2溶液
C.若省略過程Ⅱ,則銨明礬產率明顯減小
D.向銨明礬溶液中逐滴加入NaOH溶液并加熱,先后觀察到:刺激性氣體逸出→白色沉淀生成→白色沉淀消失
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】正丁醚常用作有機反應的溶劑。實驗室制備正丁醚的反應和主要實驗裝置如下:2CH3CH2CH2CH2OH![]() (CH3CH2CH2CH2)2O+H2O,反應物和產物的相關數據如下表:
(CH3CH2CH2CH2)2O+H2O,反應物和產物的相關數據如下表:
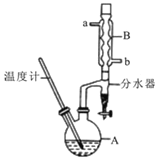

①將6 mL濃硫酸和37 g正丁醇,按一定順序添加到A中,并加幾粒沸石。
②加熱A中反應液,迅速升溫至135℃,維持反應一段時間。
③分離提純:待A中液體冷卻后將其緩慢倒入盛有70 mL水的溫度分液漏斗中,振搖后靜置,分液得粗產物。
④粗產物依次用40 mL水、20 mL NaOH溶液和40 mL水洗滌,分液后加入約3g無水氯化鈣顆粒,靜置一段時間后棄去氯化鈣。
⑤將上述處理過的粗產物進行蒸餾,收集餾分,得純凈正丁醚11g。請回答:
(1)步驟①中濃硫酸和正丁醇的添加順序為:應先加 。
(2)加熱A前,需先從 (填“a”或“b”)口向B中通入水。
(3)步驟③的目的是初步洗去 ,振搖后靜置,粗產物應 (填“上”或“下”)口倒出。
(4)步驟⑤中,加熱蒸餾時應收集 (填選項字母)左右的餾分。
A.100℃ B.117℃ C.135℃ D.142℃
(5)反應過程中會觀察到分水器中收集到液體物質,且分為上下兩層,隨著反應的進行,分水器中液體逐漸增多至充滿時,上層液體會從左側支管自動流回A。分水器中上層液體的主要成分為 ,下層液體的主要成分為 。
(6)本實驗中,正丁醚的產率為 (精確到1%)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一氯化碘![]() 是一種重要的鹵素互化物,在化工生產中有廣泛應用。有關一氯化碘的部分信息如下:
是一種重要的鹵素互化物,在化工生產中有廣泛應用。有關一氯化碘的部分信息如下:

某小組擬設計實驗制備一氯化碘并測定其純度,裝置如圖所示。

按如圖所示裝置進行實驗,當D裝置中產生紅棕色液體、固體消失時停止反應。
請回答下列問題:
(1)盛裝碘單質的儀器名稱是_____________;E裝置作用是_____________。
(2)![]() 裝置中試劑名稱是______________________________。
裝置中試劑名稱是______________________________。
(3)寫出A中反應的離子方程式______________________。
(4)啟動反應后,將D裝置的儀器放置于冷水浴中,其目的是__________________。
(5)粗產品中混有碘單質,提純產品可選擇下列裝置中的_____________![]() 填字母
填字母![]() 。
。

(6)測定產品純度。取![]() 該產品于錐形瓶,加入過量的KI溶液,充分反應。用
該產品于錐形瓶,加入過量的KI溶液,充分反應。用![]() 溶液滴定
溶液滴定![]() 有關反應:
有關反應:![]() ,
,![]() ,三次平行實驗測得數據如下:
,三次平行實驗測得數據如下:
![]()
該產品純度為___________![]() 用含a和c的代數式表示
用含a和c的代數式表示![]() ;若產品中混有少量
;若產品中混有少量![]() ,測得結果_______________
,測得結果_______________![]() 填“偏高”“偏低”或“無影響”
填“偏高”“偏低”或“無影響”![]() 。
。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】次磷酸鈉![]() 是有機合成的常用還原劑,一般制備方法是將黃磷
是有機合成的常用還原劑,一般制備方法是將黃磷![]() 和過量燒堿溶液混合、加熱,生成次磷酸鈉和
和過量燒堿溶液混合、加熱,生成次磷酸鈉和![]() 。
。![]() 是一種無色、有毒的可燃性氣體。實驗裝置如圖所示:
是一種無色、有毒的可燃性氣體。實驗裝置如圖所示:
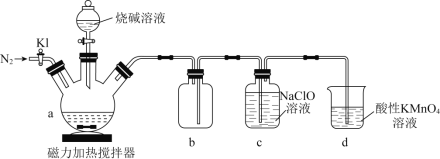
回答下列問題:
(1)在a中加入黃磷、活性炭粉末,打開![]() ,通入
,通入![]() 一段時間,關閉
一段時間,關閉![]() ,打開磁力加熱攪拌器,滴加燒堿溶液。
,打開磁力加熱攪拌器,滴加燒堿溶液。
①活性炭粉末作為黃磷的分散劑,原理是_______;b的作用______________。
②![]() 中反應的化學方程式為_______________________________。
中反應的化學方程式為_______________________________。
(2)反應結束后,打開![]() ,繼續通入
,繼續通入![]() ,目的是______________________________。d的作用是__________________。
,目的是______________________________。d的作用是__________________。
(3)![]() 中生成
中生成![]() 和NaCl,相關物質溶解度
和NaCl,相關物質溶解度![]() 如下:
如下:
|
| |
NaCl | 37 | 39 |
| 100 | 667 |
充分反應后,將c中混合液蒸發濃縮,有大量晶體析出,該晶體主要成分的化學式為_____________,然后________________、______________、過濾、洗滌、干燥,得到含![]() 的粗產品。
的粗產品。
(4)產品純度測定:
取產品m克配成![]() 溶液,取25mL于錐形瓶中,酸化后加入
溶液,取25mL于錐形瓶中,酸化后加入![]() 碘水,于暗處充分反應后,以淀粉溶液做指示劑,用
碘水,于暗處充分反應后,以淀粉溶液做指示劑,用![]() 溶液滴定至終點,平均消耗VmL。相關反應方程式為:
溶液滴定至終點,平均消耗VmL。相關反應方程式為:![]() ,
,![]() 。產品純度表達式為________________。
。產品純度表達式為________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】由下列“實驗操作和現象”與“結論”均正確的( )
選項 | 實驗操作及現象 | 結論 |
A | 將含鐵的氧化物的磚塊用鹽酸浸取,浸取液能使KMnO4溶液褪色 | 浸取液中含Fe2+ |
B | 常溫下,測得飽和Na2CO3 溶液的pH大于飽和NaHCO3 溶液的pH | 常溫下水解程度 |
C | 25℃時,向AgNO3溶液中滴加足量NaCl溶液至不再產生沉淀,然后滴加KI溶液,有黃色沉淀生成 | 25℃時,Ksp(AgCl)>Ksp(AgI) |
D | 將Cl2通入滴有酚酞的NaOH溶液后,溶液褪色 | Cl2具有漂白性 |
A.AB.BC.CD.D
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com