
【題目】化合物H是合成巴比妥類鎮靜藥物的中間體,一種以丙烯為原料合成H的路線如下:
![]()
已知:①A、B、C均可發生銀鏡反應。
②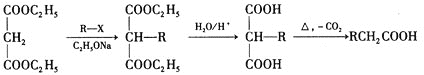
請回答下列問題:
(1)A的化學名稱是___,B中官能團的名稱是___。
(2)由C生成D中反應i的化學方程式為___。
(3)E的結構簡式為___,由E生成F的反應類型是___。
(4)與H互為同分異構體且與C互為同系物的有機物有___種,其中核磁共振氫譜有3組峰的結構簡式為___(任寫一種)。
(5)設計由乙烯、乙醇鈉和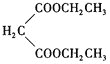 為原料制備2-乙基丁酸的合成路線
為原料制備2-乙基丁酸的合成路線![]() 無機試劑任選
無機試劑任選![]() ___。
___。
【答案】丙烯醛 醛基、羥基 OHC-CH2-CHO+4Ag(NH3)2OH![]() H4NOOC-CH2-COONH4+4Ag↓+6NH3+2H2O
H4NOOC-CH2-COONH4+4Ag↓+6NH3+2H2O 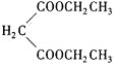 取代反應 9 OHC(CH2)4CHO或
取代反應 9 OHC(CH2)4CHO或![]()
【解析】
丙烯被氧化為A,A分子式是C3H4O,可發生銀鏡反應,所以A是CH2=CH-CHO;CH2=CH-CHO與水發生反應生成B, B相對分子質量是74,B可發生銀鏡反應,能發生催化氧化生成C,C發生銀鏡反應生成D,D 與乙醇反應生成E,E分子中含有7個碳原子,所以D分子中含有2個羧基,逆推可知D是HOOCCH2CHOOH、C是OHCCH2CHO,B是HOCH2CH2CHO;E是C2H5OOCCH2COOC2H5,C2H5OOCCH2COOC2H5與![]() 發生取代反應生成
發生取代反應生成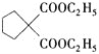 ;
; 水解為G,G是
水解為G,G是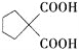 ,
, 脫掉1個CO2生成H,H是
脫掉1個CO2生成H,H是![]() 。
。
根據以上分析, ![]() 為
為![]() ,名稱是丙烯醛;B為
,名稱是丙烯醛;B為![]() ,官能團的名稱為羥基和醛基;
,官能團的名稱為羥基和醛基;
![]() 為
為![]() ,D為
,D為![]() ,由C生成D中反應i的化學方程式為OHC-CH2-CHO+4Ag(NH3)2OH
,由C生成D中反應i的化學方程式為OHC-CH2-CHO+4Ag(NH3)2OH![]() H4NOOC-CH2-COONH4+4Ag↓+6NH3+2H2O;
H4NOOC-CH2-COONH4+4Ag↓+6NH3+2H2O;
![]() 的結構簡式為
的結構簡式為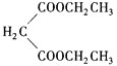 ,由E生成F可視為E分子“
,由E生成F可視為E分子“![]() ”中的兩個H與
”中的兩個H與![]() 中的溴原子發生取代反應生成
中的溴原子發生取代反應生成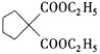 和HBr,反應類型是取代反應;
和HBr,反應類型是取代反應;
![]() 的分子式為
的分子式為![]() ,C為
,C為![]() ,故與H互為同分異構體且與C互為同系物的有機物含有2個醛基。若剩余4個碳原子的連接方式為
,故與H互為同分異構體且與C互為同系物的有機物含有2個醛基。若剩余4個碳原子的連接方式為![]() ,2個醛基連接在
,2個醛基連接在![]() 上的結構有6種,若剩余4個碳原子的連接方式為
上的結構有6種,若剩余4個碳原子的連接方式為![]() ,2個醛基連接在
,2個醛基連接在![]() 上的結構有3種,共9種,其中核磁共振氫譜有3組峰的結構簡式為
上的結構有3種,共9種,其中核磁共振氫譜有3組峰的結構簡式為![]() 或
或![]() ;
;
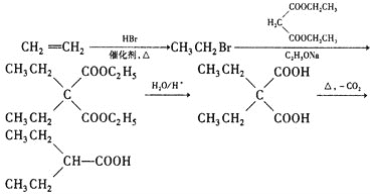
![]() 乙烯與溴化氫發生加成反應生成溴乙烷,溴乙烷與
乙烯與溴化氫發生加成反應生成溴乙烷,溴乙烷與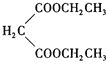 發生取代反應生成
發生取代反應生成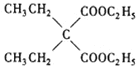 ,
, 在酸性條件下水解為
在酸性條件下水解為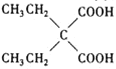 ,
, 在加熱條件下脫掉1分子CO2生成
在加熱條件下脫掉1分子CO2生成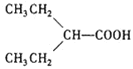 ,合成路線為
,合成路線為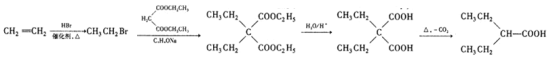 。
。


 心算口算巧算一課一練系列答案
心算口算巧算一課一練系列答案科目:高中化學 來源: 題型:
【題目】某氣態烴0.5mol能與0.5molCl2完全加成,加成產物又可被3molCl2完全取代,則此氣態烴可能是
A.CH2=CH2B.CH3-CH=CH2
C.CH2=CHCH2CH3D.CH2=CH-CH=CH2
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】向足量稀硫酸(不考慮反應過程中硫酸濃度的變化)中加入一定量的鋅粒,同時不斷向其中滴加硫酸銅溶液,觀察到生成氫氣的速率如圖所示。下列有關說法錯誤的是( )
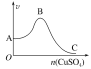
A.AB段速率的變化可能是因為溶液溫度逐漸升高
B.AB段速率的變化可能是因為形成了銅鋅原電池
C.BC段速率的變化可能是因為溶液溫度逐漸降低
D.BC段速率變化的原因主要是置換出的銅太多,覆蓋在鋅粒表面,阻礙了反應的進行
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】為落實“五水共治”,某工廠擬綜合處理含NH4+廢水和工業廢氣(主要含N2、CO2、SO2、NO、CO,不考慮其他成分),設計了如下流程:
下列說法不正確的是

A. 固體1中主要含有Ca(OH)2、CaCO3、CaSO3
B. X可以是空氣,且需過量
C. 捕獲劑所捕獲的氣體主要是CO
D. 處理含NH4+廢水時,發生反應的離子方程式為:NH4++NO2-==N2↑+2H2O
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某溫度時,N2與H2反應過程中的能量變化如圖所示。下列敘述正確的是( )
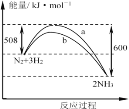
A.正反應的活化能等于逆反應的活化能
B.a曲線是加入催化劑時的能量變化曲線
C.1moN2與3moH2充分反應放出的熱量小于92kJ
D.增大壓強,可以提高反應物活化分子百分數
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)元素周期表中第VIIA族元素的單質及其化合物的用途廣泛。
①與氯元素同族的短周期元素的原子結構示意圖為______。
②能作為氯、溴、碘元素非金屬性(原子得電子能力)遞變規律的判斷依據是____。
a. Cl2、Br2、I2的熔點 b. Cl2、Br2、I2的氧化性
c. HCl、HBr、HI的熱穩定性 d. HCl、HBr、HI的酸性
③設計一個實驗方案,證明氧化性Cl2>Br2:___________。
(2)鉛是碳的同族元素,比碳多4個電子層。
①鉛在元素周期表的位置為_______。
②PbO2與濃鹽酸共熱生成黃綠色氣體,反應的化學方程式為___________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】SCR和NSR技術可有效降低柴油發動機在空氣過量條件下的NOx排放。
(1)SCR(選擇性催化還原)工作原理:
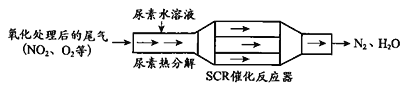
①尿素[CO(NH2)2]水溶液熱分解為NH3和CO2,請寫出CO2的電子式___________________。
②反應器內NH3還原NO2過程中,若還原產物比氧化產物少1mol,轉移電子總數__________個(用NA表示)。
③當燃油中含硫量較高時,尾氣中SO2在O2作用下會形成(NH4)2SO4,使催化劑中毒。用化學方程式表示(NH4)2SO4的形成_______________________________________________。
④尿素溶液濃度影響NO2的轉化,測定溶液中尿素(M=60 g·mol1)含量的方法如下:取a g尿素溶液,將所含氮完全轉化為NH3,所得NH3用過量的v1 mL c1 mol·L1 H2SO4溶液吸收完全,剩余H2SO4用v2 mL c2 mol·L1 NaOH溶液恰好中和,則尿素溶液中溶質的質量分數是________
(2)NSR(NOx儲存還原)工作原理:NOx的儲存和還原在不同時段交替進行,如圖a所示。
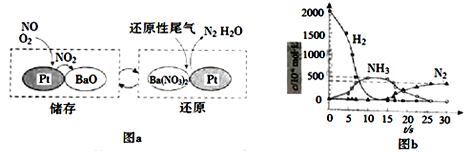
① 通過BaO和Ba(NO3)2的相互轉化實現NOx的儲存和還原。儲存NOx的物質是_________。
② 用H2模擬尾氣中還原性氣體研究了Ba(NO3)2的催化還原過程,該過程分兩步進行,圖b表示該過程相關物質濃度隨時間的變化關系。第一步反應消耗的H2與Ba(NO3)2的物質的量之比是__________。
③ 還原過程中,有時會產生笑氣(N2O)。用同位素示蹤法研究發現笑氣的產生與NO有關。在有氧條件下15NO與NH3以一定比例反應時,得到的笑氣幾乎都是15NNO。將該反應的化學方程式補充完整:________________________ ______15NNO+ ________H2O
______15NNO+ ________H2O
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)同一物質在氣態時的能量大于在液態時的能量。一定量的氫氣在氧氣中充分燃燒并放出熱量。若生成氣態水放出的熱量為Q1,生成液態水放出的熱量為Q2,那么Q1______(填“大于”“小于”或“等于”)Q2。
(2)已知:4HCl+O2=2Cl2+2H2O,該反應中,4molHCl被氧化,放出115.6kJ的熱量,則斷開1molH—O鍵與斷開1molH—Cl鍵所需能量相差約為______kJ。

(3)某溫度下在4L密閉容器中,X、Y、Z三種氣態物質的物質的量隨時間變化的曲線如圖:
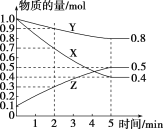
①該反應的化學方程式是__________。
②該反應達到平衡狀態的標志是________(填字母)。
A.Y的體積分數在混合氣體中保持不變
B.X、Y的反應速率之比為3:1
C.容器內氣體的壓強保持不變
D.容器內氣體的總質量保持不變
③0~2min內Y的轉化率為________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】1999年在一些國家的某些食品中“二惡英”含量嚴重超標,一時間掀起了席卷歐洲的“二惡英”恐慌癥。“二惡英”是二苯基-1,4-二氧六環及其衍生物的通稱,其中一種毒性最大的結構是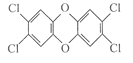 ,關于這種物質的敘述中不正確的是
,關于這種物質的敘述中不正確的是
A.該物質是一種芳香族化合物
B.該物質是一種鹵代烴
C.該物質是一種強烈致癌物
D.該物質分子中所有原子可能處在同一平面上
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com