
【題目】已知把ag金屬銅投入一定量濃硝酸中,反應開始產生紅棕色氣體,隨著反應的進行,產生的氣體顏色逐漸變淺,最后變?yōu)闊o色,反應過程中共收集到標準狀況下氣體VL,剩余固體bg。
(1)寫出反應過程中發(fā)生的化學反應___、___。
(2)在產生無色氣體的反應中___是還原劑;被還原的HNO3與參加反應的HNO3的質量之比為___;當有1molHNO3參加反應時,該反應轉移的電子的物質的量為___。
(3)在上面反應過程中,參加反應的HNO3的物質的量為___。
【答案】Cu+4HNO3(濃)=Cu(NO3)2+2NO2↑+2H2O 3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O Cu 1∶4 0.75mol (![]() +
+![]() )mol
)mol
【解析】
(1)硝酸的濃度不同,反應生成的產物不同,濃度較高生成二氧化氮,較低生成氣體一氧化氮;
(2)硝酸被還原成含氮氣體,未被還原的硝酸最后生成了Cu(NO3)2 ,寫出反應方程式分析解答;
(3)反應前后氮原子守恒的,而反應后氮原子存在于硝酸銅和含氮氣體當中,由此列出等式計算得出答案。
(1)濃硝酸氧化能力強,最后生成NO2,稀硝酸氧化性弱,最后生成NO ,所以反應開始是Cu+4HNO3(濃)=Cu(NO3)2+ 2NO2↑+2H2O,隨著反應進行,硝酸濃度降低,發(fā)生反應3Cu+ 8HNO3(稀)= 3Cu(NO3)2+ 2NO↑+4H2O;
故答案為:Cu+4HNO3(濃)=Cu(NO3)2+2NO2↑+2H2O;3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O;
(2)產生無色氣體,則是銅與稀硝酸的反應3Cu+ 8HNO3(稀)=3Cu(NO3)2+ 2NO↑+4H2O,其中Cu是還原劑,未被還原的HNO3最后形成Cu(NO3)2 ,從反應方程式中可以看出,被還原的HNO3(2mol)與參加反應的HNO3(8mol)的質量之比為1:4;1mol硝酸參加反應,則有![]() molCu參與反應,轉移電子
molCu參與反應,轉移電子![]() × 2mol=0.75mol;
× 2mol=0.75mol;
故答案為:Cu;1∶4;0.75mol;
(3 )根據(jù)氮原子反應前后守恒,則n總=2n硝酸銅+n氣體= 2n銅+ n氣體,由此可得參與反應的硝酸的物質的量是(![]() )mol=(
)mol=(![]() )mol,
)mol,
故答案為:(![]() )mol。
)mol。


科目:高中化學 來源: 題型:
【題目】NA是阿伏加德羅常數(shù)的值,下列說法正確的是( )
A.7.8g苯含σ鍵的數(shù)目為0.6NA
B.將Cl2通入FeBr2溶液中,有1molBr2生成時,轉移的電子數(shù)為2NA
C.1molNH4NO3完全溶于稀氨水中,溶液呈中性,溶液中NH![]() 的數(shù)目為NA
的數(shù)目為NA
D.有鐵粉參加的反應若生成3molFe2+,則轉移電子數(shù)一定為6NA
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】將氣體A、B置于固定容積為2 L的密閉容器中,發(fā)生如下反應:3A(g)+B(g)2C(g)+2D(g),反應進行到10 s末,達到平衡,測得A的物質的量為1.8 mol,B的物質的量為0.6 mol,C的物質的量為0.8 mol。
(1)用C表示10 s內反應的平均反應速率為________。
(2)反應前A的物質的量濃度是________。
(3)10 s末,生成物D的濃度為________。
(4)A與B的平衡轉化率之比為________。
(5)反應過程中容器內氣體的平均相對分子質量變化是________(填“增大”、“減小”或“不變”,下同),氣體的密度變化是________。
(6)平衡后,若改變下列條件,生成D的速率如何變化(填“增大”、“減小”或“不變”):①降低溫度______;②增大A的濃度________;③恒容下充入氖氣_______。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】設NA是阿伏加德羅常數(shù)的值。下列說法正確的是( )
A.1molNaHSO4固體中含有離子總數(shù)為3NA
B.11.2L(標準狀況)HF含有質子數(shù)為5NA
C.50g46%的乙醇水溶液中,含有O—H鍵數(shù)為3.5NA
D.1molCu與足量的硫蒸氣反應,轉移電子數(shù)為2NA
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】化學反應H2(g)+Cl2(g)=2HCl(g)的能量變化如圖所示,則下列說法中正確的是
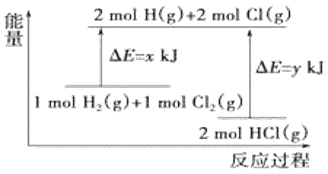
A.該反應是吸熱反應
B.斷裂1molH-H鍵和1molCl-Cl鍵時能放出x kJ的能量
C.斷裂2molH-Cl鍵時需要吸收y kJ的能量
D.2molHCl(g)的總能量高于1molH2(g)和1molCl2(g)的總能量
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】該小組的同學設計了如圖所示的實驗裝置(夾持及尾氣處理裝置未畫出),探究氨氣的還原性。
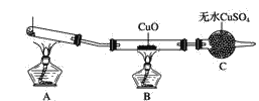
(1)利用該裝置進行實驗,觀察到CuO變?yōu)榧t色物質,無水CuSO4變藍色,同時生成一種無污染的氣體。則氨氣與CuO反應的化學方程式為___。
(2)有同學認為:NH3與CuO反應生成的紅色物質中可能含有Cu2O。已知:Cu2O是一種堿性氧化物,在酸性溶液中,Cu+→Cu+Cu2+。請設計一個簡單的實驗檢驗該紅色物質中是否含有Cu2O。____。
(3)該裝置在設計上存在明顯缺陷,為保證實驗結果的準確性,需在A和B之間增加一個裝置D,為什么?___。
請畫出裝置D的示意圖并表明所需試劑_____、_____。(限選儀器和藥品:濃H2SO4、堿石灰、集氣瓶、干燥管、玻璃導管、單孔賽、雙孔塞)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】生產工藝的實現(xiàn),涉及能源消耗、環(huán)境保護、綜合經濟效益等等。
Ⅰ.(1)下列單元操作中采用了熱交換工藝設備,以利用化學反應中放出的熱量,達到節(jié)能減排效果的有_______(填序號)。
A. 電解食鹽水制燒堿 B. 合成氨中的催化合成
C. 硫酸生產中的催化氧化 D. 煅燒石灰石制取生石灰
Ⅱ.以硅藻土為載體的五氧化二釩(V2O5)是接觸法生成硫酸的催化劑。從廢釩催化劑中回收V2O5既避免污染環(huán)境又有利于資源綜合利用。廢釩催化劑的主要成分為:
物質 | V2O5 | V2O4 | K2SO4 | SiO2 | Fe2O3 | Al2O3 |
質量分數(shù)/% | 2.20~2.90 | 2.8~3.32 | 22~28 | 60~65 | 1~2 | <1 |
以下是一種廢釩催化劑回收工藝路線:
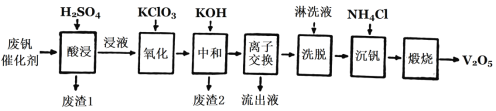
回答下列問題:
(2)“酸浸”時V2O4轉化為VO2+,反應的離子方程式為_________,同時V2O5轉化為VO2+。“廢渣1”的主要成分是________。
(3)“氧化”中使VO2+變?yōu)?/span>VO2+,則“氧化”環(huán)節(jié)中氧化劑與還原劑的物質的量之比為_____。
(4)“離子交換”和“洗脫”可簡單表示為:4ROH+V4O124-![]() R4V4O12+4OH(以ROH為強堿性陰離子交換樹脂)。為了提高化洗脫效率,淋洗液應該呈_______性(填“酸”“堿”“中”)。
R4V4O12+4OH(以ROH為強堿性陰離子交換樹脂)。為了提高化洗脫效率,淋洗液應該呈_______性(填“酸”“堿”“中”)。
(5)檢驗“流出液”中含量最多的陽離子,其實驗操作步驟是____。
(6)“煅燒”中發(fā)生反應的化學方程式2NH4VO3![]() V2O5+H2O+2NH3↑,寫出“沉釩”過程的離子方程式__________。
V2O5+H2O+2NH3↑,寫出“沉釩”過程的離子方程式__________。
(7)若有100 kg該廢釩催化劑,若轉化中釩元素利用率為80%,則最多可回收到V2O5__kg(保留小數(shù)點后一位)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】對于Zn(s)+H2SO4(aq)===ZnSO4(aq)+H2(g) ΔH<0的化學反應下列敘述不正確的是
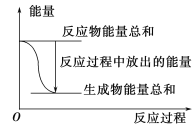
A. 反應過程中能量關系可用上圖表示
B. ΔH的值與反應方程式的計量系數(shù)有關
C. 若將該反應設計成原電池,鋅為負極
D. 若將其設計為原電池,當有32.5 g鋅溶解時,正極放出氣體一定為11.2 L
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有氯化鈉和碘化鈉的混合物共26.7 g,溶于水,通入足量氯氣后,蒸干、灼燒,固體質量變?yōu)?17.55 g。
(1)原混合物中碘化鈉的質量是________。
(2)原混合物中氯化鈉的質量分數(shù)是________。
查看答案和解析>>
湖北省互聯(lián)網違法和不良信息舉報平臺 | 網上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com