
【題目】最新報道:科學家首次用X射線激光技術觀察到CO與O在催化劑表面形成化學鍵的過程。反應過程的示意圖如下:
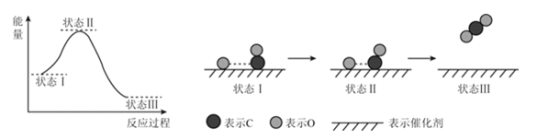
下列說法中正確的是
A. CO和O生成CO2是吸熱反應 B. 在該過程中,CO斷鍵形成C和O
C. CO和O生成了CO2 D. 狀態Ⅰ→狀態Ⅲ表示CO與O2反應的過程
科目:高中化學 來源: 題型:
【題目】在2A+B=3C+4D反應中,表示該反應速率最快的數據是
A. v(A)=0.5mol·L-1·s-1 B. v(B)=3mol·L-1·min-1
C. v(C)=0.9mol·L-1·s-1 D. v(D)=1.0mol·L-1·s-1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】實驗室制取氯氣的化學方程式:4HCl(濃)+MnO2 ![]() Cl2↑+MnCl2 +2H2O ,
Cl2↑+MnCl2 +2H2O ,
(1)反應物HCl中氯元素的化合價____,HCl在反應中表現的性質包括_______和______。
(2)在該氧化還原反應中,MnO2 做_________劑,錳元素被________。
(3)寫出該反應的離子方程式,并用單線橋法標出電子轉移的方向和數目:_______________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氮、硫及其化合物在工農業生產生活中有著重要作用。回答下列問題:
(1)有人設想利用CO還原SO2。已知S和CO的燃燒熱分別是296.0 kJ·mol1、283.0 kJ·mol1,請寫出CO還原SO2的生成CO2和S(s)熱化學方程式___________________________________。
(2)某科研小組研究臭氧氧化堿吸收法同時脫除SO2和NO工藝,氧化過程反應原理及反應熱、活化能數據如下:
反應Ⅰ:NO(g)+O3(g)![]() NO2(g)+O2(g) △H1=-200.9 kJmol1 Ea1=3.2 kJmol1
NO2(g)+O2(g) △H1=-200.9 kJmol1 Ea1=3.2 kJmol1
反應Ⅱ:SO2(g)+O3(g)![]() SO3(g)+O2(g) △H2=-241.6 kJmol1 Ea2=58 kJmol1
SO3(g)+O2(g) △H2=-241.6 kJmol1 Ea2=58 kJmol1
已知該體系中臭氧發生分解反應:2O3(g)![]() 3O2(g)。請回答:
3O2(g)。請回答:
其它條件不變,每次向容積為2 L的反應器中充入含2.0 mol NO、2.0 mol SO2的模擬煙氣和4.0 mol O3,改變溫度,反應相同時間t后體系中NO和SO2的轉化率如圖所示:

①由圖1可知相同溫度下NO的轉化率遠高于SO2,結合題中數據分析其可能原因_______。
②下列說法正確的是________。
A.Q點一定為平衡狀態點
B.溫度高于200℃后,NO和SO2的轉化率隨溫度升高顯著下降、最后幾乎為零
C.其它條件不變,若擴大反應器的容積可提高NO和SO2的轉化率
D.臭氧氧化過程不能有效地脫除SO2,但后續步驟堿吸收可以有效脫硫
③假設100℃時P、Q均為平衡點,此時反應時間為5min,發生分解反應的臭氧占充入臭氧總量的10%,則體系中剩余O3的物質的量是________mol;SO2的平均反應速率為________;反應Ⅰ在此時的平衡常數為_______________。
(3)以連二硫酸根(S2O42-)為媒介,使用間接電化學法也可處理燃煤煙氣中的NO,裝置如圖所示:

①ab是_______離子交換膜(填“陽”或“陰”)。陰極區的電極反應式為_____________。
②若NO吸收轉化后的產物為NH4+,通電過程中吸收4.48LNO(標況下),則陽極可以產生____mol氣體。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】將0.2 mol·L-1的KI溶液和0.05 mol·L-1Fe2(SO4)3溶液等體積混合后,取混合液分別完成下列實驗,能說明溶液中存在化學平衡“2Fe3++2I-![]() 2Fe2++I2”的是
2Fe2++I2”的是
實驗編號 | 實驗操作 | 實驗現象 |
① | 滴入KSCN溶液 | 溶液變紅色 |
② | 滴入AgNO3溶液 | 有黃色沉淀生成 |
③ | 滴入K3[Fe(CN)6]溶液 | 有藍色沉淀生成 |
④ | 滴入淀粉溶液 | 溶液變藍色 |
A. ①和② B. ②和④ C. ③和④ D. ①和③
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】保護環境,提倡“低碳生活”,是我們都應關注的社會問題。
(1)目前,一些汽車已改用天然氣(CNG)做燃料,以減少對空氣污染。
①16g甲烷完全燃燒生成液態水放出890kJ熱量,則甲烷燃燒的熱化學方程式是__________。
②1mol碳完全燃燒生成二氧化碳氣體放出393.5kJ熱量,通過計算比較,填寫下列表格(精確到0.01):
物質質量1g | 燃燒放出的熱量/kJ | 生成CO2的質量/g |
碳 | 32.80 | ____________ |
甲烷 | ____________ | 2.75 |
根據表格中的數據,天然氣與煤相比,用天然氣做燃料的優點是__________。
(2)為了減少二氧化碳的排放,利用海藻可將二氧化碳、氫氣轉化成水及一種可以再生的綠色能源乙醇,該反應的化學方程式是______________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一定量的![]() 在
在![]() 中燃燒后,所得混合氣體用100mL3.00mol/L的NaOH溶液恰好完全吸收,測得溶液中含0.05molNaClO。氫氣和氯氣物質的量之比是( )
中燃燒后,所得混合氣體用100mL3.00mol/L的NaOH溶液恰好完全吸收,測得溶液中含0.05molNaClO。氫氣和氯氣物質的量之比是( )
A.2:3B.3:1C.1:1D.3:2
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】工業上可由乙苯生產苯乙烯:![]() ,下列有關說法正確的是
,下列有關說法正確的是
A. 乙苯和苯乙烯均能發生取代反應、加聚反應和氧化反應
B. 用溴水可以區分苯乙烯和乙苯
C. 1 mol苯乙烯最多可與4 mol氫氣加成,加成產物的一氯代物共有5種
D. 乙苯和苯乙烯分子中共平面的碳原子數最多都為7
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】關節炎的成因是在關節滑液中形成尿酸鈉晶體——NaUr,其平衡關系為:Ur—(aq)+Na+(aq) ![]() NaUr(s),其中Ur—表示尿酸根離子。醫生常囑咐關節炎病人要注意保暖,特別是手腳等離心臟較遠的部位。因為第一次關節炎的發作大都在手指或腳趾的關節處。這說明
NaUr(s),其中Ur—表示尿酸根離子。醫生常囑咐關節炎病人要注意保暖,特別是手腳等離心臟較遠的部位。因為第一次關節炎的發作大都在手指或腳趾的關節處。這說明
A. 形成尿酸鈉晶體的反應為放熱反應 B. 形成尿酸鈉晶體的反應為吸熱反應
C. 尿酸鈉溶解度較大 D. 尿酸鈉晶體一定難溶于水
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com