
根據轉化關系判斷下列說法正確的是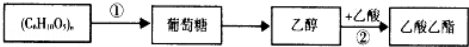
A.(C6H10O5)n可以是淀粉或纖維素,二者均屬于多糖,互為同分異構體
B.可以利用銀鏡反應證明反應①的最終產物為葡萄糖
C.酸性高錳酸鉀可將乙醇氧化為乙酸,將燒黑的銅絲趁熱插乙醇中也可得到乙酸
D.在反應②得到的混合物中倒入飽和氫氧化鈉溶液并分液可得到純凈的乙酸乙酯
 舉一反三單元同步過關卷系列答案
舉一反三單元同步過關卷系列答案科目:高中化學 來源:2015-2016學年黑龍江大慶鐵人中學高二上9月考化學試卷(解析版) 題型:填空題
(14分)請回答下列問題:
(1)下表列出了一些化學鍵的鍵能E:
化學鍵 | H—H | O===O | O—H |
E/kJ·mol-1 | 436 | x | 463 |
反應H2(g)+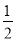 O2(g)===H2O(g) ΔH=-241.8 kJ·mol-1,則x=__________。
O2(g)===H2O(g) ΔH=-241.8 kJ·mol-1,則x=__________。
(2)鉛蓄電池是正極板上覆蓋有PbO2,負極板上覆蓋有Pb,電解質溶液是H2SO4溶液,電池放電時的總反應:Pb+PbO2+2H2SO4=2PbSO4+2H2O。
請寫出充電時陰極的電極反應式:
(3)反應m A+n B p C,在某溫度下達到平衡。
p C,在某溫度下達到平衡。

①若A、B、C都是氣體,減壓后正反應速率小于逆反應速率,則m、n、p的關系是_______。
②若C為氣體,且m + n = p,在加壓時化學平衡發生移動,則平衡必定向_______方向移動。
③若再升高溫度,平衡向逆向移動,則正反應為 反應(填“吸熱”或“放熱”)
(4)依據氧化還原反應Zn(s)+Cu2+(aq)===Zn2+(aq)+Cu(s)設計的原電池如圖所示。

①請在圖中標出電極材料及電解質溶液(寫化學式)
②鹽橋中的Cl-向________極移動(填“左”或“右”)。
查看答案和解析>>
科目:高中化學 來源:2014-2015學年廣東省佛山市高三上學期第一次月考化學試卷(解析版) 題型:選擇題
氫化鋰(LiH)屬于離子化合物。LiH跟水反應可以放出氫氣。下列敘述中正確的是
A.LiH的水溶液顯中性 B.LiH中的氫離子可以被還原生成氫氣
C.LiH是一種強氧化劑 D.LiH中氫離子比鋰離子的半徑大
查看答案和解析>>
科目:高中化學 來源:2016屆山東省滕州市高三第一學期開學初檢測化學試卷(解析版) 題型:填空題
[化學選修——2:化學與技術]我國火電廠粉煤灰的主要氧化物組成為SiO2、Al2O3、FeO、Fe2O3等。一種利用粉煤灰制取氧化鋁、硫酸鐵溶液、二氧化硅的工藝流程如下:
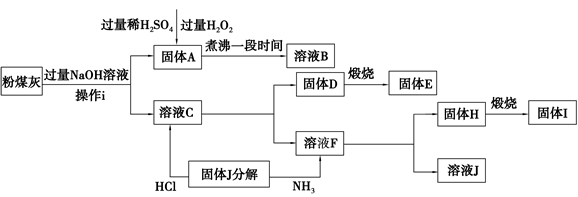
(1)操作i的名稱為 。
(2)工業上若需加快粉煤灰與NaOH溶液反應的浸出速率,可采取的措施有 (寫兩點即可)。
(3)寫出固體A溶解在稀硫酸中所得溶液與H2O2反應的離子方程式 。
(4)以上流程中可以循環利用的物質是 (填化學式)。
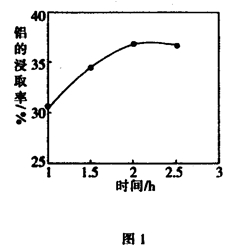
(5)某科研小組用硫酸作為浸取液,浸取粉煤灰中的鋁元素和鐵元素,在104℃用硫酸浸取時,鋁的浸取率與時間的關系如圖1,適宜的浸取時間為 h;鋁的浸取率與的關系如圖2所示,從浸取率角度考慮,三種助溶劑NH4F、KF及NH4F與KF的混合物,在相同時,浸取率最高的是 (填化學式)。

(6)Al/AgO電池是一種新型安全電池,廣泛用于軍事領域,其電池總反應為:2Al + 3AgO + 2OH―+ 3H2O 2[Al(OH)4]―+ 3Ag,則該電池工作時正極的電極反應方程式為 ,若電池產生6mol電子轉移,整體上分析電池負極消耗的OH―物質的量最終為 mol。
2[Al(OH)4]―+ 3Ag,則該電池工作時正極的電極反應方程式為 ,若電池產生6mol電子轉移,整體上分析電池負極消耗的OH―物質的量最終為 mol。
查看答案和解析>>
科目:高中化學 來源:2016屆貴州省貴陽市高三8月摸底考試化學試卷(解析版) 題型:選擇題
隨著公路上汽車流量的迅速增長,交通事故頻繁發生。汽車安全氣囊是在發生撞車時、產生二次碰撞前能夠自動膨脹保護乘員的裝置,碰撞時發生反應: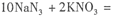
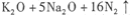 。下列判斷正確的是
。下列判斷正確的是
A.N2既是氧化劑又是還原劑
B.NaN3中N元素被還原
C.每生成16molN2轉移30mole-
D.還原產物與氧化產物質量之比為l:15
查看答案和解析>>
科目:高中化學 來源:2016屆安徽省等六校教研會高三第一次聯考化學試卷(解析版) 題型:填空題
下面是元素周期表的一部分,參照元素①-⑧在表中的位置,請用化學用語回答下列問題:
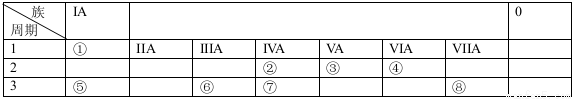
(1)④、⑤、⑦的原子半徑由大到小的順序為(元素符號)____________ ____。
(2)②、⑦、⑧的最高價含氧酸的酸性由強到弱的順序是(填化學式)_______。
(3)在①、④、⑤、⑧中的某些元素之間可形成既含離子鍵又含非極性共價鍵的離子化合物,寫出其中一種化合物的電子式:_______________。
(4)由②和④組成的化合物與⑤的同周期相鄰主族元素的單質反應的化學方程式為:_______。
(5)⑦單質與⑤的最高價氧化物的水化物反應的離子方程式為 。
(6)常溫下,由①②④組成最簡單的液態有機物可作為燃料電池的原料之一,請寫出其在堿性介質中的電極反應式: 。
查看答案和解析>>
科目:高中化學 來源:2016屆四川省高三秋季零診考試化學試卷(解析版) 題型:實驗題
(15分)某氯化鐵與氯化亞鐵的混合物。現要測定其中鐵元素的質量分數,實驗按以下步驟進行:

Ⅰ.請根據上面流程,回答以下問題:
(1)操作I所用到的玻璃儀器除燒杯、玻璃棒外,還必須有________、________,(填儀器名稱)。
(2)請寫出加入溴水發生的離子反應方程式__________________。
(3)將沉淀物加熱,冷卻至室溫,用天平稱量其質量為b1 g,再次加熱并冷卻至室溫稱量其質量為b2 g,若b1-b2=0.3g,則接下來還應進行的操作是____________;若蒸發皿質量是w1 g,蒸發皿與加熱后固體總質量是w2 g,則樣品中鐵元素的質量分數是_____。
Ⅱ.有同學提出,還可以采用以下方法來測定:

(1)溶解樣品改用了硫酸,而不在用鹽酸,為什么?
__________________________。
(2)選擇的還原劑是否能用鐵__________(填“是”或“否”),原因是:__________。
(3)若滴定用掉c mol/L KMnO4溶液b mL,則樣品中鐵元素的質量分數是____________。
查看答案和解析>>
科目:高中化學 來源:2016屆湖北省高三9月調考化學試卷(解析版) 題型:選擇題
下列各組離子在指定分散系中一定能大量共存的是
A.明礬溶液中:Na+、Mg2+、NO3-、HCO3-
B.澄清透明的溶液中:Na+、K+、MnO4-、ClO-
C.pH=0的溶液中:Al3+、Ag(NH3)2+、Cl?、SO42?
D.通入足量CO2后的溶液中:Na+、SiO32-、CH3COO-、SO32-
查看答案和解析>>
科目:高中化學 來源:2016屆江西省三校高三上第一次聯考化學試卷(解析版) 題型:選擇題
用NA表示阿伏加德羅常數的值。下列敘述正確的是
A.25℃時,1L pH=1的H2SO4溶液中,SO42-數目為0.1NA
B.將7.8gNa2O2放入足量的CO2和水蒸氣組成的氣體中充分反應,轉移電子總數為0.1 NA
C.9g重氧水(H218O)含電子總數為10 NA
D.常溫常壓下,2.24L正戊烷、異戊烷及新戊烷的混合物,含C-H數目為1.2 NA
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com