
| A. | 從海水中可以得到NaCl電解熔融NaCl可制備金屬鈉 | |
| B. | 海水蒸發制海鹽的過程中不涉及化學變化 | |
| C. | 從海水中提溴、碘、鎂單質,都利用了氧化還原反應 | |
| D. | 利用潮汐發電是將化學能轉化為電能 |
分析 A.從海水中可以得到NaCl,鈉為活潑金屬,電解熔融NaCl可制備金屬鈉;
B.海水中海鹽主要含有氯化鈉,經過海水蒸發制得氯化鈉,只發生了物理變化;
C.發生的化學反應中,若存在元素的化合價變化,則屬于氧化還原反應;
D.根據能量轉化的方式分析,潮汐發電的原理是潮汐能轉化為電能.
解答 解:A.從海水中得到氯化鈉后,可以電解熔融狀態的氯化鈉2NaCl$\frac{\underline{\;電解\;}}{\;}$2Na+Cl2↑,生成氯氣和金屬鈉,故A正確;
B.海水中海鹽主要含有氯化鈉,經過海水蒸發制得氯化鈉,是溶液中溶質和溶劑的分離,只發生了物理變化,沒有發生化學變化,故B正確;
C.海水提溴是由溴元素的化合物變為溴元素的單質,有元素化合價的變化,屬于氧化還原反應,海帶提碘是由KI變為I2,有元素化合價的變化,屬于氧化還原反應,
海水提鎂,涉及生成氫氧化鎂、氫氧化鎂與鹽酸反應,生成氯化鎂電解可生成鎂,涉及元素化合價的變化,屬于氧化還原反應,故C正確;
D.利用朝汐發電是朝汐能轉化為電能,沒有發生化學反應,而化學能轉化為電能必須要發生化學反應,故D錯誤;
故選D.
點評 本題考查化學變化、海水制鹽原理、氧化還原反應、潮汐發電等,題目難度不大,注意海水蒸發制海鹽的過程為物理變化,主要考查基本知識和基本反應原理,需要正確記憶并深化理解.


科目:高中化學 來源:2016-2017學年河北省唐山市高二上10月月考化學試卷 (解析版) 題型:選擇題
X、Y、Z、M、N代表五種金屬。有以下化學反應:
①水溶液中:X+Y2+===X2++Y
②Z+2H2O(冷)===Z(OH)2+H2↑
③M、N為電極與N鹽溶液組成原電池,發生的電極反應為:M-2e-===M2+
④Y可以溶于稀H2SO4中,M不被稀H2SO4氧化,則這五種金屬的活動性由弱到強的順序是( )
A.M<N<Y<X<Z B.N<M<X<Y<Z
C.N<M<Y<X<Z D.X<Z<N<M<Y
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 食鹽水 | B. | 白醋 | C. | 淀粉溶液 | D. | 蔗糖溶液 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
| 試管 | 溫度 | 過氧化氫濃度 | 催化劑 |
| a | 室溫(25℃) | 12% | 有 |
| b | 水浴加熱(50℃) | 4% | 無 |
| c | 水浴加熱(50℃) | 12% | 有 |
| d | 室溫(25℃) | 4% | 無 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
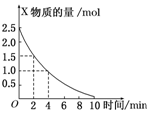 在容積為3L的密閉容器中,放入氣態物質X和Y在一定條件下發生反應2X+Y═2Z,如圖所示是該反應中X的物質的量隨時間變化的曲線.
在容積為3L的密閉容器中,放入氣態物質X和Y在一定條件下發生反應2X+Y═2Z,如圖所示是該反應中X的物質的量隨時間變化的曲線.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | CO2的電子式: | |
| B. | 乙烯的結構簡式:CH2CH2 | |
| C. | NH4Cl的電子式: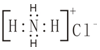 | |
| D. | 原子核內有10個中子的氧原子:${\;}_{8}^{18}$O |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 兩者生成硝酸銅的物質的量不同 | |
| B. | 濃硝酸產生的氣體更少 | |
| C. | 稀硝酸被還原之后的生成物的價態更低,所以稀硝酸的氧化性更強 | |
| D. | 兩個反應中的電子轉移的數目相同 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com