
| A. | 0.1molZn與含0.1molHCl的鹽酸充分反應,轉移的電子數目為0.2NA | |
| B. | 1molNa與足量O2反應,生成Na2O和Na2O2的混合物,轉移的電子數為NA | |
| C. | 1molNa2O2與足量CO2充分反應轉移的電子數為2NA | |
| D. | 向FeI2溶液中通入適量Cl2,當有1molFe2+被氧化時,共轉移的電子的數目為NA |
分析 A、0.1molZn與含0.1molHCl的鹽酸反應時,鋅過量;
B、根據反應后鈉元素為+1價來分析;
C、過氧化鈉與水的反應為歧化反應;
D、根據碘離子和亞鐵離子都能夠被氯氣氧化且先氧化碘離子再氧化亞鐵離子分析;
解答 解:A、0.1molZn與含0.1molHCl的鹽酸反應時,鋅過量,0.1mol鹽酸完全反應,轉移0.1mol電子即0.1NA個,故A錯誤;
B、由于反應后鈉元素為+1價,故1mol鈉反應轉移1mol電子即NA個,與產物無關,故B正確;
C、1mol Na2O2與足量CO2充分反應轉移的電子數為NA,故C錯誤;
D、FeI2溶液中,碘離子的還原性大于亞鐵離子的,通入適量氯氣,當有1molFe2+被氧化時,溶液中碘離子已經完全被氧化,由于不知道碘化亞鐵的物質的量,無法計算轉移的電子數,故D錯誤;
故選B.
點評 本題考查了阿伏伽德羅常數的有關計算,熟練掌握公式的使用和物質的結構是解題關鍵,難度不大.


 備戰中考寒假系列答案
備戰中考寒假系列答案科目:高中化學 來源: 題型:填空題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 標準狀況下,2.24L水所含的分子數目為0.1 NA | |
| B. | 9g水中含有的電子數目為0.5NA | |
| C. | 0.3 mol/L的MgCl2溶液中含Mg2+數目為0.3 NA | |
| D. | 常常壓下,28gN2和CO混合氣體中所含有的原子數目為2NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Ag+、K+、NO${\;}_{3}^{-}$、Cl- | B. | Mg2+、Na+、Cl-、SO${\;}_{4}^{2-}$ | ||
| C. | Ca2+、Mg2+、Fe2+、Cl- | D. | H+、Na+、CO${\;}_{3}^{2-}$、SO${\;}_{4}^{2-}$ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 (1)A、B、C、D、F五種物質的焰色反應均為黃色,A、B、C、D與鹽酸反應均生成E,此外B還生成一種可燃性氣體.而C、D還生成一種無色無味氣體H,該氣體能使澄清石灰水變渾濁.D和A可反應生成C,F和H也可反應生成C和另一種無色無味氣體.請回答下列問題:
(1)A、B、C、D、F五種物質的焰色反應均為黃色,A、B、C、D與鹽酸反應均生成E,此外B還生成一種可燃性氣體.而C、D還生成一種無色無味氣體H,該氣體能使澄清石灰水變渾濁.D和A可反應生成C,F和H也可反應生成C和另一種無色無味氣體.請回答下列問題:查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 某化學興趣小組同學看到一則報道:某造紙廠誤將槽車中漂白液(NaCl和NaClO的混合液)倒入盛放飽和KAl(SO4)2溶液的池中,造成中毒事件.該小組同學為探究中毒原因進行了如下實驗.
某化學興趣小組同學看到一則報道:某造紙廠誤將槽車中漂白液(NaCl和NaClO的混合液)倒入盛放飽和KAl(SO4)2溶液的池中,造成中毒事件.該小組同學為探究中毒原因進行了如下實驗.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
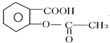 具有的官能團有酯基和羧基(寫名稱).用阿司匹林和氫氧化鈉中和制得可溶性阿司匹林,該反應的化學方程式為C6H5OOCCH3COOH+H2O→CH3COOH+C6H5OHCOOH.
具有的官能團有酯基和羧基(寫名稱).用阿司匹林和氫氧化鈉中和制得可溶性阿司匹林,該反應的化學方程式為C6H5OOCCH3COOH+H2O→CH3COOH+C6H5OHCOOH.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 膠體區別于其他分散系的本質特征是分散質的微粒直徑在1nm~100nm之間 | |
| B. | 用平行光照射CuSO4溶液和Fe(OH)3膠體,可以加以區分 | |
| C. | 把FeCl3飽和溶液滴入到NaOH溶液中,以制取Fe(OH)3膠體 | |
| D. | 樹林中的晨曦,該現象與丁達爾效應有關 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com