
| A. | 2.7 g | B. | 5.4 g | C. | 6.75 g | D. | 8.1 g |
分析 鹽酸和氫氧化鈉溶液中溶質的物質的量相同,加入鋁的質量相同,若Al都完全反應,則生成氫氣應相等,而應結束后測得生成的氣體體積比為2:5,由方程式:2Al+6HCl═2AlCl3+3H2↑、2Al+2NaOH+2H2O═2NaAlO2+3H2↑,可知酸與金屬反應時酸不過量,堿與金屬反應時堿過量,結合方程式計算解答.
解答 解:鹽酸和氫氧化鈉溶液中溶質的物質的量相同,加入鋁的質量相同,若Al都完全反應,則生成氫氣應相等,而應結束后測得生成的氣體體積比為2:5,由方程式:2Al+6HCl═2AlCl3+3H2↑、2Al+2NaOH+2H2O═2NaAlO2+3H2↑,可知酸與金屬反應時酸不過量,堿與金屬反應時堿過量.
鹽酸和氫氧化鈉溶液中溶質的物質的量均為0.1L×3mol/L=0.3mol,
設鋁與酸反應時酸完全反應,生成的氫氣的物質的量為x,則:
2Al+6HCl═2AlCl3+3H2↑
6 3
0.3mol x
解得x=$\frac{0.3mol×3}{6}$=0.15mol,
則堿與金屬鋁反應生成的氫氣的物質的量為0.15mol×$\frac{5}{2}$=0.375mol,
堿與金屬鋁反應時鋁完全反應,設與堿反應的鋁的物質的量為y,則:
2Al+2NaOH+2H2O═2NaAlO2+3H2↑
2 3
y 0.375mol
解得y=$\frac{0.375mol×2}{3}$=0.25mol,
則鋁的質量為0.25mol×27g/mol=6.75g,
故選:C.
點評 本題考查化學反應方程式的計算,關鍵是判斷反應中酸、堿是否足量,難度中等.


 快樂小博士鞏固與提高系列答案
快樂小博士鞏固與提高系列答案科目:高中化學 來源: 題型:選擇題
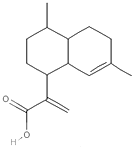
| A. | 能發生酯化反應 | B. | 屬于芳香族化合物 | ||
| C. | 能與NaHCO3溶液反應 | D. | 能使溴的四氯化碳溶液褪色 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
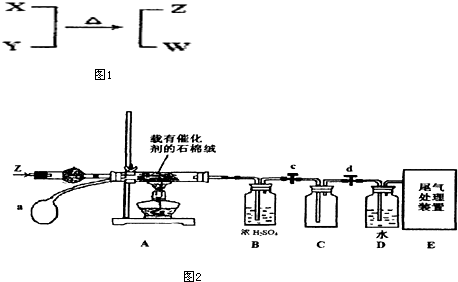
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 稱取1.8g氫氧化鈉固體,加入450mL水 | |
| B. | 稱取1.8g氫氧化鈉固體配成450mL溶液 | |
| C. | 稱取2.0g氫氧化鈉固體,加入500mL水 | |
| D. | 稱取2.0g氫氧化鈉固體配成500mL溶液 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ${\;}_{6}^{13}$C的質量數是13,原子序數是6,核內有6個中子 | |
| B. | ${\;}_{6}^{13}$C與金剛石、石墨、C60等互為同素異形體 | |
| C. | ${\;}_{6}^{13}$C與${\;}_{6}^{12}$C是兩種不同的碳元素 | |
| D. | ${\;}_{6}^{13}$C是碳的一種核素,與${\;}_{6}^{12}$C互為同位素 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
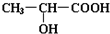
 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 氯原子的結構示意圖: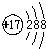 | |
| B. | 硫酸的電離方程式:H2SO4═H2++SO42- | |
| C. | 蘇打粉的化學式:NaHCO3 | |
| D. | 明礬的化學式:KAl(SO4)2•12H2O |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com