
| A. | 22.4LCO中一定含有6.02×1023個分子 | |
| B. | 在標準狀況下,22.4LCH4與18gH2O所含有的電子數均為10NA | |
| C. | 常溫常壓下,16gO2與16gO3含有的分了數相同 | |
| D. | 0.1mol/LK2SO4溶液中含有K+為0.2NA |
分析 A、CO所處的狀態不明確;
B、分別求出甲烷和水的物質的量,然后根據甲烷和水均為10電子分子來分析;
C、氧氣和臭氧的摩爾質量不同;
D、溶液體積不明確.
解答 解:A、CO所處的狀態不明確,故22.4LCO的物質的量無法計算,則含有的分子個數無法計算,故A錯誤;
B、標況下22.4L甲烷的物質的量為1mol,18g水的物質的量也為1mol,而甲烷和水均為10電子分子,故1mol甲烷和1mol水中含有的電子個數均為10NA個,故B正確;
C、氧氣和臭氧的摩爾質量分別為32g/mol和48g/mol,故16g氧氣和16g臭氧的物質的量之比為48:32=3:2,則分子個數之比也為3:2,故C錯誤;
D、溶液體積不明確,故溶液中的鉀離子的個數無法計算,故D錯誤.
故選B.
點評 本題考查了阿伏伽德羅常數的有關計算,熟練掌握公式的使用和物質的結構是解題關鍵,難度不大.


科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 濃度均為0.1 mol•L-1的CH3COOH和CH3COONa混合液,溶液顯酸性,則溶液中粒子濃度:c(CH3COOH)>c(CH3COO-)>c (Na+)>c(H+)>c(OH-) | |
| B. | 濃度均為0.1 mol•L-1的NaClO、NaHCO3混合溶液中:c(HClO)+c(ClO-)═c(HCO3-)+c(H2CO3) | |
| C. | 將0.2mol•L-1的某一元酸HA溶液和0.1mol•L-1的NaOH溶液等體積混合后溶液的pH大于7,則反應后的混合液:2c(OH-)+c(A-)═2c(H+)+c(HA) | |
| D. | 某二元弱酸的酸式鹽NaHA溶液中:c(H+)+c(Na+)═c(OH-)+c(HA-)+c(A2-) |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 得電子越多,其氧化性越強 | |
| B. | 陽離子只有氧化性,陰離子只有還原性 | |
| C. | 要完成SO32-→SO42-的轉化,必須加入氧化劑 | |
| D. | 金屬活動順序表中,排在前面的金屬陽離子的氧化性強于排在后面的金屬陽離子 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題

| A. | 稀釋前,c (A)>10 c (B) | |
| B. | 稀釋前,A溶液中水電離出的OH- 濃度是B溶液中由水電離出的OH- 濃度的10倍 | |
| C. | 在M點,A、B兩種堿溶液中陽離子的物質的量濃度相等 | |
| D. | M點時A和B的濃度相等 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 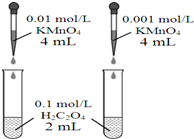 依據褪色快慢比較濃度對反應速率的影響 | |
| B. | 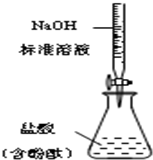 測定鹽酸濃度 | |
| C. | 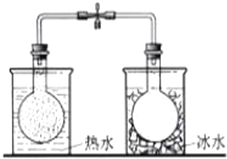 依據氣體顏色變化,證明溫度對平衡移動的影響 | |
| D. | 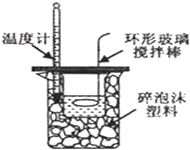 中和熱的測定 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com