
| A. | 丙烯分子中有8個σ鍵,1個π鍵 | |
| B. | 在SiO2晶體中,1個Si原子和2個O原子形成2個共價鍵 | |
| C. | NF3的沸點比NH3的沸點低得多,是因為NH3分子間有氫鍵,NF3只有范德華力 | |
| D. | NCl3和BC13分子中,中心原子都采用sp3雜化 | |
| E. | 在“冰→水→水蒸氣→氧氣和氫氣”的變化過程中,各階段被破壞的粒子間主要的相互作用依次是氫鍵、分子間作用力、極性鍵 |
分析 A.根據結構簡式CH3-CH=CH2判斷;
B.SiO2晶體中,每個Si原子形成4個共價鍵;
C.NH3分子間有氫鍵,沸點較高;
D.NCl3中N形成3個σ鍵,孤電子對數=1,為SP3雜化,BCl3中B形成3個σ鍵,無孤電子對,為sp2雜化;
E.根據冰→水→水蒸氣的過程為物理變化,破壞的是分子間作用力,主要是氫鍵,水蒸氣→氧氣和氫氣是化學變化,破壞的是化學鍵,為極性鍵
解答 解:A.結構簡式為CH3-CH=CH2,C-C、C-H鍵均為σ鍵,C=C中一個σ鍵,一個π鍵,則丙烯分子有8個σ鍵和1個π鍵,故A正確;
B.SiO2晶體中,每個Si原子形成4個共價鍵,1個O原子和2個Si原子形成2個共價鍵,故B錯誤;
C.NF3的沸點比NH3的沸點低得多,是因為NH3分子間有氫鍵,NF3分子間只有范德華力,故C正確;
D.NCl3中N形成3個σ鍵,孤電子對數=$\frac{5-3×1}{2}$=1,為SP3雜化,BCl3中B形成3個σ鍵,無孤電子對,為sp2雜化,故D錯誤;
E.固態水中和液態水中含有氫鍵,當冰→水→水蒸氣主要是氫鍵被破壞,但屬于物理變化,共價鍵沒有破壞,水蒸氣→氧氣和氫氣,為化學變化,破壞的是極性共價鍵,故E錯誤.
故選AC.
點評 本題綜合考查了共價鍵的形成和共價鍵的種類、雜化方式和類型、晶體的微粒間作用,綜合性較強,難度一般,注意基礎知識的積累.


科目:高中化學 來源: 題型:解答題
 有機物A是石油裂解的主要產物之一,其標準狀況下的密度為1.25g/L.反應⑦能緩解目前一個重要的環境問題,生成的聚合物G(C3H4O3)n是一種可降解塑料.有關轉化關系如圖所示:
有機物A是石油裂解的主要產物之一,其標準狀況下的密度為1.25g/L.反應⑦能緩解目前一個重要的環境問題,生成的聚合物G(C3H4O3)n是一種可降解塑料.有關轉化關系如圖所示: +CaCl2+2H2O.
+CaCl2+2H2O.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | V(逆)>V(正) | B. | V(逆)<V(正) | ||
| C. | V(逆)>V(正),正逆反應停止 | D. | V(逆)=V(正),正逆反應仍進行 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 25℃時pH=10的NaOH溶液與pH=10的氨水中:c(Na+)>c(NH${\;}_{4}^{+}$) | |
| B. | 物質的量濃度相等的CH3COOH和CH3COONa溶液等體積混合:c(CH3COO-)+c(OH-)=c(H+)+c(CH3COOH) | |
| C. | 在NaHA溶液中(H2A為弱酸):c(Na+)>c(HA-)>c(OH-)>c(H+) | |
| D. | 室溫下,向0.01 mol•L-1 NH4HSO4溶液中滴加NaOH溶液至中性:c(Na+)>c(SO${\;}_{4}^{2-}$)>c(NH${\;}_{4}^{+}$)>c(OH-)=c(H+) |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
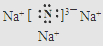 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 0.2mol Na+ | B. | 0.05mol CO${\;}_{3}^{2-}$ | ||
| C. | 6.02×1023個O | D. | 0.1mol H |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題

| A. | 甲、乙、丙三種單質全是非金屬 | |
| B. | 上述轉化關系所涉及的化合物中有一種是電解質 | |
| C. | 上圖所示的五個轉化關系中,有三個是化合反應 | |
| D. | 上圖所示的五個轉化關系中,均為放熱反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
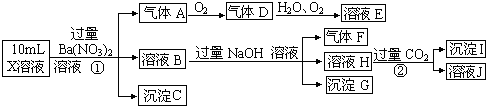
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1:9 | B. | 1:49 | C. | 1:99 | D. | 以上都不正確 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com