
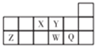
| A. | 離子Y2-和Z3+的核外電子排布相同 | |
| B. | X3-的離子半徑小于Z3+的離子半徑 | |
| C. | 元素Y的最高正價與最低負價絕對值之和為8 | |
| D. | 元素W的氣態氫化物的穩定性比Q的強 |
分析 根據元素所在周期表中的位置可知,X為N元素,Y為O元素,Z為Al元素,W為S元素,Q為Cl元素.
A.O2-、Al3+離子核外電子數均為10;
B.電子層結構相同,核電荷數越大,離子半徑越小;
C.氧元素沒有最高正化合價+6;
D.非金屬性越強,對應的氫化物的穩定性越穩定.
解答 解:根據元素所在周期表中的位置可知,X為N元素,Y為O元素,Z為Al元素,W為S元素,Q為Cl元素.
A.O2-、Al3+離子核外電子數均為10,二者核外電子排布相同,故A正確;
B.電子層結構相同,核電荷數越大,離子半徑越小,故離子半徑:N3->Al3+,故B錯誤;
C.Y為氧元素,沒有最高正化合價+6,故C錯誤;
D.同周期元素從左到右元素的非金屬性逐漸增強,對應的氫化物的穩定性逐漸增強,故D錯誤;
故選A.
點評 本題考查位置結構性質的相互關系及應用,難度中等,注意掌握元素周期表的結構和元素周期律的遞變規律.


 開心快樂假期作業暑假作業西安出版社系列答案
開心快樂假期作業暑假作業西安出版社系列答案 名題訓練系列答案
名題訓練系列答案 期末集結號系列答案
期末集結號系列答案科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
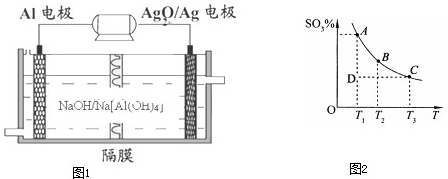
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
 ,其一氯代物的結構簡式是
,其一氯代物的結構簡式是 ;其中一氯代物種類最多的是
;其中一氯代物種類最多的是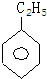 .(均填結構簡式)
.(均填結構簡式)查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | MgCl2+Ca(OH)2═CaCl2+Mg(OH)2↓ | B. | Mg(OH)2+2HCl═MgCl2+2H2O | ||
| C. | Mg(OH)2+H2SO4═MgSO4+2H2O | D. | MgCl2$\frac{\underline{\;通電\;}}{熔融}$Mg+Cl2↑ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Cl2通入水中:Cl2+H2O=2H++Cl-+ClO- | |
| B. | Mg(OH)2溶于硝酸:OH-+H+=H2O | |
| C. | Al與NaOH溶液反應:Al+2OH-=AlO2-+H2↑ | |
| D. | Ca(HCO3)2溶液與少量NaOH溶液反應:HCO3-+Ca2++OH-=CaCO3↓+H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 將pH=4的某酸稀釋10倍,測得其pH<5,則該酸為弱酸 | |
| B. | 0.1mol•L-1的NaHCO3溶液中C(Na+)=c(HCO3-)+c(H2CO3)+c(CO32-) | |
| C. | 0.1mol•L-1的NaHA溶液pH=5,則溶液:c(Na+)+c(H+)=c(OH-)+c(HA-)+c(A2-) | |
| D. | pH=4的醋酸與pH=10的氫氧化鈉溶液等體積混合,所得溶液pH<7 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

| 離子 | Na+ | Mg2+ | Cl- | SO42- |
| 濃度/(g•L-1) | 63.7 | 28.8 | 144.6 | 46.4 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com