
| A. | 碳酸鈉溶液 | B. | 氫氧化鈉溶液 | C. | 硫酸鉀溶液 | D. | 硝酸鈉溶液 |
分析 適當降低氫離子濃度、將Zn換為不如Zn活潑且能與氫離子反應生成氫氣的金屬能減緩反應速率,不影響生成氫氣總量,則酸最終電離出氫離子總量不變,以此解答該題.
解答 解:A.加入碳酸鈉,消耗硫酸,生成氫氣的量減少,故A錯誤;
B.加入氫氧化鈉,發生中和反應,消耗硫酸,生成氫氣的總量減小,故B錯誤;
C.加入硫酸鉀溶液,氫離子濃度減小,反應速率降低,但最終電離出氫離子物質的量不變,則生成氫氣總量不變,故C正確;
D.加入硝酸鈉溶液,硝酸和鋅反應不生成氫氣而生成氮氧化物,故D錯誤;
故選C.
點評 本題考查化學反應速率影響因素,為高頻考點,明確濃度、物質性質是解本題關鍵,易錯選項是D,注意D中隱含條件,題目難度不大.


科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 金屬氫化物都是強還原劑 | |
| B. | 金屬與H2制備金屬氫化合物時,H2作還原劑 | |
| C. | 金屬氫化物與水反應生成對應的堿和H2 | |
| D. | 離子半徑:r(H-)>r(Li+) |
查看答案和解析>>
科目:高中化學 來源: 題型:計算題
查看答案和解析>>
科目:高中化學 來源: 題型:計算題
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 若pH>7時,則一定是c1V1=c2V2 | |
| B. | 只有當pH<7時,才能滿足c(R+)+c(H+)=c(A-)+c(OH-) | |
| C. | 當pH=7時,若V1=V2,則一定是c1<c2 | |
| D. | 若V1=V2、c1=c2,則c(A-)+c(HA)=c(R+) |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
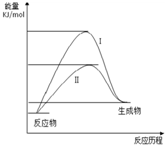 某化工生產反應歷程的能量變化如圖,過程I沒有使用催化劑,過程Ⅱ使用了催化劑,則可判斷催化劑除了能改變反應速率外,還可以改變的是( )
某化工生產反應歷程的能量變化如圖,過程I沒有使用催化劑,過程Ⅱ使用了催化劑,則可判斷催化劑除了能改變反應速率外,還可以改變的是( )| A. | 反應物的狀態 | B. | 反應的完成程度 | C. | 生產能耗 | D. | 反應熱效應 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com