
| 選項 | 實驗操作 | 實驗現象 | 實驗結論 | 離子反應 |
| A | 向FeCl2溶液中加入Zn片 | 淺綠色溶液變為無色 | Zn具有還原性 | Fe2++Zn═Zn2++Fe |
| B | 向FeCl2溶液中滴新制氯水 | 淺綠色溶液變為棕黃色 | Fe2+具有還原性 | 2Fe2++Cl2═2Fe3++2Cl- |
| C | 向FeCl3溶液中加入鐵粉 | 棕黃色溶液變為淺綠色 | Fe具有還原性 | Fe+Fe3+═2Fe2+ |
| D | 向FeCl3溶液中加入銅粉 | 藍色溶液變為棕黃色 | Fe3+具有氧化性 | Fe3++Cu═Fe2++Cu2+ |
| A. | A | B. | B | C. | C | D. | D |
分析 氯化亞鐵溶液為淺綠色,氯化鐵溶液為黃色,氯化鋅為無色,氯化銅為藍綠色;
A.鋅和氯化亞鐵溶液反應生成氯化鋅和鐵單質;
B.氯氣具有氧化性,氯化亞鐵具有還原性,二者在溶液中發生氧化還原反應生成氯化鐵溶液;
C.鐵還原氯化鐵溶液生成氯化亞鐵溶液;
D.向FeCl3溶液中加入銅粉,氯化鐵具有氧化性和銅發生氧化還原反應生成氯化亞鐵和氯化銅;
解答 解:A.鋅具有還原性,氯化亞鐵溶液中+2價的鐵,具有氧化性,能氧化鋅發生氧化還原反應,鋅置換出鐵發生的置換反應,溶液顏色變化的同時會析出黑色固體鐵,實驗現象描述錯誤,離子方程式正確,故A錯誤;
B.在氯化亞鐵溶液中滴加新制氯水,氯化亞鐵溶液為淺綠色,+2價的鐵被氯水氧化,生成+3價的鐵,溶液淺綠色變為棕黃色,離子方程式正確,故B正確;
C.向FeCl3溶液中加入鐵粉發生反應生成氯化亞鐵,棕黃色溶液變為淺綠色,離子反應的方程式左右電荷不守恒,正確為:2Fe3++Fe=3Fe2+,故C錯誤;
D.實驗現象中,溶液的顏色反應前氯化鐵溶液為黃色,Fe3+具有氧化性氧化銅生成氯化亞鐵和氯化銅溶液,反應后氯化亞鐵溶液為淺綠色,氯化銅溶液為藍綠色,離子方程式電荷不守恒,正確的為:2Fe3++Cu═2Fe2++Cu2+,故D錯誤;
故選B.
點評 該題主要考查了各種金屬化合物在溶液中的顏色,氧化還原反應的分析,要求能根據顏色判斷是什么物質,根據元素化合價變化對氧化還原反應的理解應用,題目難度中等.


科目:高中化學 來源: 題型:選擇題
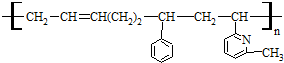
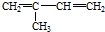
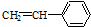
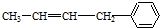
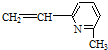
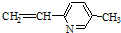
| A. | ②③⑥ | B. | ①②⑥ | C. | ②③⑤ | D. | ②④⑥ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | KN03 | B. | NH4NO3 | C. | CaC2 | D. | P4(白磷) |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| ① | ② | ③ | 實驗結論或目的 | 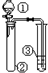 | |
| A | 濃鹽酸 | KMnO4 | 石蕊試液 | 氯氣的水溶液有酸性、漂白性 | |
| B | 稀硫酸 | Na2S | AgNO3與AgCl的濁液 | Ksp(AgCl)>Ksp(Ag2S) | |
| C | 硝酸 | Na2CO3溶液 | Na2SiO3溶液 | 比較硝酸、碳酸、硅酸酸性強弱 | |
| D | 溴水 | FeBr3、苯 | AgNO3溶液 | 苯和溴水能發生取代反應 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
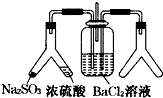
| A. | 只有①② | B. | 只有③⑤ | C. | 只有①②③ | D. | 只有①②④⑤ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | H+、K-、CIO-、Fe2+ | B. | OH-、Na+、Mg2+、Br- | ||
| C. | Cu2+、H+、CI-、NO3- | D. | Na+、SiO32-、Ca2+、CI- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 有單質鐵生成 | B. | 有氣泡產生、最終有白色沉淀生成 | ||
| C. | 氧化劑只有H20 | D. | 被氧化的元素有鈉、鐵兩種元素. |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 原子半徑:W>Y>X | |
| B. | 元素X與M形成的化合物的空間構型可能是正四面體、直線型或平面型 | |
| C. | 將XZ2通入W單質與水反應后的溶液中,生成的鹽一定只有一種 | |
| D. | 由Z、M兩種種元素形成的化合物一定只有極性共價鍵 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com