
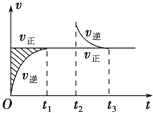
 恒溫密閉容器發生可逆反應:Z(?)+W(?)?X(g)+Y(?);△H,在t1時刻反應達到平衡,在t2時刻縮小容器體積,t3時刻再次達到平衡狀態后不再改變條件.下列有關說法中正確的是( )
恒溫密閉容器發生可逆反應:Z(?)+W(?)?X(g)+Y(?);△H,在t1時刻反應達到平衡,在t2時刻縮小容器體積,t3時刻再次達到平衡狀態后不再改變條件.下列有關說法中正確的是( )| A、Z和W在該條件下都不可能為氣態 |
| B、t1~t2時間段與t3時刻后,兩時間段反應體系中氣體的平均摩爾質量不可能相等 |
| C、若該反應只在某溫度T0以上自發進行,則該反應的平衡常數K隨溫度升高而增大 |
| D、若在該溫度下此反應平衡常數表達式為K=c(X),則t1~t2時間段與t3時刻后的X濃度不相等. |


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:
 (1)某溫度下,純水中的c(H+)=2.0×10-7mol/L,此時溶液的c(OH-)=
(1)某溫度下,純水中的c(H+)=2.0×10-7mol/L,此時溶液的c(OH-)=查看答案和解析>>
科目:高中化學 來源: 題型:
| A、0.2 mol?L-1 |
| B、0.25 mol?L-1 |
| C、0.45 mol?L-1 |
| D、0.225 mol?L-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:
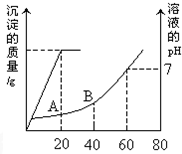
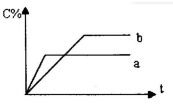 如圖表示可逆反應A(g)+B(g)?nC(g)△H<0,在不同條件下反應混合物中C的質量分數C%和反應過程所需時間的關系曲線,有關敘述一定正確的是( )
如圖表示可逆反應A(g)+B(g)?nC(g)△H<0,在不同條件下反應混合物中C的質量分數C%和反應過程所需時間的關系曲線,有關敘述一定正確的是( )| A、a表示有催化劑,而b無催化劑 |
| B、若其他條件相同,a比b的溫度高 |
| C、若其他條件相同,a比b的壓強大,n=l |
| D、反應由逆反應方向開始 |
查看答案和解析>>
科目:高中化學 來源: 題型:
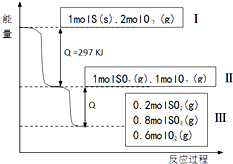 (已知:2SO2(g)+O2(g)?2SO3(g)△H=-196.6KJ?mol- 1),恒溫恒容條件下,硫可以發生如下轉化,其反應過程和能量關系,如圖所示.以下敘述錯誤的是( )
(已知:2SO2(g)+O2(g)?2SO3(g)△H=-196.6KJ?mol- 1),恒溫恒容條件下,硫可以發生如下轉化,其反應過程和能量關系,如圖所示.以下敘述錯誤的是( )| A、表示硫的燃燒熱的熱化學方程式:S(s)+O2(g)═SO2 (g)△H=-297 KJ?mol-1 |
| B、由Ⅱ到Ⅲ的過程放出的熱量為98.3KJ |
| C、恒溫恒容時,1molSO2和2molO2 充分反應,放出熱量的數值大于78.64KJ |
| D、將Ⅲ中的混合氣體通入足量的NaOH溶液中消耗NaOH的物質的量為 2mol |
查看答案和解析>>
科目:高中化學 來源: 題型:
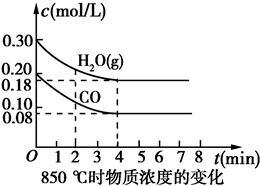 已知:CO(g)+H2O(g)?CO2(g)+H2(g)△H=Q,其平衡常數隨溫度變化如下表所示:
已知:CO(g)+H2O(g)?CO2(g)+H2(g)△H=Q,其平衡常數隨溫度變化如下表所示:| 溫度/℃ | 400 | 500 | 850 |
| 平衡常數 | 9.94 | 9 | 1 |
查看答案和解析>>
科目:高中化學 來源: 題型:
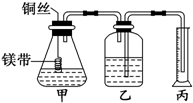 某研究性學習小組為證明在同溫同壓下,相同濃度、相同體積酸性不同的兩種二元酸與足量鎂帶反應時,生成氫氣的體積相同而反應速率不同,同時測定實驗室條件下的氣體摩爾體積.設計的簡易實驗裝置如圖所示.該實驗的主要操作步驟如下:
某研究性學習小組為證明在同溫同壓下,相同濃度、相同體積酸性不同的兩種二元酸與足量鎂帶反應時,生成氫氣的體積相同而反應速率不同,同時測定實驗室條件下的氣體摩爾體積.設計的簡易實驗裝置如圖所示.該實驗的主要操作步驟如下:查看答案和解析>>
科目:高中化學 來源: 題型:
A、碳在氧氣中燃燒,n(C)/n(O2)與生成物的關系: |
B、分散系的分類與分散質粒直徑大小關系: |
C、AlCl3和NaOH反應后鋁元素的存在形式與反應物中n(OH-)/n(Al3+) |
D、Na與O2反應的產物與反應物n(Na)/n(O2)的關系: |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com