
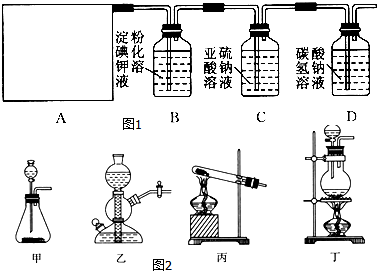
分析 依據實驗目的:制取氯氣并驗證其性質,依據化學方程式為Ca(ClO)2+CaCl2+2H2SO4$\frac{△}{\;}$2CaSO4+2Cl2↑+2H2O中反應物狀態和反應條件選擇發生裝置,然后依次通入盛有淀粉碘化鉀溶液的B、亞硫酸鈉溶液的C、碳酸氫鈉溶液的D驗證氯水的性質,注意氯氣有毒,需要進行尾氣處理,據此解答;
(1)根據反應物的狀態及反應條件選擇氣體的發生裝置;
(2)氯氣具有強的氧化性,與碘化鉀反應生成單質碘和氯化鉀,單質碘遇淀粉變藍;氯氣是有毒的氣體,不能直接排放到空氣中,要用尾氣處理裝置處理;
(3)氯氣溶于水和水反應生成鹽酸和次氯酸,鹽酸和碳酸氫鈉反應生成水和二氧化碳;
(4)亞硫酸鈉被氧化生成硫酸鈉,只有驗證硫酸根離子的存在就可證明亞硫酸鈉已經被氧化;
解答 解:(1)從方程式可知反應物是固體和液體,反應條件是加熱,所以應選固液混合加熱型裝置,
故答案為:丁;
(2)氯氣具有強的氧化性,碘化鉀反應2KI+Cl2═2KCl+I2,生成的I2遇到淀粉變藍色;氯氣是有毒的氣體,不能直接排放到空氣中,要用尾氣處理裝置處理;
故答案為:溶液變成藍色;2KI+Cl2═2KCl+I2;無尾氣吸收;
(3)D裝置中發生兩個反應:氯氣和水反應、鹽酸和碳酸氫鈉,反應的離子方程式分別為:Cl2+H2O═H++Cl-+HClO,H++HCO3-═H2O+CO2↑,
故答案為:Cl2+H2O═H++Cl-+HClO,H++HCO3-═H2O+CO2↑.
(4)亞硫酸鈉被氧化生成硫酸鈉,只有驗證硫酸根離子的存在就可證明亞硫酸鈉已經被氧化,檢驗硫酸根離子的存在選用試劑稀鹽酸和氯化鋇溶液,實驗設計如下:取少量溶液置于潔凈試管中,向其中加入稀鹽酸至不再產生氣體,再向其中滴入氯化鋇溶液,若產生白色沉淀證明Na2SO3已被氧化;
故答案為:取少量溶液置于潔凈試管中,向其中加入稀鹽酸至不再產生氣體,再向其中滴入氯化鋇溶液,若產生白色沉淀證明Na2SO3已被氧化;
點評 本題考查氯氣的實驗室制備、氯氣的性質、實驗的設計,硫酸根離子的檢驗注意排除其他離子的干擾.


科目:高中化學 來源: 題型:選擇題
| A. | 若誤飲c(Ba2+)=1.0×10-5mol/L溶液時,不會引起Ba2+中毒 | |
| B. | 因為Ksp(BaCO3)>Ksp(BaSO4),所以BaCO3不能作內服造影劑 | |
| C. | 向同濃度Na2SO4和Na2CO3的混合溶液中滴加BaCl2溶液,BaSO4先析出 | |
| D. | 在BaSO4和BaCO3共存的懸濁液中,c(SO42-):c(CO32-)=1:51 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 10.5% | B. | 9.1% | C. | 8% | D. | 5% |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | S與Cu反應:Cu+S$\frac{\underline{\;\;△\;\;}}{\;}$CuS | |
| B. | 酸雨放置過程中pH變小:2H2SO3+O2═2H2SO4 | |
| C. | 亞硫酸氫鈣溶液與澄清的石灰水混合:Ca2++HSO3-+OH-═CaSO3↓+H2O | |
| D. | 向Na2S和Na2SO3的混合溶液中滴加稀H2SO4[n(Na2S):n(Na2SO3)=2:1]:2S2-+SO32-+6H+═3S↓+3H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 二氧化硅是酸性氧化物,它可以跟強堿反應,但是不能與任何酸反應 | |
| B. | 根據SiO2+CaCO3$\frac{\underline{\;高溫\;}}{\;}$CaSiO3+CO2↑的反應,可推知硅酸酸性比碳酸強 | |
| C. | 二氧化碳氣體通入硅酸鈉溶液中可以制得硅酸 | |
| D. | 二氧化硅對應的水化物只有H2SiO3 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
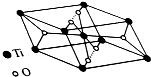 (1)下列說法正確的是AD(填序號)
(1)下列說法正確的是AD(填序號) ,Ni能與CO形成正四面體形的配合物Ni(CO)4,1 mol Ni(CO)4的含有σ 鍵的數目為8NA.
,Ni能與CO形成正四面體形的配合物Ni(CO)4,1 mol Ni(CO)4的含有σ 鍵的數目為8NA.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
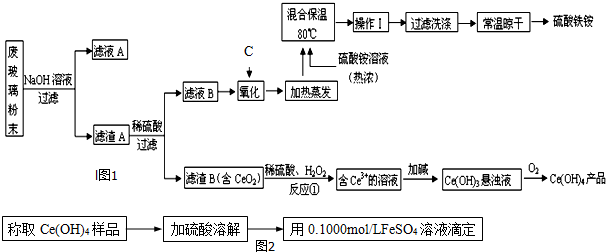
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 除去N2中的O2:通過灼熱的CuO粉末,收集氣體 | |
| B. | 某吸熱反應能自發進行,則該反應一定是熵增的反應 | |
| C. |  如圖是從化學試劑商店買回的硫酸試劑標簽,配制80mL2.3mol•L-1的稀硫酸需量取該硫酸12.5 mL | |
| D. | 下列各種物質在一定條件下反應,所得產物與反應物的用量或與反應條件無關①Na2SiO3+CO2+H2O ②Fe+Cl2 ③Ca(HCO3)2+Ca(OH)2 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com