
| △ |
| t/min | 0 | 5 | 10 |
| AO/mol?Lˉ1 | 1.00 | 0.65 | 0.50 |
| H2/mol?Lˉ1 | 2.00 | 1.00 | |
| AH3OH/mol?Lˉ1 | 0.00 | 0.35 | 0.50 |
 ,
, ;
;| 3 |
| 12 |
| 4 |
| 32 |
| 0.7mol/L |
| 5min |
| 0.5 |
| 0.5×12 |


科目:高中化學 來源: 題型:
| A | CH3CH3+Cl2
CH2=CH2+HCl→CH3CH2Cl | 均為取代反應 | ||
| B | 明礬用于凈水 碳酸鈉溶液顯堿性 | 均發生了水解反應 | ||
| C | Cl2+2Br?=2Cl?+Br2 Zn+Cu2+=Zn2++Cu | 均為單質被還原的置換反應 | ||
| D | 2Na2O2+2H2O=4NaOH+O2↑ Cl2+H2O=HCl+HClO | 均為水作還原劑的氧化還原反應 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化學 來源: 題型:
| 2 |
| 3 |
查看答案和解析>>
科目:高中化學 來源: 題型:
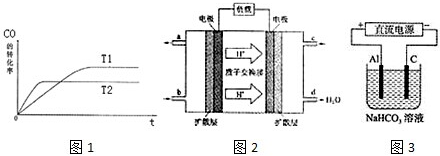
 純堿、燒堿等是重要的化工原料.
純堿、燒堿等是重要的化工原料.| 實驗操作 | 實驗現象 | 結論 |
| (1)取少量白色固體于試管中,加足量水溶解,再加足量BaCl2溶液 | ||
| (2) |
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com