
| ||
| ||
| 1 |
| 0.8 |


科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
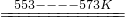 SiHCl3(l)+H2(g)
SiHCl3(l)+H2(g)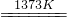 Si(純)+3HCl
Si(純)+3HCl
查看答案和解析>>
科目:高中化學 來源:專項題 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:
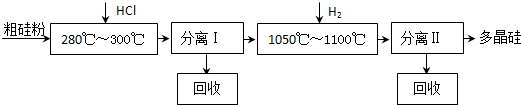
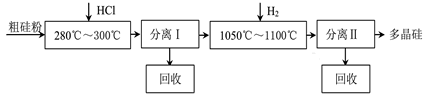
(10分)我國目前制備多晶硅主要采用三氯氫硅氫還原法、硅烷熱解法和四氯化硅氫還
原法。由于三氯氫硅還原法具有一定優點,被廣泛應用。其簡化的工藝流程如圖所示:
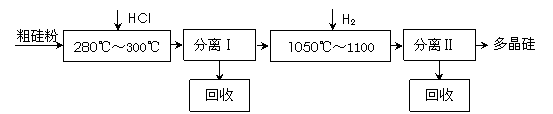 |
(1)制備三氯氫硅的反應為:Si(s)+3HCl(g) == SiHCl3(g)+H2(g) ΔH=-210 kJ•mol-1。
伴隨的副反應有:Si(s)+4HCl(g) == SiCl4(g)+2H2(g) ΔH=-241 kJ•mol-1。
SiCl4在一定條件下與H2反應可轉化為SiHCl3,反應的熱化學方程式為:
![]() SiCl4(g)+H2(g) == SiHCl3(g)+HCl(g) ΔH= 。
SiCl4(g)+H2(g) == SiHCl3(g)+HCl(g) ΔH= 。
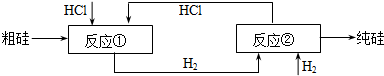
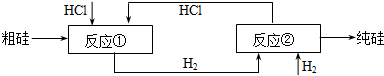
(2)由純SiHCl3制備高純硅的化學反應方程式為 。該生產工藝中可以循環使用的物質是 (至少寫出兩種)。
(3)由于SiH4具有易提純的特點,因此硅烷熱分解法是制備高純硅很有發展潛力的方法。工業上廣泛采用的合成硅烷方法是讓硅化鎂和固體氯化銨在液氨介質中反應得到硅烷,化學方程式是 ;整個制備過程必須嚴格控制無水,否則反應將不能生成硅烷,而是生成硅酸和氫氣等,其化學方程式為 ;整個系統還必須與氧隔絕,其原因是 。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com