
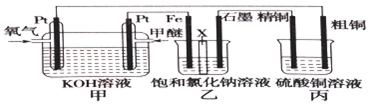
分析 (1)甲裝置為燃料電池是將化學能轉變為電能的裝置,屬于原電池,投放燃料的電極是負極,負極上燃料失電子發生氧化反應;
(2)乙裝置為電解氯化鈉裝置,鐵電極連接原電池的負極,為電解池的陰極,石墨為陽極,氫氧化鈉在陰極生,;
(3)丙裝置為精煉銅裝置,活潑性Zn>Cu>Ag,陽極上鋅、銅被氧化;
(4)根據轉移電子數相等知,陽極上溶解的銅小于陰極上析出的銅,所以丙裝置中反應一段時間,硫酸銅溶液濃度將減小;
(5)據串聯電池中轉移電子數相等得氧氣和銅的關系式為:O2-----2Cu計算;
(6)用石墨作電極電解體積為2L的CuSO4溶液生成銅、氧氣和硫酸;補充22.2gA即Cu2(OH)2CO3,其物質的量為0.1mol,即可使電解液恢復原濃度與體積,根據銅元素守恒可知,n[CuSO4]=0.2mol,根據c=$\frac{n}{V}$計算;若將丙設計成在鍍件上鍍銅的裝置,則銅作陽極,鍍件作陰極;
(7)若將乙中的交換膜去掉,發現只有H2逸出,則生成的氯氣與氫氧化鈉繼續反應生成氯化鈉和次氯酸鈉,據此書寫.
解答 解:(1)甲裝置為燃料電池是將化學能轉變為電能的裝置,屬于原電池,投放燃料的電極是負極,負極上甲醚失電子和氫氧根離子反應生成碳酸根離子和水,電極反應式為:CH3OCH3-12e-+16OH-═2CO32-+11H2O,
故答案為:CH3OCH3-12e-+16OH-═2CO32-+11H2O;
(2)乙裝置為電解氯化鈉裝置,鐵電極連接原電池的負極,為電解池的陰極,石墨為陽極,陽極上氯離子放電生成氯氣,陰極上氫離子放電,導致陰極附近氫氧根離子濃度大于氫離子濃度溶液呈堿性,所以乙裝置中生成氫氧化鈉主要在鐵極區,故答案為:鐵極;
(3)如果粗銅中含有鋅、銀等雜質,陽極上不僅銅還有鋅、銀失電子進入溶液,陰極上析出銅離子,陽極電極方程式分別為Zn-2e-=Zn2+、Cu-2e-=Cu2+,故答案為:Zn-2e-=Zn2+、Cu-2e-=Cu2+;
(4)由(3)陽極電極方程式分別為Zn-2e-=Zn2+、Cu-2e-=Cu2+,根據轉移電子數相等知,陽極上溶解的銅小于陰極上析出的銅,所以丙裝置中反應一段時間,硫酸銅溶液濃度將減小,
故答案為:減小;
(5)根據串聯電池中轉移電子數相等得氧氣和銅的關系式為:O2----2Cu,設生成銅的質量是x,
O2---------2Cu
22.4L 128g
2.24L x
x=12.8g,
故答案為:12.8 g;
(6)用石墨作電極電解體積為2L的CuSO4溶液生成銅、氧氣和硫酸,離子方程式為:2Cu2++2H2O$\frac{\underline{\;電解\;}}{\;}$2Cu+O2↑+4H+,補充22.2gA即Cu2(OH)2CO3,其物質的量為0.1mol,即可使電解液恢復原濃度與體積,根據銅元素守恒可知,n[CuSO4]=0.2mol,所以則原溶液CuSO4的濃度是$\frac{0.2mol}{2L}$=0.1mol•L-1;若將丙設計成在鍍件上鍍銅的裝置,則銅作陽極,鍍件作陰極,所以將陽極粗銅改成純銅,將陰極純銅改成鍍件即可,故答案為:2Cu2++2H2O$\frac{\underline{\;電解\;}}{\;}$2Cu+O2↑+4H+;0.1;將陽極粗銅改成純銅,將陰極純銅改成鍍件;
(7)若將乙中的交換膜去掉,發現只有H2逸出,則生成的氯氣與氫氧化鈉繼續反應生成氯化鈉和次氯酸鈉,總反應為:NaCl+H2O$\frac{\underline{\;電解\;}}{\;}$NaClO+H2↑,故答案為:NaCl+H2O$\frac{\underline{\;電解\;}}{\;}$NaClO+H2↑.
點評 本題考查原電池和電解池知識,為高考常見題型,側重于學生的分析能力和計算能力的考查,注意把握電極方程式的書寫,為解答該題的關鍵,結合串聯電路的特點解答該題,難度不大.


 小博士期末闖關100分系列答案
小博士期末闖關100分系列答案 名校名師培優作業本加核心試卷系列答案
名校名師培優作業本加核心試卷系列答案科目:高中化學 來源: 題型:選擇題
| A. | 能使酚酞試液變紅的溶液中:H+、SO42-、Na+、NO3- | |
| B. | 加入Al能放出氫氣的溶液中:NH4+、SO42-、Mg2+、HCO3- | |
| C. | 含有大量Cl2的溶液中:Ba2+、K+、NO3-、I- | |
| D. | 強酸性的溶液中:Cu2+、Br-、Ca2+、Cl- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 0.1mol•L-1氨水中,c(OH-)=c(NH4+) | |
| B. | 在0.1mol•L-1CH3COONa溶液中,c(OH-)=c(CH3COOH)+c(H+) | |
| C. | 10 mL 0.02mol•L-1HCl溶液與10 mL 0.02mol•L-1Ba(OH)2溶液充分混合,若混合后溶液的體積為20 mL,則溶液的pH=10 | |
| D. | 0.1mol•L-1某二元弱酸強堿鹽NaHA溶液中,c(Na+)=2c(A2-)+c(HA-)+c(H2A) |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Na2B溶液存在H2B | |
| B. | NaHB溶液一定顯堿性 | |
| C. | NaHB溶液一定顯酸性 | |
| D. | NaHB溶液與稀鹽酸反應的離子方程式是HB-+H+=H2B |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①③④ | B. | ①②④ | C. | ②③④ | D. | ①②③④ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 35.5 | B. | 71g | C. | 35.5g/mol | D. | 71g/mol |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 11.24 g | B. | 22.8 g | C. | 17.02 g | D. | 24.84 g |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com