
【題目】以淀粉為主要原料合成一種具有果香味有機物C和高分子化合物E的合成路線如下圖所示。

請回答下列問題:
(1)E的結構簡式為_________________, D中含有官能團的名稱為:_________。
(2)寫出下列反應的反應類型:③____________________,⑤____________________。
(3)寫出下列反應的化學方程式:
①____________________________________________________________________ ;
③_____________________________________________________________________。
D與HBr反應:________________________________________________________。
(4)某同學欲用下圖裝置制備物質C,將試管B中乙酸乙酯分離出來,用到的主要玻璃儀器有:燒杯、____________,試管B中盛裝的溶液為_________________,其作用為:__________。

A.中和乙酸和乙醇
B.中和乙酸并吸收部分乙醇
C.乙酸乙酯在飽和碳酸鈉溶液中的溶解度比在水中更小,有利于分層析出
D.加速酯的生成,提高其產率
試管A中防止液體加熱暴沸所采用的方法是:____________,其中濃硫酸的作用除催化劑外還有:______,目的是:_____________________。(從化學平衡角度分析)
(5)與C互為同分異構且能與Na2CO3反應生成CO2的有機物的結構簡式為:_________、___________。
【答案】 ![]() 碳碳雙鍵 酯化反應(或取代反應) 加聚反應 2CH3CH2OH+O2
碳碳雙鍵 酯化反應(或取代反應) 加聚反應 2CH3CH2OH+O2![]() 2CH3CHO+2H2O CH3COOH+CH3CH2OH
2CH3CHO+2H2O CH3COOH+CH3CH2OH![]() CH3COOCH2CH3+H2O CH2=CH2+HBr→CH3CH2Br 分液漏斗 飽和Na2CO3溶液 B、C 加入2~3片碎瓷片 吸水劑 減少水的量使平衡正向移動,提高乙酸乙酯的產率 CH3CH2CH2COOH CH(CH3)2COOH
CH3COOCH2CH3+H2O CH2=CH2+HBr→CH3CH2Br 分液漏斗 飽和Na2CO3溶液 B、C 加入2~3片碎瓷片 吸水劑 減少水的量使平衡正向移動,提高乙酸乙酯的產率 CH3CH2CH2COOH CH(CH3)2COOH
【解析】CH3CH2OH在Cu催化劑條件下發生催化氧化生成A為CH3CHO,CH3CHO進一步氧化生成B為CH3COOH,CH3COOH與CH3CH2OH發生酯化反應生成C為CH3COOC2H5,乙醇發生消去反應生成D為CH2=CH2,乙烯發生加聚反應生成高分子物質E為聚乙烯,
(1)E的結構簡式為![]() ;D為乙烯中含有官能團的名稱為:碳碳雙鍵;(2)寫出下列反應的反應類型:③酯化反應;⑤加成反應。(3)反應的化學方程式:①2CH3CH2OH+O2
;D為乙烯中含有官能團的名稱為:碳碳雙鍵;(2)寫出下列反應的反應類型:③酯化反應;⑤加成反應。(3)反應的化學方程式:①2CH3CH2OH+O2![]() 2CH3CHO+2H2O ;③ CH3COOH+CH3CH2OH
2CH3CHO+2H2O ;③ CH3COOH+CH3CH2OH![]() CH3COOCH2CH3+H2O;D與HBr反應:CH2=CH2+HBr→CH3CH2Br;(4)乙酸乙酯不溶于飽和碳酸鈉溶液,可用分液的方法分離,用到的儀器有燒杯、分液漏斗等,試管B盛飽和Na2CO3溶液,其作用為吸末反應的乙醇和乙酸,乙酸乙酯在飽和碳酸鈉溶液中的溶解度比在水中更小,有利于分層析出,故選BC。試管A中防止液體加熱暴沸所采用的方法是:加入2~3片碎瓷片,其中濃硫酸的作用除催化劑外還有:吸水劑,目的是:減少水的量使平衡正向移動,提高乙酸乙酯的產率;(5)C為CH3COOC2H5,與C互為同分異構且能與Na2CO3反應生成CO2的有機物為酸,結構簡式為:CH3CH2CH2COOH 和 CH(CH3)2COOH。
CH3COOCH2CH3+H2O;D與HBr反應:CH2=CH2+HBr→CH3CH2Br;(4)乙酸乙酯不溶于飽和碳酸鈉溶液,可用分液的方法分離,用到的儀器有燒杯、分液漏斗等,試管B盛飽和Na2CO3溶液,其作用為吸末反應的乙醇和乙酸,乙酸乙酯在飽和碳酸鈉溶液中的溶解度比在水中更小,有利于分層析出,故選BC。試管A中防止液體加熱暴沸所采用的方法是:加入2~3片碎瓷片,其中濃硫酸的作用除催化劑外還有:吸水劑,目的是:減少水的量使平衡正向移動,提高乙酸乙酯的產率;(5)C為CH3COOC2H5,與C互為同分異構且能與Na2CO3反應生成CO2的有機物為酸,結構簡式為:CH3CH2CH2COOH 和 CH(CH3)2COOH。


 新課標快樂提優暑假作業陜西旅游出版社系列答案
新課標快樂提優暑假作業陜西旅游出版社系列答案科目:高中化學 來源: 題型:
【題目】2.0molPCl3和1.0molCl2充入體積不變的密閉容器中,在一定條件下發生下述反應PCl3(g)+Cl2(g)![]() PCl5(g),達平衡時PCl5為0.4mol,如果此時移走1.0molPCl3和0.5molCl2,在相同溫度下再達平衡時PCl5物質的量是
PCl5(g),達平衡時PCl5為0.4mol,如果此時移走1.0molPCl3和0.5molCl2,在相同溫度下再達平衡時PCl5物質的量是
A. 0.4 mol B. 0.2 mol
C. 小于0.2 mol D. 大于0.2 mol小于0.4mol
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】化合物X是一種醫藥中間體,其結構簡式如圖所示。下列 有關化合物X的說法正確的是
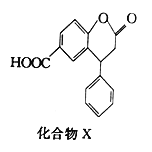
A. 在酸性條件下水解,水解產物只有一種 B. 不能與飽和Na2CO3溶液反應
C. 分子中兩個苯環一定處于同一平面 D. 1 mol化合物X最多能與2 mol NaOH反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】高錳酸鉀是常用的氧化劑。工業上以軟錳礦(主要成分是MnO2)為原料制備高錳酸鉀晶體。中間產物為錳酸鉀。下圖是實驗室模擬制備KMnO4晶體的操作流程:

已知:錳酸鉀(K2MnO4)是墨綠色晶體,其水溶液呈深綠色,這是錳酸根離子(MnO42-)在水溶液中的特征顏色,在強堿性溶液中能穩定存在;在酸性、中性和弱堿性環境下,MnO42-會發生自身氧化還原反應,生成MnO4-和MnO2。
回答下列問題:
(1)KOH的電子式為______,煅燒KOH和軟錳礦的混合物應放在_______中加熱(填標號)。
a.燒杯 b.瓷坩堝 c.蒸發皿 d.鐵坩堝
(2)調節溶液pH過程中,所得氧化產物與還原產物的物質的量之比為______。
(3)趁熱過濾的目的是_______________________________。
(4)已知20℃時K2SO4、KCl、CH3COOK的溶解度分別為11.1g、34g、217g,則從理論上分析,選用下列酸中__________(填標號),得到的高錳酸鉀晶體純度更高。
a.稀硫酸 b.濃鹽酸 c.醋酸 d.稀鹽酸
(5)產品中KMnO4的定量分析:
①配制濃度為0.1250mg·mL-1的KMnO4標準溶液100mL。
②將上述溶液稀釋為濃度分別為2.5、5.0、7.5、10.0、12.5、15.0(單位:mg·L-1)的溶液,分別測定不同濃度溶液對光的吸收程度,并將測定結果繪制成曲線如下。

③稱取KMnO4樣品(不含K2MnO4)0.1250g按步驟①配得產品溶液1000mL,取10mL稀釋至100mL,然后按步驟②的方法進行測定,兩次測定所得的吸光度分別為0.149、0.151,則樣品中KMnO4的質量分數為____。
(6)酸性KMnO4溶液與FeSO4溶液反應的離子方程式為_______________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下圖是元素周期表的一部分,表中列出了①⑨種元素的位置,請根據要求回答問題。
族 周期 | IA | ⅡA | ⅢA | ⅣA | VA | VIA | ⅦA | 0 |
二 | ① | ② | ||||||
三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
四 | ⑨ |
(1)在這些元素中,化學性質最不活潑的原子的原子結構示意圖為________________。
(2)②與④形成的化合物的電子式可表示為 _________________________________________。
(3)這些元素的最髙價氧化物對應的水化物中,酸性最強的是____________________(填化學式)。
(4)寫出⑤與氫氧化鈉溶液反應的化學方程式:_____________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】化學與生產、生活息息相關,下列敘述錯誤的是( )
A. 次氯酸鈉溶液可用于環境的消毒殺菌
B. 二氧化硫不可廣泛用于食品的增白
C. 大量燃燒化石燃料是造成霧霾天氣的一種重要因素
D. 光化學煙霧是由SO2引起的環境污染
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】將貓薄荷中分離出的荊芥內酯與等物質的量的氫氣進行加成,得到的二氫荊芥內酯是一種有效的驅蟲劑,可用于商業生產。下圖為二氫荊芥內酯的一種合成路線:

已知A(C10H16O)的結構中有一個五元環,核磁共振氫譜顯示其側鏈上有四種不同環境的氫,且峰面積比為1:2:3:3。回答下列問題:
(1)A的結構簡式為 ,B含有的官能團的名稱是 。
(2)B與CH3OH發生的反應類型是 ,C與HBr發生的反應類型是 。
(3)由D生成二氫荊芥內酯的化學方程式為 。
(4)D在某催化劑作用下可發生反應生成一種高聚物,其結構簡式為 ,若該高聚物平均相對分子質量約為20000,則其平均聚合度約為 (填標號)。
a.54 b.108 c. 119 d.133
(5)寫出符合以下條件的荊芥內酯的同分異構體的結構簡式 ,其分子中最多有 個碳原子在同一平面上。
①結構中含有苯環 ②只有一個側鏈
③能發生酯化反應 ④不能發生消去反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】利用CO和H2在催化劑的作用下合成甲醇,發生如下反應:CO(g)+2H2(g) ![]() CH3OH(g)。在體積一定的密閉容器中按物質的量之比1∶2充入CO和H2,測得平衡混合物中CH3OH的體積分數在不同壓強下隨溫度的變化情況如右圖所示。下列結論正確的是
CH3OH(g)。在體積一定的密閉容器中按物質的量之比1∶2充入CO和H2,測得平衡混合物中CH3OH的體積分數在不同壓強下隨溫度的變化情況如右圖所示。下列結論正確的是
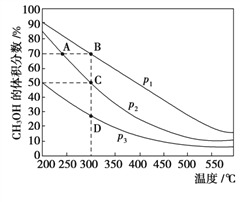
A. 該反應的ΔH>0 B. 平衡常數:K(C)< K(D)
C. 壓強:p1>p2 D. 達到平衡時,反應速率:v(A)> v(B)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】硝酸銨可用作化肥、軍用炸藥、殺蟲劑、冷凍劑,工業制取硝酸銨的工藝流程如下:

(1)N2分子的電子式為_____,NH3分子中含有的化學鍵類型是____________。
(2)乙裝置中發生反應的化學方程式是_________,標準狀況下,該反應生成2.24LNO氣體轉移的電子數目為______。
(3)生產硝酸排放的尾氣中常含有NO、NO2,可用以下兩種方法處理:
方法一:堿液吸收法。寫出用其氧化鈉溶液吸收NO、NO2生成亞硝酸鈉的離子方程式_________。
方法二:甲烷吸收法。在恒壓條件下,將一定量的CH4和NO2兩種氣體置于密閉容器中,發生CH4(g)+2NO2(g)![]() N2(g)+CO2(g)+2H2O(g) ΔH<0,提高NO2轉化率的措施有______(填字母)。
N2(g)+CO2(g)+2H2O(g) ΔH<0,提高NO2轉化率的措施有______(填字母)。
A.增加催化劑表面積 B.減小投料比:n(NO2)/n(CH4)
C.增大壓強 D.升高溫度
(4)配制100mL0.1mol·L-1NH4NO3溶液所需要的玻璃儀器有燒杯、玻璃棒、量筒、膠頭滴管和______。
(5)25℃時,下列關于硝酸銨溶液中的離子濃度關系不正確的是_____ 。
A.Kw/c(H+)>1×10-7mol·L-1 B.c(NO3-)>c(NH4+)>c(H+)>c(OH-)
C.c(H+)=c(OH-)+c(NH3·H2O) D.c(NH4+)+c(H+)=c(NO3-)+c(OH-)
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com