
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解

| ||
| ||
| 品 名 | 氯化亞鐵 |
| 理化特性 | 白色,遇空氣易變成黃色,易吸水,有腐蝕性… |
| 注意事項 | 避免接觸空氣、堿等;聚乙烯塑料桶包裝;避免受熱 |
| ||
| ||
查看答案和解析>>
科目:高中化學 來源:安徽省皖南八校2011屆高三上學期摸底聯考化學試題 題型:013
|
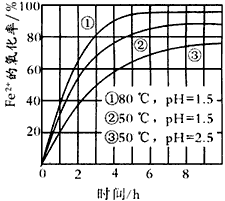
下圖是空氣氧化Fe2+為Fe3+過程中的實驗結果,下列有關說法正確的是
| |
| [ ] | |
A. |
80℃下氧化效果較50℃好,說明該氧化反應是吸熱反應 |
B. |
最佳氧化條件為80℃、pH=1.5下氧化4小時左右 |
C. |
pH=1.5時氧化效果一定比pH=2.5時好 |
D. |
氧化的離子方程式為:Fe2++O2+4H+ |
查看答案和解析>>
科目:高中化學 來源:2013-2014學年湖北省八校高三第二次聯考理綜化學試卷(解析版) 題型:填空題
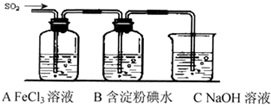
氯化亞銅(CuCl)常用作有機合成工業中的催化劑,是一種白色粉末;微溶于水、不溶于乙醇及稀硫酸;在空氣中迅速被氧化成綠色;見光則分解,變成褐色;下圖是工業上以制作印刷電路的廢液(含Fe3+、Cu2+、Fe2+、Cl-)生產CuCl的流程如下:


根據以上信息回答下列問題:
(1)該生產過程還可以與氯堿工業、硫酸工業生產相結合,工業生產硫酸的方法是______________、氯堿工業的裝置是_____________________。
(2)寫出生產過程中X__________? Y___________ (填化學式)
(3)寫出產生CuCl的化學方程式________________________________________________________。
(4)生產中為了提高CuCl產品的質量,采用______________法快速過濾,析出的CuCl晶體不用水而用無水乙醇洗滌的目的是______________________________;生產過程中調節溶液的pH不能過大的原因是______________________________。
(5)在CuCl的生成過程中理論上不需要補充SO2氣體,其理由是__________________________。
(6)在CuCl的生成過程中除環境問題、安全問題外,你認為還應該注意的關鍵問題是:
_____________________________________。
(7)氯化亞銅的定量分析:
①稱取樣品0.25g(稱準至0.0002g)置于預先放入玻璃珠50粒和10ml過量的FeCl3溶液250ml錐形瓶中,不斷搖動;玻璃珠的作用是____________________________。
②待樣品溶解后,加水50ml,鄰菲羅啉指示劑2滴;
③立即用0.10 mol·L-1硫酸鈰標準溶液滴至綠色出現為終點;同時做空白試驗一次。已知:CuCl + FeCl3 =CuCl2 + FeCl2????? Fe2+ + Ce4+ = Fe3+ + Ce3+
如此再重復二次測得:
| 1 | 2 | 3 |
空白實驗消耗硫酸鈰標準溶液的體積(ml) | 0.75 | 0.50 | 0.80 |
0.25克樣品消耗硫酸鈰標準溶液的體積(ml) | 24.65 | 24.75 | 24.70 |
④數據處理:計算得CuCl的純度為____________。(平行實驗結果相差不能超過0.3%)
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com